
分析 (1)依据溶液稀释过程中所含溶质的物质的量不变计算需要溶液的体积;
(2)依据配制一定物质的量浓度溶液的一般步骤选则需要的仪器;
(3)依据容量瓶构造解答;
(4)依据配制一定物质的量浓度溶液的正确操作步骤结合容量瓶、量筒使用方法解答;
(5)分析操作对溶质的物质的量和溶液体积的影响,依据C=$\frac{n}{V}$进行误差分析.
解答 解:(1)依据溶液稀释过程中所含溶质的物质的量不变得V×18.4mol/L=0.4mol/L×250mL,解得V=5.4mL;
故答案为:5.4;
(2)配制一定物质的量浓度溶液的一般步骤:计算、量取、稀释、冷却、移液、洗涤、定容、摇匀,用到的仪器:烧杯、玻璃棒、10ml 量筒、250ml 容量瓶;还缺少的仪器:胶头滴管;
故答案为:①②③⑥;胶头滴管;
(3)容量瓶上需标有:温度、容积、刻度线;
故答案为:B;
(4)①用量筒量取V ml 浓硫酸,故正确;
②量筒为精密仪器,不能用来溶解固体、稀释浓溶液,故错误;
③立即将稀释后的溶液转入容量瓶中,冷却后溶液体积偏小,溶液浓度偏高,故错误;
④定容时,小心地往容量瓶中加水至刻度1-2cm处,改用胶头滴管,故正确;
⑤平视凹液面定容,故正确;
⑥摇匀时把容量瓶瓶塞塞紧,再振荡,上下颠倒摇匀,故正确;
故选:②③;
(5)①将稀释后的硫酸转移至容量瓶中后,未洗涤烧杯和玻璃棒,导致溶质的物质的量偏小,溶液浓度偏低,故选;
②将烧杯内的稀硫酸向容量瓶中转移时,因操作不当使部分稀硫酸溅出瓶外,导致溶质的物质的量偏小,溶液浓度偏低,故选;
③定容操作不慎使溶液凹液面高于容量瓶刻度线,此时立即将多余的液体吸出,使溶液凹液面与容量瓶刻度线相切,导致溶质的物质的量偏小,溶液浓度偏低,故选;
④定容时仰视容量瓶刻度线,导致溶液的体积偏大,溶液浓度偏低,故选;
故选:①②③④.
点评 本题考查了一定物质的量浓度溶液的配制,明确配制原理及操作步骤是解题关键,注意误差分析的方法和技巧,题目难度不大.


 课堂练加测系列答案
课堂练加测系列答案 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案科目:高中化学 来源: 题型:选择题
| 序号 | 甲 | 乙 |
| ① | SO2 | 石灰水 |
| ② | CO2 | 石灰水 |
| ③ | SO2 | Ba(NO3)2 |
| ④ | NO2 | CaCl2 |
| A. | ②③④ | B. | ②③ | C. | ①③④ | D. | ①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
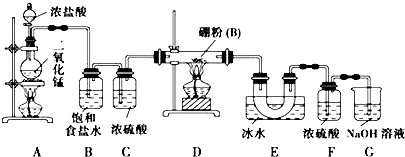
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
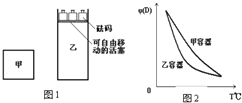 一定温度下,有可逆反应:2A(g)+2B(g)?C(g)+3D(g);△H<0.现将2molA和2mol B充入体积为V的甲容器,将2 mol C和6 mol D充入乙容器并使乙容器在反应开始前的体积为2V(如图1).关于两容器中反应的说法正确的是( )
一定温度下,有可逆反应:2A(g)+2B(g)?C(g)+3D(g);△H<0.现将2molA和2mol B充入体积为V的甲容器,将2 mol C和6 mol D充入乙容器并使乙容器在反应开始前的体积为2V(如图1).关于两容器中反应的说法正确的是( )| A. | 甲容器中的反应先达到化学平衡状态 | |
| B. | 两容器中的反应均达平衡时,平衡混合物中各组份的体积百分组成相同,混合气体的平均相对分子质量也相同 | |
| C. | 两容器达平衡后升高相同的温度,两容器中物质D的体积分数随温度变化如图2所示 | |
| D. | 在甲容器中再充入2 mol A和2 mol B,平衡后甲中物质C的浓度和乙中物质C的浓度相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 联合制碱法中循环使用CO2和NH3,以提高原料利用率 | |
| B. | 硫酸工业中,SO2氧化为SO3时采用常压,因为高压会降低SO2转化率 | |
| C. | 合成氨生产过程中将NH3液化分离,可加快正反应速率,提高N2、H2的转化率 | |
| D. | 炼钢是在高温下利用氧化剂把生铁中过多的碳和其他杂质氧化成气体或炉渣除去 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 磷在氯气中燃烧产生大量的白烟,并放出热量 | |
| B. | 纯净的氢气在氯气中安静燃烧,发出黄色火焰 | |
| C. | 光照新制氯水有气泡逸出,该气体是Cl2 | |
| D. | 实验室制备氯气可用排饱和食盐水法收集 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
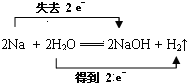 反应中,H2O是氧化剂.
反应中,H2O是氧化剂.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 不慎将酸溅到眼中,应立即用碱液冲洗,边洗边眨眼睛 | |
| B. | 酸式滴定管,碱式滴定管、移液管都是准确量取一定体积液体的仪器,它们在使用时都要进行检查是否漏水、水洗、润洗、注液、调整液面等几个过程 | |
| C. | 除去硬脂酸钠溶液中的甘油方法是:往溶液中加入食盐,过滤 | |
| D. | 常温下,准确称取14.8g Ca(OH)2,配制100mL 2.0 mol/L的Ca(OH)2溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com