
以甲烷燃料电池为例来分析在不同的环境下电极反应式的书写方法:
(1)酸性条件
燃料电池总反应式:CH4+2O2===CO2+2H2O ①
燃料电池正极反应式:O2+4H++4e-===2H2O ②
①-②×2,得燃料电池负极反应式:________________________________________
________________________________________________________________________。
(2)碱性条件
燃料电池总反应式:CH4+2O2+2NaOH===Na2CO3+3H2O ①
燃料电池正极反应式:O2+2H2O+4e-===4OH- ②
①-②×2,得燃料电池负极反应式:_______________________________________
________________________________________________________________________。
(3)固体电解质(高温下能传导O2-)
燃料电池总反应式:CH4+2O2===CO2+2H2O ①
燃料电池正极反应式:O2+4e-===2O2- ②
①-②×2,得燃料电池负极反应式:______________________________________
________________________________________________________________________。 (4)熔融碳酸盐(如:熔融K2CO3)环境下
电池总反应式:CH4+2O2===CO2+2H2O ①
正极电极反应式:O2+2CO2+4e-===2CO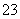 ②
②
①-②×2,得燃料电池负极反应式:_______________________________________
________________________________________________________________________。
科目:高中化学 来源: 题型:
实验室用2.00mol/L的盐酸和漂粉精[成分为Ca(ClO)2、CaCl2]反应生成氯气、氯化钙和水,若产生2.24L(标准状况)氯气,发生反应的盐酸为_________m,l。
查看答案和解析>>
科目:高中化学 来源: 题型:
某烃1mol 最多能和2molHBr 加成反应,其所得的产物又能跟8molBr2 发生取代反应,最后得到一种只含碳、溴两种元素的化合物,则原烃为 ( )
A.C2H2 B.C3H4 C.C3H6 D.C4H6
查看答案和解析>>
科目:高中化学 来源: 题型:
把适合题意的图像填在横线上(用A、B、C、D表示)
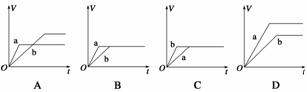
(1)将等质量的两份锌粉a、b分别加入过量的稀硫酸,同时向a中加入少量的CuSO4溶液,产生H2的体积V(L)与时间t(min)的关系是________。
(2)将过量的两份锌粉a、b分别加入定量的稀硫酸,同时向a中加入少量的CuSO4溶液,产生H2的体积V(L)与时间t(min)的关系是_____ ___
___
(3)将(1)中的CuSO4溶液改成CH3COONa溶液,其他条件不变,则图像是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
控制适合的条件,将反应2Fe3++2I-2Fe2++I2设计成如下图所示的原电池。下列判断不正确的是 ( )
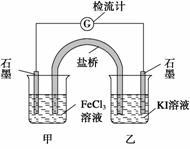
A.反应开始时,乙中石墨电极上发生氧化反应
B.反应开始时,甲中石墨电极上Fe3+被还原
C.检流计读数为零时,反应达到化学平衡状态
D.检流计读数为零后,在甲中溶入FeCl2固体,乙中的石墨电极为负极
查看答案和解析>>
科目:高中化学 来源: 题型:
一种基于酸性燃料电池原理设计的酒精检测仪,负极上的反应为CH3CH2OH-4e-+H2O===CH3COOH+4H+。下列有关说法正确的是 ( )
A.检测时,电解质溶液中的H+向负极移动
B.若有0.4 mol电子转移,则在标准状况下消耗4.48 L氧气
C.电池反应的化学方程式为CH3CH2OH+O2===CH3COOH+H2O
D.正极上发生的反应为O2+4e-+2H2O===4OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
某研究性学习小组根据反应2KMnO4+10FeSO4+8H2SO4===2MnSO4+5Fe2(SO4)3+K2SO4+8H2O设计如下原电池,其中甲、乙两烧杯中各物质的物质的量浓度均为
1 mol·L-1,溶液的体积均为200 mL,盐桥中装有饱和K2SO4溶液。
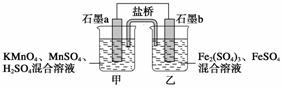
回答下列问题:
(1)此原电池的正极是石墨__________(填“a”或“b”),发生________反应。
(2)电池工作时,盐桥中的SO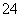 移向________(填“甲”或“乙”)烧杯。
移向________(填“甲”或“乙”)烧杯。
(3)两烧杯中的电极反应式分别为
甲________________________________________________________________________;
乙________________________________________________________________________。
(4)若不考虑溶液的体积变化,MnSO4浓度变为1.5 mol·L-1,则反应中转移的电子为________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液中离子浓度的关系一定正确的是
A. 和
和 溶液中:
溶液中: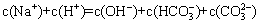
B.一元弱碱MOH对应的盐MCl溶液中: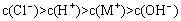
C.等物质的量的一元弱酸HX与其钾盐KX的混合溶液中:
D.pH=3的一元酸HX和pH=11的一元碱MOH等体积混合:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com