
(15分)四种主族元素的性质或结构信息如下:
元素编号 | 相关信息 |
X | 地壳中含量最大的金属元素;元素最高价为+3价。 |
Y | 原子最外层电子数是电子层数的2倍,最外层电子数是X最外层电子数的2倍。 |
Z | 同周期主族元素中原子半径最小,常温下单质呈液态。 |
M | 能从海水中提取的金属元素,单质可在氮气或二氧化碳中燃烧。 |
(1)M的原子结构示意图是 ;上述元素最高价氧化物对应的水化物碱性最强的是(写分子式) (元素用元素符号表示,下同!)。
(2)Y单质溶于热浓的硫酸产生的气体的化学式为 。
(3)能体现Z单质比Y单质活泼性强的一个化学方程式: 。
(4)常温下,不能与X的单质持续发生反应的是(填选项序号) 。
A.CuSO4溶液 B.Fe2O3 C.浓硫酸 D.NaOH溶液 E.Na2CO3固体
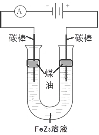
(5)铁元素与Z元素形成化合物FeZ3,FeZ3溶液按下图所示进行试验。装置通电后,连接电源 (填“正极”或“负极”)碳棒边的煤油颜色将变深,另一碳棒附近溶液将出现的现象是 。
(1)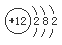 ; Mg(OH)2;(2)SO2(3)S2- + Br2 = S + 2Br-
; Mg(OH)2;(2)SO2(3)S2- + Br2 = S + 2Br-
4)B C E (5)正极 溶液逐渐变成浅绿色。
【解析】
试题分析:根据题意可知:X是Al;Y是S;Z是Br;M是Mg。(1)Mg的原子结构示意图是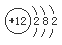 ;在上述元素中金属性最强的元素是Mg,其最高价氧化物对应的水化物碱性最强,化学式是Mg(OH)2;(2)(2)S单质溶于热浓的硫酸发生反应: S+2H2SO4(浓) △3SO2↑+2H2O产生的气体的化学式为SO2,(3)活动性强的能把活动性弱的从化合物中置换出来。能体现Z单质比Y单质活泼性强的一个化学方程式:Na2S+ Br2 = S↓+ 2NaBr;离子方程式是S2- + Br2 = S ↓+ 2Br-。(4)A.Al+ 3CuSO4= 3Cu+Al2(SO4)3.错误。B.Fe2O3与Al发生反应要在高温条件下,在常温不能反应。正确。C.在常温下Al遇浓硫酸会发生钝化,使反应不能在进行。正确。D.2Al+2NaOH+2H2O=2NaAlO2+3H2↑.错误。E.Na2CO3固体与Al不能发生反应。正确。因此选项为B C E。(5)用惰性电极电解FeBr3溶液。由于阴离子的放电能力Br->OH-,所以在与电源的正极相连接的阳极碳棒上发生反应:2Br--2e-=Br2. Br2容易溶解在煤油中,所以煤油颜色将变深,在阴极碳棒上发生反应:2Fe3++2e-=2Fe2+;附近的水溶液由黄色溶液逐渐变成浅绿色。
;在上述元素中金属性最强的元素是Mg,其最高价氧化物对应的水化物碱性最强,化学式是Mg(OH)2;(2)(2)S单质溶于热浓的硫酸发生反应: S+2H2SO4(浓) △3SO2↑+2H2O产生的气体的化学式为SO2,(3)活动性强的能把活动性弱的从化合物中置换出来。能体现Z单质比Y单质活泼性强的一个化学方程式:Na2S+ Br2 = S↓+ 2NaBr;离子方程式是S2- + Br2 = S ↓+ 2Br-。(4)A.Al+ 3CuSO4= 3Cu+Al2(SO4)3.错误。B.Fe2O3与Al发生反应要在高温条件下,在常温不能反应。正确。C.在常温下Al遇浓硫酸会发生钝化,使反应不能在进行。正确。D.2Al+2NaOH+2H2O=2NaAlO2+3H2↑.错误。E.Na2CO3固体与Al不能发生反应。正确。因此选项为B C E。(5)用惰性电极电解FeBr3溶液。由于阴离子的放电能力Br->OH-,所以在与电源的正极相连接的阳极碳棒上发生反应:2Br--2e-=Br2. Br2容易溶解在煤油中,所以煤油颜色将变深,在阴极碳棒上发生反应:2Fe3++2e-=2Fe2+;附近的水溶液由黄色溶液逐渐变成浅绿色。
考点:考查元素的推断、性质、原子结构示意图、离子方程式的书写及电解原理的应用的知识。


科目:高中化学 来源:2013-2014辽宁省大连市高三双基测试化学试卷(解析版) 题型:选择题
下列关于有机化合物的结构、性质的叙述正确的是
A.苯、油脂均能使酸性KMnO4溶液褪色
B.甲烷和Cl2的反应与乙烯和Br2的反应属于同一类型的反应
C.蔗糖、麦芽糖的分子式均为C12H22O11,二者互为同分异构体
D.乙醇、乙酸均能与NaOH反应,因为分子中均含有官能团“—OH”
查看答案和解析>>
科目:高中化学 来源:2013-2014辽宁省五校第二学期期末联考高一化学试卷(解析版) 题型:选择题
把100mL 2mol/L的H2SO4跟过量锌粉反应,在一定温度下,为了减缓反应速率而不影响生成H2的总量,可在反应物中加入适量的
A.硫酸铜溶液 B.硝酸钠溶液 C.醋酸钠溶液 D.氢氧化钠溶液
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省高三高考模拟理综化学试卷(解析版) 题型:填空题
碱式硫酸铁[Fe(OH)SO4]是一种用于污水处理的新型高效絮凝剂。工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁的工艺流程如下:
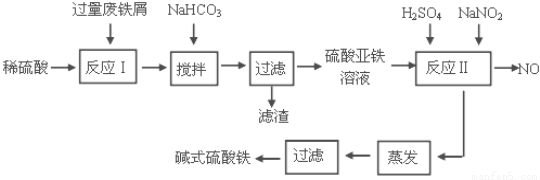
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
开始沉淀 | 2.3 | 7.5 | 3.4 |
完全沉淀 | 3.2 | 9.7 | 4.4 |
回答下列问题:
(1)加入少量NaHCO3的目的是调节pH在 范围内。
(2)反应Ⅱ中加入NaNO2的目的是氧化亚铁离子,写出该反应的离子方程式为
。
(3)实际生产中,反应Ⅱ常同时通入O2以减少NaNO2的用量,若参与反应的O2体积为 11.2 L(标准状况),则相当于节约NaNO2的物质的量为 。
(4)碱式硫酸铁溶于水后生成的Fe(OH)2+离子可部分水解生成Fe2(OH)42+ 聚合离子,该水解反应的离子方程式为 。
(5)在医药上常用硫酸亚铁与硫酸、硝酸的混合液反应制备碱式硫酸铁。根据我国质量标准,产品中不得含有Fe2+及NO3-。为检验所得产品中是否含有Fe2+,应使用的试剂为 。
A.氯水 B.KSCN溶液 C.NaOH溶液 D.酸性KMnO4溶液
(6)为测定含Fe2+和Fe3+溶液中铁元素的总含量,实验操作如下:准确量取20.00mL溶液于带塞锥形瓶中,加入足量H2O2,调节pH<3,加热除去过量H2O2;加入过量KI充分反应后,再用 0.1000 mol·L-1 Na2S2O3标准溶液滴定至终点,消耗标准溶液20.00mL。
已知:
则溶液中铁元素的总含量为 g·L-1。若滴定前溶液中H2O2没有除尽,所测定的铁元素的含量将会
(填“偏高” “偏低” “不变”)
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省高三高考模拟理综化学试卷(解析版) 题型:选择题
制备乙酸乙酯的绿色合成路线之一为:

下列说法不正确的是
A.M的分子式为C6H12O6 B.N的结构简式为CH3COOH
C.④的反应类型属于取代反应 D.淀粉与纤维素互为同分异构体
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省福州市高三5月综合练习理综化学试卷(解析版) 题型:选择题
基于实验现象的推论,你认为合理的是( )
选项 | 实验现象 | 推论 |
A | 乙烯气体可以使溴水褪色 | 乙烯发生取代反应 |
B | 浓硫酸电导率比较低 | 硫酸浓度大时是弱电解质 |
C | 氨气用于喷泉实验 | 氨气极易溶于水 |
D | 硝酸溶液使pH试纸先变红后变白 | 硝酸酸性太强不能用pH试纸检测 |
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省福州八县高二下学期期末考试化学试卷(解析版) 题型:选择题
向盛有硝酸银水溶液的试管里加入氨水,首先形成难溶物,继续添加氨水,难溶物溶解得到无色的透明溶液,下列对此现象的说法正确的是( )
A.反应前后Ag+的浓度不变
B.沉淀溶解后,生成[Ag (NH3) 2] OH难电离
C.配合离子[Ag (NH3)2] + 存在离子键和共价键
D.配合离子[Ag (NH3)2] +中,Ag+提供空轨道,NH3给出孤对电子
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省福州八县高二下学期期末考试化学试卷(解析版) 题型:选择题
已知1 g氢气完全燃烧生成水蒸气时放出热量121 kJ,氧气中1 mol O=O键完全断裂时吸收热量496 kJ,水蒸气中1 mol H-O键形成时放出热量463 kJ,则氢气中1mol H-H键断裂时吸收热量为( )
A.920 kJ B.557 kJ C.436 kJ D.188 kJ
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省高三5月校质检理综化学试卷(解析版) 题型:选择题
下列实验能达到目的的是( )
|
|
|
|
A. 检验SO2具有漂白性 | B.配制0.1 mol?L-1NaOH溶液时定容 | C.分离出碘水中的碘 | D.配制一定浓度硫酸溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com