
����Ŀ����4mol A�����2mol B������2L�������л�ϲ���һ�������·�����Ӧ��2A��g��+B��g��2C��g������2s����C��Ũ��Ϊ0.6molL��1 �� ���м���˵������ȷ���ǣ� ��
A.������A��ʾ��Ӧ��ƽ������Ϊ0.3 molL��1s��1
B.������B��ʾ��Ӧ��ƽ������Ϊ0.3 molL��1s��1
C.2 sʱ����A��ת����Ϊ70%
D.2 sʱ����B��Ũ��Ϊ0.3 molL��1
���𰸡�A
���������⣺v��C��= ![]() mol/��L��s��=0.3 molL��1s��1�� A��ͬһ���淴Ӧ��ͬһʱ���ڸ����ʵķ�Ӧ����֮�ȵ����������֮�ȣ�����v��A��=v��C��=
mol/��L��s��=0.3 molL��1s��1�� A��ͬһ���淴Ӧ��ͬһʱ���ڸ����ʵķ�Ӧ����֮�ȵ����������֮�ȣ�����v��A��=v��C��= ![]() mol/��L��s��=0.3 molL��1s��1 �� ��A��ȷ��
mol/��L��s��=0.3 molL��1s��1 �� ��A��ȷ��
B��ͬһ���淴Ӧ��ͬһʱ���ڸ����ʵķ�Ӧ����֮�ȵ����������֮�ȣ�����v��B��= ![]() v��C��=
v��C��= ![]() ��0.3 molL��1s��1=0.15molL��1s��1 �� ��B����
��0.3 molL��1s��1=0.15molL��1s��1 �� ��B����
C.2sʱ������n��C��=0.6mol/L��2L=1.2mol����μӷ�Ӧ��n��A��=n��C��=1.2mol��A��ת����= ![]() ��100%=
��100%= ![]() =30%����C����
=30%����C����
D.2sʱ������n��C��=0.6mol/L��2L=1.2mol����μӷ�Ӧ��n��B��= ![]() n��C��=
n��C��= ![]() ��1.2mol=0.6mol��ʣ��n��B��=��2��0.6��mol=1.4mol��Bƽ��ʱŨ��C=
��1.2mol=0.6mol��ʣ��n��B��=��2��0.6��mol=1.4mol��Bƽ��ʱŨ��C= ![]() =
= ![]() =0.7mol/L����D����
=0.7mol/L����D����
��ѡA��
�����㾫����������Ŀ����֪���������û�ѧƽ��ļ�������֪ʶ���Եõ�����Ĵ𰸣���Ҫ���շ�Ӧ��ת����=ת��Ũ�ȡ���ʼŨ�ȡ�100%=ת�����ʵ�������ʼ���ʵ�����100%����Ʒ�IJ���=ʵ�����ɲ�������ʵ����������Ͽɵõ���������ʵ�����100%��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и������ʵ���Һ�����������Լ���Ҳ������ɫ��Ӧ���ܽ���������������(����)
A.AgNO3 NaCl BaCl2 NaOH
B.K2CO3 KHCO3 HCl H2SO4
C.Na2CO3 HCl Ba(NO3)2 KCl
D.KNO3 NaCl BaCl2 (NH4)2SO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��ں����������˵������ȷ����
A.��ҵ�Ͽ�ʹ��Һ���������B.NO2 �ܵ��¡��⻯ѧ���������γ�
C.Ũ����������۳�����D.�������ֳƷ���ۣ�������̬����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ʽ̼��ͭ��һ����;�㷺�Ļ���ԭ�ϣ�ʵ�����Է�ͭмΪԭ����ȡ��ʽ̼��ͭ�IJ������£�
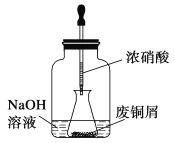
����һ����ͭм������ͭ
��ͼ���ý�ͷ�ι���ȡŨ���Ỻ���ӵ���ƿ�ڵķ�ͭм��(��ͭм����)����ַ�Ӧ����ˣ��õ�����ͭ��Һ��
���������ʽ̼��ͭ���Ʊ�
����Թ��м���̼������Һ������ͭ��Һ��ˮԡ������70 �����ң���0.4 mol��L��1��NaOH��Һ����pH��8.5�������ã����ˣ�����ˮϴ�ӣ���ɣ��õ���ʽ̼��ͭ��Ʒ��
���������գ�
(1)д��Ũ������ͭ��Ӧ�����ӷ���ʽ___________________________________________��
(2)��ͼװ����NaOH��Һ��������_________________________��
(3)������У�ˮԡ��������������________��________(���ȡ��г�������ʯ��������)��ˮԡ���ȵ��ŵ���_______________________��
(4) ��֪��CuCO3��Cu(OH)2���Ⱦ��ֽ⣬�����ж���CuO���ɡ���ʽ̼��ͭ�ɱ�ʾΪxCuCO3��yCu(OH)2��zH2O��x��y��zȡ���������ⶨ��ʽ̼��ͭ��ɵķ����ж��֣��ֲ���������ԭ������ش��������⣺����֪M��Cu����63.5 g��mol��1����
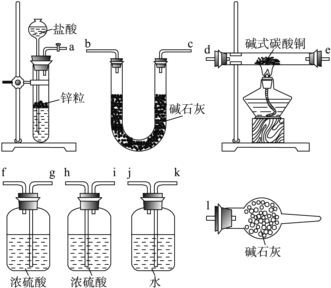
��д��xCuCO3��yCu��OH��2��zH2O��������Ӧ�Ļ�ѧ����ʽ��__________________��
��ʵ��װ�������������������Ӷ��ɣ������������������˳���ǣ����������ӿ���ĸ��ţ����� a ������ ���� ������ ���� ������ ���� ������ ���� ������ ���� ������ l ��_____
�۳�ȡ23.9 gij��ʽ̼��ͭ��Ʒ����ַ�Ӧ��õ�12.7 g���������4.4 g������̼��7.2 gˮ������Ʒ�Ľᾧˮ����Ϊ______ g����ѧʽΪ____________��
��ijͬѧ�Ե���������������������ȫ�����������ⶨ��ʽ̼��ͭ����ɣ�����Ϊ�Ƿ���У�__________������С������С�����˵������________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2015��ŵ�������������������ȡ�Ŀ�ű��ҩ�����صĽṹ��ʽ���ü���ʽ��ʾ��ͼ��
��1�������صķ���ʽΪ ��
��2��Ϊ����������� ![]() ����Ҫ���л��ϳ��������ǻ��������ǻ��ķ�Ӧ��������ѡ���ţ�
����Ҫ���л��ϳ��������ǻ��������ǻ��ķ�Ӧ��������ѡ���ţ�
��ȡ�� �ڼӳ� ����ȥ ������ �ݻ�ԭ
��3������٢۵������� ��
��4��C8H10O3�Ľṹ��ʽ�� ��
��5��C��������Ȼ���ȩ��Ϊͬ���칹�壬д����������������C��һ�ֽṹ��ʽ ��
���б���������ˮ�⣻���ܷ���������Ӧ������FeCl3��Һ������ɫ��Ӧ��
��6���л���ȩ ![]() �Ǻϳ������ص��м�ԭ��֮һ��д���ɱ���ȩ��������Ϊԭ�ϣ��Ʊ��л���ȩ�ĺϳ�·������ͼ�����Լ����ã� �� ��֪���ʻ�����H�ɷ�����Ӧ��
�Ǻϳ������ص��м�ԭ��֮һ��д���ɱ���ȩ��������Ϊԭ�ϣ��Ʊ��л���ȩ�ĺϳ�·������ͼ�����Լ����ã� �� ��֪���ʻ�����H�ɷ�����Ӧ�� ![]()

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����п����������þ���ֽ�����������ɵĻ����10�ˣ������������ᷴӦ�����������ڱ�״����Ϊ11.2L����������һ�����еĽ�����( )
A. п B. �� C. �� D. þ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����е��뷽��ʽ��ȷ���ǣ� ��
A. MgSO4=Mg��2��SO4-2
B. Ba(OH)2=Ba2����OH2-
C. Al2(SO4)3=2Al3����3SO42-
D. KClO3=K����Cl����3O2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ��������м��ȡĪ���ε���Ҫ�����ǣ�����м��ϡ����ˮԡ������ȡFeSO4��FeSO4��(NH4)2SO4�Ե����ʵ�����Ϻ���ȣ�Ũ���ᾧ��Ī���Ρ�
��1��������м��ϡ����ʱ������Ҫ��������ˮ��ԭ����
��2��ʵ����Ϊ����������������ʧ�����˷�������������ҺʱӦע�����������
��3��Ϊ��ֹFe2����������ʵ���пɲ�ȡ�Ĵ�ʩ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������У����������ƶ���Cl������(����)
A. KCl����B. Һ̬�Ȼ���C. CaCl2��ҺD. NaClO3��Һ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com