
����Ŀ��ij��ѧ��ȤС��ij�Ա��һ���ʯ���۲���۷��ָÿ�ʯ��Ӳ�ҳʺ��ɫ��Ͷ��ˮ��û���κα仯������ˮ�м�Ũ��������������ʯ�����ܽ⣬���д�����ɫ�������ɣ�ѧ���²�ÿ�ʯ������CaCO3��SiO2��Fe2O3���ֳɷ���ɣ������ʵ��֤��CaCO3��������ֳɷ֣� ����ѡ����������Լ����ձ����Թܡ����������ιܡ�ҩ�ס�©����©���ܣ�2 molL��1���ᡢ2molL��1NaOH��Һ��2%��KSCN��Һ��
��1����ʵ�鷽������������ʾ��ͼ��ʾ����д��ÿ�������Լ������ƻ�ѧʽ�� 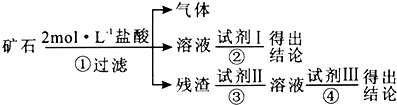
�Լ������Լ������Լ��� ��
��2������²��dz����ģ��Ը�������ʵ�鷽��������ʵ�������Ԥ������ͽ��ۣ�
��� | ʵ����� | Ԥ������ͽ��� |
�� | ȡ������ʯ��ϸ���� | �д�����ɫ�������ɣ����ػ� |
�� | ||
�� | ||
�� |
���𰸡�
��1��2%��KSCN��Һ��2mol?L��1NaOH��Һ��2mol?L��1����
��2��ȡ�ٲ�������Һ�������ڽྻ�Թ��У����μӼ���2%��KSCN��Һ����Һ��Ϊ��ɫ��˵��ԭ��ʯ���ܺ���Fe2O3��ȡ�ٲ����ò���������������ձ��У���������2 mol?L��1NaOH��Һ����ֽ��裻���������ȫ�ܽ���2 mol?L��1NaOH��Һ��������ɫ��Һ��ȡ�۲�������ɫ��Һ�������ڽྻ�Թ��У��ý�ͷ�ιܵ���2 mol?L��1�������������а�ɫ��״�������Ҳ����ڹ������ᣬ˵��ԭ��ʯ�п��ܺ���SiO2
���������⣺��1��Fe2O3���������ᣬFe3+��������Һ�У�����SCN�����飬�Ӷ�˵����ʯ��Fe2O3 �� SiO2���������ᣬ��Ϊ�������˳���Ϊ��һ��ȷ�ϣ��Ƿ����SiO2 �� ����NaOH��Һ����ַ�Ӧ���ټ����ᣬ��������˰�ɫ��״��������ΪH2SiO3 �� ˵����ʯ����SiO2 �� ���Դ��ǣ�2%��KSCN��Һ��2 molL��1 NaOH��Һ��2 molL��1�����2�������ʯ�к���Fe2O3 �� �����ᷴӦ�����Ȼ�����ȡ�������������еĢ���2%KSCN��Һ����Һ��ΪѪ��ɫ��������������
�����Ƿ��ж������裬ȡ�ٲ����ò���������������ձ��У���������2 molL��1NaOH��Һ����ֽ��裬���������ȫ�ܽ���2 molL��1NaOH��Һ��������ɫ��Һ��
Ȼ��ȡ�۲�������ɫ��Һ�������ڽྻ�Թ��У��ý�ͷ�ιܵ���2 molL��1�������������а�ɫ��״�������Ҳ����ڹ������ᣬ��˵�����ж������裬
���Դ��ǣ�
�� | ȡ�ٲ�������Һ�������ڽྻ�Թ��У����μӼ���2%��KSCN��Һ | ��Һ��Ϊ��ɫ��˵��ԭ��ʯ���ܺ���Fe2O3 |
�� | ȡ�ٲ����ò���������������ձ��У���������2 molL��1NaOH��Һ����ֽ��� | ���������ȫ�ܽ���2 molL��1NaOH��Һ��������ɫ��Һ |
�� | ȡ�۲�������ɫ��Һ�������ڽྻ�Թ��У��ý�ͷ�ιܵ���2 molL��1���������� | �а�ɫ��״�������Ҳ����ڹ������ᣬ˵��ԭ��ʯ�п��ܺ���SiO2 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������[NaaFeb��SO4��c��OH��d]���г��������������ʿ졢�����˵��ص㣮ij�о�С���Ƚ�ij��ˮ��Fe2+����ΪFe3+ �� �ټ���Na2SO4ʹ�����ɻ�����������ȥ����Ϊ�ⶨ������������ɣ���С�����������ʵ�飺
�ٳ�ȡ12.125g��Ʒ����������ȫ�ܽ�����250.00mL��ҺA��
����ȡ25.00mL��ҺA������������KI������0.2500molL��1Na2S2O3��Һ�ζ����ɵ�I2����Ӧԭ��ΪI2+2Na2S2O3=2NaI+Na2S4O6��������30.00mL Na2S2O3��Һ���յ㣮
����ȡ50.00mL��ҺA����������BaCl2��Һ��ַ�Ӧ���ˣ������ó���ϴ�ӡ�����Ƶ�������Ϊ2.330g��
��1��NaaFeb��SO4��c��OH��d��a��b��c��d֮��Ĵ�����ϵʽΪ ��
��2��ͨ������ȷ�����������Ļ�ѧʽ��д��������̣���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ѡ�õij����Լ���ʵ���������ȷ���ǣ�������Ϊ���ʣ��� ��
���� | �����Լ�(������ | �������� | |
A | CO2(HC1) | ����������Һ | ����ͨ��ʢ������������Һ��ϴ��ƿ |
B | K2CO3(KCl) | ϡ���� | ����ϡ���ᡢ�������ᾧ |
C | FeSO4(CuSO4) | ���� | �������۲����� |
D | Zn(Fe) | ϡ���� | ����ϡ���ᣬ���� |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Fe2+��I����Br������Һ��ͨ��������������Һ�и������ӵ����ʵ����仯��ͼ��ʾ�й�˵����ȷ���ǣ� �� 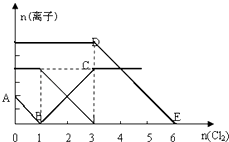
A.�߶�BC����Cl����Ŀ�ı仯���
B.ԭ�����Һ��c��FeBr2��=6mol/L
C.��ͨ��Cl22molʱ����Һ���ѷ��������ӷ�Ӧ�ɱ�ʾΪ��2Fe2++2I��+2Cl2=2Fe3++I2+4 Cl��
D.ԭ��Һ��n��Fe2+����n��I������n��Br����=2��2��3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�����������7mol/L������100mL��һ��������ǡ����ȫ�ܽ⣬������Һ��ͨ��0.56L��״���µ�����ʱ���պ�ʹ��Һ��Fe2+��ȫת��ΪFe3+ �� ���������Ļ�ѧʽ�ɱ�ʾΪ�� ��
A.FeO
B.Fe3O4
C.Fe4O5
D.Fe5O7
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������л���������ȷ���ǣ� ��
A.![]() 2���һ�����
2���һ�����
B.CH3CH2CH2CH2OH 1������
C.![]() ����ױ�
����ױ�
D.![]() 2������2����ϩ
2������2����ϩ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪ij�л��� A���� C��H��O Ԫ�أ����������ܶ�����ͬ״���������ܶȵ�30����������Ԫ�ص���������Ϊ26.7%������л���ķ���ʽΪ �� Ϊ�ⶨ A �Ľṹ�����˴Ź������ף��������������շ壬�Ҹ����ʿ�������Ʒ�Ӧ����A���ܵĽṹ��ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ���Ի�ͭ����Ҫ�ɷ�CuFeS2��Ϊԭ���Ʊ�CuSO45H2O����Ҫ������ͼ�� 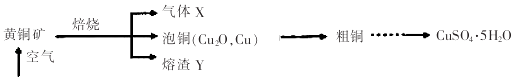
��1������װ�ò���������������X����������ţ��� 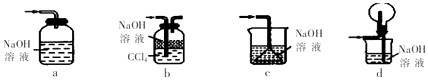
��2������Y�ijɷ�ΪFe2O3��FeO��ѡ���ṩ���Լ������ʵ����֤�����к���FeO��д���й�ʵ���������������ۣ�
�ṩ���Լ���ϡ���ᡢϡ���ᡢKSCN��Һ��KMnO4��Һ��NaOH��Һ����ˮ�� ��
��3�����ͭ�м������������Ļ�����Һ��ȡ����ͭʱ�����ʲ��μӷ�Ӧ����������HNO3��H2SO4��������ʵ���֮��Ϊ
��4���õζ����ⶨ���ò�Ʒ��CuSO45H2O�ĺ�������ȡag��Ʒ���100mL��Һ��ȡ��20.00mL����c mol��L��l�ζ���EDTA�� H2Y2��������Һ�ζ����յ㣨�ζ����������ʷ�Ӧ�������ĵζ���bmL���ζ���Ӧ���£�Cu2++H2Y2��=CuY2��+2H+ �� ��CuSO45H2O��������Ϊ �� �ζ���������ˮϴ�Ӻ�ֱ��ע�����Һ����ᵼ�²ⶨ���ƫ �� ���ƫ�ߡ�����ƫ�͡��͡���Ӱ�족��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com