
已知异丙苯的结构简式如下,下列说法错误的是

A. 异丙苯的分子式为C9H12
B. 异丙苯的沸点比苯高
C. 异丙苯中碳原子可能都处于同一平面
D. 异丙苯和苯为同系物
科目:高中化学 来源:2017届广西省桂林市高三上第二次月考化学试卷(解析版) 题型:填空题
氯化亚铜(CuCl)常用作有机合成工业中的催化剂,是一种白色粉末;微溶于水、不溶于乙醇及稀硫酸。下图是工业上用印刷电路的蚀刻液的废液(含Fe3+、Cu2+、Fe2+、Cl-)生产CuCl的流程:
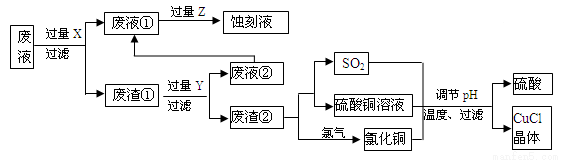
按要求回答下列问题:
⑴ 废液①的主要含有的金属阳离子是__________(填化学符号,下同);废渣①的成分是_____________,Y为__________。
⑵废液①与Z反应的离子方程式为:______________________。
⑶ 写出废渣②生成二氧化硫的化学方程式_____________________。
⑷ 为得到纯净的CuCl晶体,可用下列_________(填序号)进行洗涤。
a.纯净水 b.乙醇 c.稀硫酸 d.氯化铜溶液
⑸ 生产过程中调节溶液的pH不能过大的原因是___________________。
⑹ 写出产生CuCl的离子方程式_______________________。
⑺ 氯化亚铜的定量分析:
① 称取样品0.25g加入10mL过量的FeCl3溶液250mlL锥形瓶中,不断摇动;
② 待样品溶解后,加水50mL和2滴指示剂;
③ 立即用0.10 mol·L-1硫酸铈标准溶液滴至绿色出现为终点;
④ 重复三次,消耗硫酸铈溶液平均体积为25.00mL。
已知:CuCl的分子式量为99;CuCl + FeCl3 = CuCl2 + FeCl2; Fe2+ + Ce4+ = Fe3+ + Ce3+。
则CuCl的纯度为____________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年吉林省高二上9月月考化学卷(解析版) 题型:实验题
燃料电池是符合绿色化学理念的新型发电装置。下图为氢氧燃料电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:
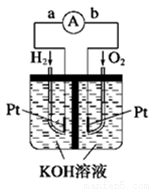
(1)氢氧燃料电池的能量转化主要形式是 ,在导线中电子流动方向为 (用a、b 表示)。
(2)负极反应式为 ,正极反应式为 ;
(3)该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能。因此,大量安全储氢是关键技术之一。金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
Ⅰ.2Li+H2
 2LiH Ⅱ.LiH+H2O
2LiH Ⅱ.LiH+H2O LiOH+H2↑
LiOH+H2↑
反应Ⅰ中的还原剂是 ,反应Ⅱ中的氧化剂是 ;
(4)如果该电池是甲烷-氧气燃料电池,负极反应式为 ;
(5)如果该电池是肼(N2H4)-氧气燃料电池,负极反应式为 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年吉林省高二上9月月考化学卷(解析版) 题型:选择题
100 mL浓度为2 mol·L-1的盐酸跟过量的锌片反应,为加快反应速率,又不影响生成氢气的总量,可采用的方法是
A.加入适量的6 mol·L-1的盐酸 B.加入数滴氯化铜溶液
C.加入适量蒸馏水 D.加入适量的氯化钠溶液
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高二上9月月考化学卷(解析版) 题型:填空题
联氨(又称联肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题:
(1)联氨分子的电子式为_____________,其中氮的化合价为__________。
(2)实验室可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为___________。
(3)①2O2(g)+N2(g)=N2O4(l) △H1
②N2(g)+2H2 (g)=N2H4(l) △H2
③O2(g)+2H2(g)=2H2O(g) △H3
④2 N2H4(l) + N2O4(l)= 3N2(g)+ 4H2O(g) △H4=-1048.9kJ/mol
上述反应热效应之间的关系式为△H4=________________,联氨和N2O4可作为火箭推进剂的主要原因为____________________。
(4)联氨为二元弱碱,在水中的电离方程式与氨相似。联氨与硫酸形成的酸式盐的化学式为 。
(5)联氨是一种常用的还原剂,可用于处理高压锅炉水中的氧,防止锅炉被腐蚀。理论上1kg的联氨可除去水中溶解的O2 kg;与使用Na2SO3处理水中溶解的O2相比,联氨的优点是 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高二上9月月考化学卷(解析版) 题型:选择题
已知X+、Y2+、Z-、W2-四种离子均具有相同的电子层结构,下列关于X、Y、Z、W 四种元素的描述,不正确的是
A. 原子半径:X>Y>Z>W
B. 原子序数:Y>X>Z>W
C. 原子最外层电子数:Z>W>Y>X
D. 金属性:X>Y,还原性:W2->Z-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高二上9月月考化学卷(解析版) 题型:选择题
美国科学家将铅和氪两种元素的原子核对撞,获得了一种质子数为118、质量数为293的新元素,该元素原子核内的中子数和核外电子数之差为
A. 47 B. 175 C. 61 D. 57
查看答案和解析>>
科目:高中化学 来源:2017届海南中学高三上第二次月考化学试卷(解析版) 题型:填空题
FeCl3是一种重要的化工产品。
(1)电子工业用FeCl3腐蚀铜的原理制造印刷电路板,写出FeCl3与Cu反应的离子方程式:_______________。
(2)某校同学为测定FeCl3腐蚀铜后所得溶液的组成,进行了如下实验:
首先取少量待测溶液,滴入KSCN溶液呈红色,则可推断溶液中含有的金属阳离子是______________。
在此基础上,又进行了定量组成的测定:
①取50.0 mL待测溶液,向其中加入足量的AgNO3溶液,得白色沉淀,过滤、干燥、称量,沉淀质量为43.05 g。溶液中c(Cl-)=___________。
②再取50.0 mL待测溶液,向其中加入过量稀硝酸,得到0.448 L(标准状况下)的一种无色气体。写出反应的离子方程式:_____________,待测溶液中c(Cu2+)=_________。
查看答案和解析>>
科目:高中化学 来源:2017届湖南省邵阳市高三上第一次月考化学试卷(解析版) 题型:选择题
向等物质的量浓度的NaOH和Na2CO3的混合溶液中加入稀盐酸。下列离子方程式与事实不相符的是 ( )
A.OH-+CO32-+2H+ HCO3-+H2O
HCO3-+H2O
B.2OH-+CO32-+3H+ HCO3-+2H2O
HCO3-+2H2O
C.2OH-+CO32-+4H+ CO2↑+3H2O
CO2↑+3H2O
D.OH-+CO32-+3H+ CO2↑+2H2O
CO2↑+2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com