
(本题共12分)某化学小组的同学模拟工业制硝酸设计了如下图所示的装置。已知:
CaCl2+ nH2O→CaCl2·nH2O;CaCl2+ 8NH3→[Ca(NH3)8]Cl2
根据题意完成下列填空:

33.分液漏斗中氨水的浓度为9.0mol/L。现用质量分数为0.35、密度为0.88g/cm3的氨水配制9.0mol/L的氨水100mL,需要的定量仪器有 (选填编号)。
a.100mL容量瓶 b.10mL量筒 c.50mL量筒 d.电子天平
34.受热时,乙中反应的化学方程式为 。
35.实验开始先加热催化剂,当催化剂达红热时再打开分液漏斗活塞并移走酒精灯,可观察到的现象有 。
36.干燥管甲的作用是 ;丙中盛放的药品为 (选填下列编号),其目的是 。
a.浓H2SO4 b.无水CaCl2 c.碱石灰 d.无水CuSO4
37.丁中除了NO之外,还可能存在的气体有 (填写化学式)。烧杯中发生反应的化学方程式 、 。
33、a、c (1分×2) 34、4NH3+5O2 4NO+6H2O(1分)
4NO+6H2O(1分)
35、乙中Cr2O3仍能保持红热状态;丁的烧瓶中气体由无色转化为红棕色;试管里的石蕊试液由紫色变为红色。(1分×3)
36、干燥氧气和氨气的混合气体(1分); b(1分);吸收水及多余NH3(1分)。
37、N2、O2、NO2 (N2O4) (1分) 2NO2+ 2NaOH→NaNO2+ NaNO3+ H2O(1分);
NO+ NO2+ 2NaOH→2NaNO2+ H2O(1分)
【解析】
试题分析:33、配制9.0mol/L的氨水100mL,需要的定量仪器有100ml容量瓶。需要氨水的体积是 ,所以还需要50ml量筒,答案选ac。
,所以还需要50ml量筒,答案选ac。
34、过氧化钠吸水生成氢氧化钠和氧气,生成氧气和氨气在催化剂作用下发生催化氧化生成NO和水,反应的化学方程式为4NH3+5O2 4NO+6H2O。
4NO+6H2O。
35、由于反应是放热反应,因此当催化剂达红热时再打开分液漏斗活塞并移走酒精灯,可观察到的现象乙中Cr2O3仍能保持红热状态;生成的NO被氧气氧化生成红棕色NO2,NO2溶于水生成硝酸和NO,所以还能观察到的实验现象是丁的烧瓶中气体由无色转化为红棕色;试管里的石蕊试液由紫色变为红色。
36、由于进入乙装置的氨气和氧气含有水蒸气,因此干燥管甲的作用是干燥氧气和氨气的混合气体。反应中氨气过量,氨气是碱性气体,会干扰后续实验,所以干燥管丙中的固体药品原来吸收多余的氨气,则需要盛放的药品是无水氯化钙,答案选b。
37、由于氨气再与氧气反应时也可能被氧化为氮气,而生成的NO又易被氧化生成NO2,所以丁中除了NO之外,还可能存在的气体有N2、O2、NO2 (N2O4)。NO、NO2均是有毒气体,所以烧杯中氢氧化钠的作用是吸收尾气,有关反应的化学方程式为2NO2+ 2NaOH→NaNO2+ NaNO3+ H2O、NO+ NO2+ 2NaOH→2NaNO2+ H2O。
考点:考查氨气制备以及性质实验方案设计与探究


 ABC考王全优卷系列答案
ABC考王全优卷系列答案科目:高中化学 来源:2014-2015学年浙江省高三1月份阶段测试化学试卷(解析版) 题型:选择题
下列关于有机化合物的结构、性质的叙述正确的是
A.苯、油脂均能使酸性KMnO4溶液褪色
B.甲烷和Cl2的反应与乙烯和Br2的反应属于同一类型的反应
C.蔗糖、麦芽糖的分子式均为C12H22O11,二者互为同分异构体
D.乙醇、乙酸均能与NaOH稀溶液反应,因为分子中均含有官能团“—OH ”
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市闸北区高三上学期期末化学试卷(解析版) 题型:填空题
(本题共12分)葡萄糖酸钙是一种可促进骨骼生长的营养物质。葡萄糖酸钙可通过以下反应制得:C6H12O6(葡萄糖)+Br2+H2O→C6H12O7(葡萄糖酸)+2HBr
2C6H12O7(葡萄糖酸)+CaCO3→ (C6H11O7)2 Ca (葡萄糖酸钙)+H2O+CO2
相关物质的溶解性见下表:
物质名称 | 葡萄糖酸钙 | 葡萄糖酸 | 溴化钙 | 氯化钙 |
水中的溶解性 | 可溶于冷水 易溶于热水 | 可溶 | 易溶 | 易溶 |
乙醇中的溶解性 | 微溶 | 微溶 | 可溶 | 可溶 |
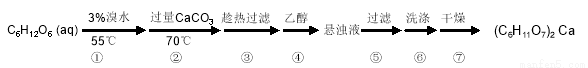
实验流程如下:
请回答下列问题:
32.第②步中所加CaCO3还发生了其他反应,写出其中一个主要反应的方程式________;充分反应后CaCO3固体需有剩余,目的是______________________;
33.第③步需趁热过滤,原因是______________________;
34.第④步加入乙醇的作用是______________________;
35.第⑥步中,下列洗涤剂最合适的是________。
A.冷水 B.热水 C.乙醇 D.乙醇-水混合溶液
锌是人体健康所必需的元素,葡萄糖酸锌是一种常用的补锌剂,对婴儿及青少年的智力和身体发育有重要作用。工业上以葡萄糖酸钙为原料通过如下两步制备葡萄糖酸锌:

步骤1:充分反应后,过滤除去CaSO4沉淀。步骤2:将葡萄糖酸溶液与ZnO混合。
36.步骤2中,待其充分反应后,须继续加入葡萄糖酸溶液至pH为5.8,目的是 。
37.下列物质可替代ZnO的是 (填字母)。
a.NH3·H2O
b.Zn(OH)2
c.NaOH
d.ZnSO4
e.ZnCO3
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市闸北区高三上学期期末化学试卷(解析版) 题型:选择题
生活处处有化学,下列说法正确的是
A.氢氧化铝可作胃酸过多的中和剂
B.福尔马林可作食品的保鲜剂
C.用聚乙烯塑料代替聚乳酸塑料可减少白色污染
D.煎炸食物的花生油、牛油都属于可皂化的饱和酯类
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市普陀区高三一模化学试卷(解析版) 题型:选择题
H2C2O4是一种二元弱酸,NaHC2O4溶液显酸性。现测得某溶液中存在的离子有C2O42-、HC2O4-、OH-、Na+、H+。下列判断正确的是
A.该溶液的溶质只能是Na2C2O4或NaHC2O4或两者的混合物
B.该溶液可能显酸性、碱性或中性
C.溶液中一定存在c(Na+) > c(HC2O4- )
D.溶液中一定存在c(H+) - c(OH-) > c(HC2O4- ) - c(Na+)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市普陀区高三一模化学试卷(解析版) 题型:选择题
取一定量FeO和Fe2O3的混合物,在H2流中加热充分反应。冷却,称得剩余固体比原混合物质量减轻1.200g。若将同量的该混合物与盐酸反应完全,至少需1mol/L盐酸的体积为
A.37.5mL B.75mL C.150mL D.300mL
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市嘉定区高三一模化学试卷(解析版) 题型:填空题
坐落在沿海地区的某纯碱厂是我国重点大型企业,其生产工艺流程可简要表示如图所示:

34.上述生产纯碱的方法称________________;副产品的一种用途为_______________。
35.使原料氯化钠的利用率从70%提高到90%以上,主要是设计了__________(填上述流程中的编号)的循环。从沉淀池中取出沉淀的操作所需玻璃仪器有烧杯、_______________________等。
36.母液中含有NaCl、NH4Cl、_____________________(以化学式表示)。向母液中通入氨气,加入细小食盐颗粒,冷却析出副产品,通氨气的作用有___________
硫酸铜晶体(CuSO4·xH2O),采用加热法测定该晶体中结晶水x的值,实验数据记录如下:
坩埚质量 | 坩埚与晶体总质量 | 加热后坩埚与固体总质量 | ||
第一次称量 | 第二次称量 | |||
11.710g | 22.700g | 18.621g | a | |
37.若无需再进行第三次称量,则a的数值范围应为 。
38.若加热后坩埚与固体总质量为18.620g,计算x 的实测值 (保留二位小数),相对误差 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市虹口区高三上学期期末考试化学试卷(解析版) 题型:选择题
兴奋剂是体育比赛中禁用的药物,有一种兴奋剂的结构如图。关于它的说法中正确的是

A.该有机物能发生银镜反应
B.分子中有4个碳碳双键
C.既能发生还原反应,又能发生氧化反应
D.1 mol 该物质最多跟6 mol氢气发生反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com