
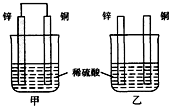
| A、两烧杯中铜片表面均无气泡产生 |
| B、甲中铜片是正极,乙中铜片是负极 |
| C、两烧杯中溶液的酸性均减弱 |
| D、产生气泡的速度甲比乙慢 |


科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
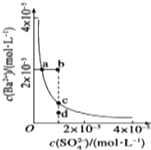
| A、通过加水稀释可以使溶液由b点变到a点 |
| B、加入适量BaCl2(固体) 可以使溶液由d点变到c点 |
| C、d点无BaSO4沉淀生成 |
| D、a点对应的Ksp等于c点对应的Ksp |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、ZO3-的空间构型是平面三角形 |
| B、Z、M、W三种元素的第一电离能由大到小的顺序是W>M>Z |
| C、W所在族的氢化物中沸点最低的是HCl |
| D、在ZX4W中,各种粒子间的相互作用力包括极性共价键、配位键、离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、若向烧杯a中滴加几滴酚酞试液,溶液呈红色 |
| B、装置工作过程中,烧杯b中电极发生氧化反应 |
| C、烧杯c的左侧的电极反应为2H2O+2e-=2OH-+H2↑ |
| D、烧杯c的右侧溶液由黄色变为橙色,是因为该侧电极上发生了反应2CrO42-+H2O-2e-=Cr2O72-+2OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②⑤ | B、②③④ |
| C、①③④⑤ | D、①③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、使淀粉-KI试纸变蓝色 |
| B、加入KI溶液后变蓝色 |
| C、加入硝酸银溶液产生黄色沉淀 |
| D、加入溴水后液体变蓝色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
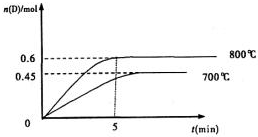 在容积为2L的密闭容器中,进行如下反应:
在容积为2L的密闭容器中,进行如下反应:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com