
| A、焰色反应为黄色,则该物质一定为钠的化合物 |
| B、加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH4+ |
| C、加入稀盐酸酸化的氯化钡溶液有白色沉淀产生,则一定含有SO42- |
| D、加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+ |


科目:高中化学 来源: 题型:
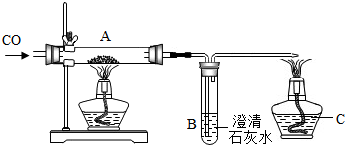 用如图装置测定某铁的氧化物中铁元素和氧元素的质量比,记录如下:
用如图装置测定某铁的氧化物中铁元素和氧元素的质量比,记录如下:查看答案和解析>>
科目:高中化学 来源: 题型:
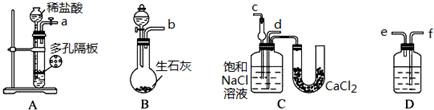
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||

查看答案和解析>>
科目:高中化学 来源: 题型:
 影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进行探究.他们利用他们利用Cu、Fe、Mg和不同浓度的硫酸(0.5mol/L、2mol/L、18.4mol/L),设计实验方案来研究影响反应速率的因素.
影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进行探究.他们利用他们利用Cu、Fe、Mg和不同浓度的硫酸(0.5mol/L、2mol/L、18.4mol/L),设计实验方案来研究影响反应速率的因素.| 实 验 步 骤 | 现 象 | 结 论 |
| ①分别取等体积的2mol/L硫酸于试管中; ②分别投入大小、形状相同的Cu、Fe、Mg. | 反应快慢: Mg>Fe>Cu | 反应物的性质越活泼,反应速率越快. |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、pH=7的溶液中Al3+、Cl-、SO42-、HCO3- |
| B、由水电离出来的c(H+)=10-12mol/L的溶液中Na+、HCO3-、SO42-、K+ |
| C、pH=0的溶液中Na+、K+、Fe2+、ClO- |
| D、c(OH-)=10-2mol/L的溶液中S2-、SO42-、S2O32-、Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
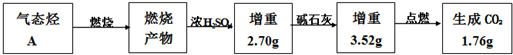
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、正极反应为:4OH-═O2+2H2O+4e- |
| B、放电时CO32- 向负极移动 |
| C、电池供应1mol水蒸气,转移的电子数为4mol |
| D、放电时CO32- 向正极移动 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com