
| A£® | Ńō¼«·¢ÉśŃõ»Æ·“Ó¦£¬Ęäµē¼«·“Ó¦Ź½Ö÷ŅŖŹĒ£ŗNi-2e-=Ni2+ | |
| B£® | µē½ā¹ż³ĢÖŠ£¬Ńō¼«ÖŹĮæµÄ¼õÉŁÓėŅõ¼«ÖŹĮæµÄŌö¼Ó²»ĻąµČ | |
| C£® | µē½āŗó£¬ČÜŅŗÖŠ“ęŌŚµÄ½šŹōŃōĄė×ÓÖ»ÓŠFe2+”¢Ni2+ŗĶZn2+ | |
| D£® | µē½āŗ󣬵ē½ā²Ūµ×²æµÄŃō¼«ÄąÖŠÖ»ÓŠPt |
·ÖĪö A”¢Ńō¼«Ź§Č„µē×Ó·¢ÉśŃõ»Æ·“Ó¦£¬øł¾Ż½šŹōµÄ»īĘĆŠŌÅŠ¶Ļµē¼«·“Ó¦£»
B”¢Ńō¼«Ź§µē×ÓµÄÓŠFe”¢Zn”¢Cu£»Ņõ¼«Īö³öµÄŹĒĶ£»ŅĄ¾Żµē×ÓŹŲŗć¼ĘĖć·ÖĪö£»
C”¢¾«Į¶¹ż³ĢÖŠ£¬µē½āÖŹČÜŅŗÖŠŅ»¶Øŗ¬ÓŠNi2+£»
D”¢“ÖÄųÖŠŗ¬ÓŠÉŁĮæFe”¢Zn”¢Cu”¢PtµČŌÓÖŹ×öŃō¼«£¬ĶŗĶćK²»Ź§µē×Ó³Į½µµē½ā³Ųµ×²æŠĪ³ÉŃō¼«Äą£®
½ā“š ½ā£ŗA”¢Ńō¼«·¢ÉśŃõ»Æ·“Ó¦£¬Ęäµē¼«·“Ó¦Ź½£ŗNi-2e-=Ni2+£¬Fe-2e-=Fe2+£»Zn-2e-=Zn2+£¬¹ŹA“ķĪó£»
B”¢µē½ā¹ż³ĢÖŠŃō¼«Ź§µē×ÓµÄÓŠFe”¢Zn”¢Cu£»Ņõ¼«Īö³öµÄŹĒĶ£»ŅĄ¾Żµē×ÓŹŲŗć£¬Ńō¼«ÖŹĮæµÄ¼õÉŁÓėŅõ¼«ÖŹĮæµÄŌö¼Ó²»ĻąµČ£¬¹ŹBÕżČ·£»
C”¢µē½āŗó£¬ČÜŅŗÖŠ“ęŌŚµÄŃōĄė×ÓÓŠH+”¢Fe2+”¢Zn2+”¢Ni2+£¬¹ŹC“ķĪó£»
D”¢“ÖÄųÖŠŗ¬ÓŠÉŁĮæFe”¢Zn”¢Cu”¢PtµČŌÓÖŹ×öŃō¼«£¬ĶŗĶćK²»Ź§µē×Ó³Į½µµē½ā³Ųµ×²æŠĪ³ÉŃō¼«Äą£¬µē½āŗ󣬵ē½ā²Ūµ×²æµÄŃō¼«ÄąÖŠÖ»ÓŠCuŗĶPt£¬¹ŹD“ķĪó£»
¹ŹŃ”B£®
µćĘĄ ±¾Ģāæ¼²éĮĖµē¼«ŌĄķµÄÓ¦ÓĆ£¬Ö÷ŅŖæ¼²éµē½ā¾«Į¶ÄųµÄŌĄķ·ÖĪöÅŠ¶Ļ£¬ĢāÄæÄѶČÖŠµČ£®


 Źī¼ŁĻĪ½ÓÅąÓŽĢ²ÄÕć½¹¤ÉĢ“óѧ³ö°ęÉēĻµĮŠ“š°ø
Źī¼ŁĻĪ½ÓÅąÓŽĢ²ÄÕć½¹¤ÉĢ“óѧ³ö°ęÉēĻµĮŠ“š°ø ŠĄÓļĪÄ»ÆæģĄÖŹī¼ŁÉņŃō³ö°ęÉēĻµĮŠ“š°ø
ŠĄÓļĪÄ»ÆæģĄÖŹī¼ŁÉņŃō³ö°ęÉēĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | 2H2£Øg£©+O2£Øg£©=2H2O£Øg£©”÷H1 2H2£Øg£©+O2£Øg£©=2H2O£Øl£©”÷H2 | |
| B£® | S£Øg£©+O2£Øg£©=SO2£Øg£©”÷H1 S£Øs£©+O2£Øg£©=SO2£Øg£©”÷H2 | |
| C£® | C£Øs£©+$\frac{1}{2}$O2£Øg£©=CO£Øg£©”÷H1 C£Øs£©+O2£Øg£©=CO2 £Øg£©”÷H2 | |
| D£® | H2£Øg£©+Cl2£Øg£©=2HCl£Øg£©”÷H1 $\frac{1}{2}$H2£Øg£©+$\frac{1}{2}$Cl2£Øg£©=HCl£Øg£©”÷H2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | SŌ×Ó½į¹¹Ź¾ŅāĶ¼£ŗ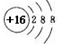 | |
| B£® | ¶žŃõ»ÆĢ¼µÄµē×ÓŹ½£ŗ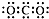 | |
| C£® | H”¢D”¢T±ķŹ¾Ķ¬Ņ»ÖÖŗĖĖŲ | |
| D£® | Ō×ÓŗĖÄŚÓŠ10øöÖŠ×ÓµÄŃõŌ×Ó£ŗ${\;}_{8}^{18}O$ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | NH4Cl | B£® | NaF | C£® | KOH | D£® | H2SO4 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 0.64g | B£® | 1.28g | C£® | 2.56g | D£® | 5.12g |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŠæŹĒÕż¼«£¬Ńõ»ÆŅųŹĒøŗ¼« | |
| B£® | Šæ·¢Éś»¹Ō·“Ó¦£¬Ńõ»ÆŅų·¢ÉśŃõ»Æ·“Ó¦ | |
| C£® | ČÜŅŗÖŠOH-ĻņÕż¼«ŅĘ¶Æ£¬K+”¢H+Ļņøŗ¼«ŅĘ¶Æ | |
| D£® | ŌŚµē³Ų·ÅµēµÄ¹ż³ĢÖŠ£¬µē½āÖŹČÜŅŗµÄ¼īŠŌ±ä“ó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
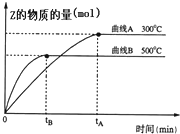 Ļņa LĆܱÕČŻĘ÷ÖŠ¼ÓČė1mol XĘųĢåŗĶ2mol YĘųĢ壬·¢ÉśČēĻĀ·“Ó¦£ŗX£Øg£©+2Y£Øg£©?2Z£Øg£©£¬²»Ķ¬ĪĀ¶ČĻĀ£¬²āµĆĘ½ŗāדĢ¬ZµÄĪļÖŹµÄĮæ±ä»ÆĒśĻßČēĶ¼ĖłŹ¾£®
Ļņa LĆܱÕČŻĘ÷ÖŠ¼ÓČė1mol XĘųĢåŗĶ2mol YĘųĢ壬·¢ÉśČēĻĀ·“Ó¦£ŗX£Øg£©+2Y£Øg£©?2Z£Øg£©£¬²»Ķ¬ĪĀ¶ČĻĀ£¬²āµĆĘ½ŗāדĢ¬ZµÄĪļÖŹµÄĮæ±ä»ÆĒśĻßČēĶ¼ĖłŹ¾£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

| ĪĀ¶Č£Ø”ę£© | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| ĶµÄĘ½¾łČܽāĖŁĀŹ £Ø”Į10-3mol•L-1•min-1£© | 7.34 | 8.01 | 9.25 | 7.98 | 7.24 | 6.73 | 5.76 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com