
【题目】某固体化合物A,按图所示发生系列变化,已知E溶液中加入氨水后产生的白色沉淀很快变为灰绿色,最后变为红褐色。
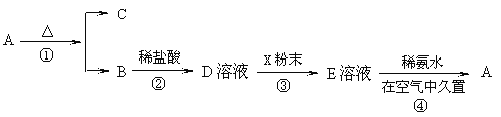
回答下列问题:(1)物质A是___(填化学式)。
(2)反应②的离子反应方程式为___。
(3)反应④的化学反应方程式为___。
【答案】Fe(OH)3 Fe2O3+6H+=2Fe3++3H2O 4Fe(OH)2+O2+2H2O=4Fe(OH)3
【解析】
已知E溶液中加入氨水后产生的白色沉淀很快变为灰绿色,最后变为红褐色说明A为氢氧化铁,Fe(OH)3,A加热分解生成B为Fe2O3,C为H2O,依据流程分析判断D为FeCl3,X为Fe,E为FeCl2 溶液,据此分析。
已知E溶液中加入氨水后产生的白色沉淀很快变为灰绿色,最后变为红褐色说明A为氢氧化铁,Fe(OH)3,A加热分解生成B为Fe2O3,C为H2O,依据流程分析判断D为FeCl3,X为Fe,E为FeCl2 溶液。
(1)依据推断可知A为Fe(OH)3;
(2)反应②是盐酸和氧化铁发生的复分解反应,反应的离子反应方程式为Fe2O3+6H+=2Fe3++3H2O;
(3)反应④是氢氧化亚铁和氧气水 发生反应生成氢氧化铁的也还原反应,反应的化学反应方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3。


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:
【题目】A、B、C、D均为短周期元素。A、B可形成两种液态化合物甲和乙,其最简式分别为BA和B2A。A与D可形成气态化合物DA、DA2。A、B、D可组成离子化合物,该晶体化学式为B4A3D2,其水溶液呈弱酸性。B与D可形成一种极易溶于水的碱性气体X。B与C可形成极易溶于水的酸性气体Y。已知X分子与乙分子中的电子数相等,Y分子与甲分子中的电子数相等。请回答:
(1)A元素为___,甲的电子式为____________。
(2)常温下,pH为a的Y溶液与pH为b的氢氧化钠溶液按体积比1∶10混合后,正好完全反应,则a与b的关系为______。
(3)已知X在液态时和水一样,可发生微弱的电离,产生两种含相同电子数的粒子,请写出它电离方程式:____________________。
(4)将X和Y的稀溶液按某种比例混合,
①若所得溶液中只含一种溶质,则该溶质是______,溶液中离子浓度的大小顺序为____________________________;
②若该溶液是由体积相等的X和Y溶液混合而成,且恰好呈中性,则混合前c(X)____c(Y),混合前酸中c(H+)和碱中c(OH-)的关系c(H+)____c(OH-)(填“大于”、“等于”、“小于”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高锰酸钾是中学化学常用的试剂。主要用于防腐、化工、制药等。实验室模拟工业上用软锰矿制备高锰酸钾的流程如下:
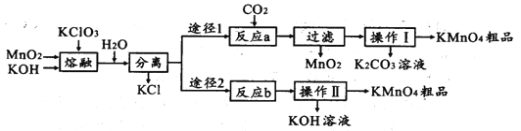
(1)实验室熔融二氧化锰、氧氧化钾、氯酸钾时应选择哪一种仪器________________
a.普通玻璃坩埚 b.石英坩埚 c.陶瓷坩埚 d.铁坩埚
(2)第一步熔融时生成K2MnO4的化学方程式:_________
(3)操作Ⅰ中根据KMnO4和K2CO3两物质在____________ (填性质)上的差异,采用浓缩结晶、趁热过滤得到KMnO4。趁热过滤的原因是_______________
(4)反应b是电解法制备KMnO4,其装置如图所示,a作____________极(填“阳”或“阴”),中间的离子交换膜是_____ (填“阳”或“阴”)离子交换膜。阳极的电极反应式为____________
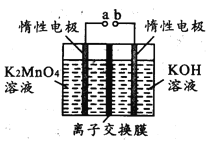
(5)KMnO4稀溶液是一种常用的消毒剂。其消毒原理与下列物质相同的________(填标号)。
a.双氧水 b.84消液(NaClO溶液) c.75%酒精
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室常见的几种气体发生装置如图1中A、B、C所示:
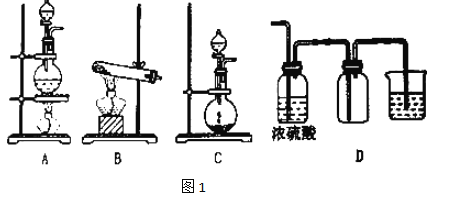
(1)实验室可以用B或C装置制取O2,如果用C装置,通常使用的药品是___;检查C装置气密性的操作方法是__。
(2)若用A装置与D装置相连制取收集X气体,则X可能是下列气体中的(填序号,下同)___;
①CO2 ②Cl2 ③H2
实验室中制取该气体的离子方程式为:__;其中在D装置中连接小烧杯的目的是__。
(3)气体的性质是选择气体收集方法的主要依据。下列气体的性质与收集方法无关的是__。
①密度 ②颜色 ③溶解性 ④热稳定性 ⑤是否与氧气反应
图2是某学生设计的收集气体的几种装置,其中不可行的是__。
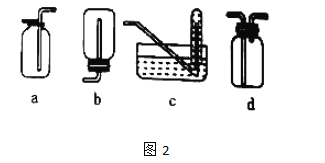
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2014年3月22日是第二十二届“世界水日”,保护水资,从我做起!
(1)ClO2和Cl2(还原产物都为Cl-)是生活中常用的消毒剂。当消耗等物质的量的两种物质时,ClO2的消毒效率是Cl2的_______倍。
(2)炼金废水中含有络离子[Au(CN)2]+,与弱电解质碳酸的电离方式相似,[Au(CN)2]+也存在着两步电离,其电离出CN-有毒,CN-与H+结合生成毒性更强的HCN。[Au(CN)2]+的一级电离方程式:__________________________;在碱性条件下NaClO将废水中的CN-氧化成CO![]() 和N2,其反应的离子方程式为: _______________________________________________ 。
和N2,其反应的离子方程式为: _______________________________________________ 。
(3)某无色废水中可能含有Fe3+、Al3+、Mg2+、Na+、NO3-、CO32-、SO42-离子中的几种,为分析其成分,分别取废水样品100mL,进行了三组实验,其操作和有关现象如下图所示:
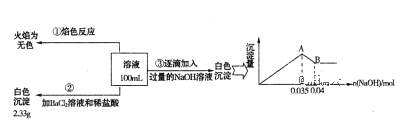
请根据上图回答下列问题:
①实验中需配制1.0mol/L的NaOH溶液100mL,所需仪器除了玻璃棒、托盘天平、量筒、药匙、烧杯、胶头滴管,还缺少的仪器为________________。
②实验③中沉淀量由A→B过程中所发生反应的离子方程式为_______________________________。
③试确定NO3-是否存在?_________________(填“存在”、“不存在”或“不确定”),若存在,试计算c(NO3-)_________________(若不存在,此问不必作答)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为氯及其化合物的“价-类”二维图。
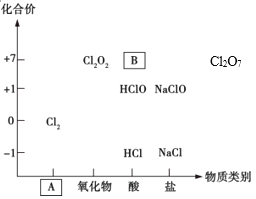
(1)填写二维图缺失的类别A_________和化学式B_________。
(2)某同学利用以下试剂研究HCl性质,进行了如下预测:
a.NaClO b.Fe c.NaOH d.KMnO4 e.AgNO3
从物质类别上看,HCl属于______,可能与__________发生反应(填序号);
从化合价角度看,Cl-具有______性,可能与_____发生反应(填序号)。
(3)某工厂用NaCl溶液制备氯气,其化学原理为如下反应:
![]() H2O +
H2O + ![]() NaCl == Cl2 +
NaCl == Cl2 + ![]() NaOH+
NaOH+![]()
①请将上述方程式补充完整,并用单线桥表示电子转移。_____________
②反应中NaCl作_________剂,理由是_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常用调味剂花椒油是一种从花椒籽中提取的水蒸气挥发性香精油,溶于乙醇、乙醚等有机溶剂。利用如图所示装置处理花椒籽粉,经分离提纯得到花椒油。
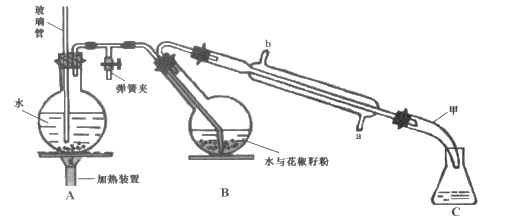
实验步骤:
(一)在A装置中的圆底烧瓶中装入![]() 容积的水,加1~2粒沸石。同时,在B中的圆底烧瓶中加入20g花椒籽粉和50mL水。
容积的水,加1~2粒沸石。同时,在B中的圆底烧瓶中加入20g花椒籽粉和50mL水。
(二)加热A装置中的圆底烧瓶,当有大量蒸气产生时关闭弹簧夹,进行蒸馏。
(三)向馏出液中加入食盐至饱和,再用15mL乙醚萃取2次,将两次萃取的醚层合并,加入少量无水Na2SO4;将液体倾倒入蒸馏烧瓶中,蒸馏得花椒油。
(1)装置A中玻璃管的作用是_______。装置B中圆底烧瓶倾斜的目的是 ________。
(2)步骤(二)中,当观察到_______现象时,可停止蒸馏。蒸馏结束时,下列操作的顺序为_______(填标号)。
①停止加热②打开弹簧夹③关闭冷凝水
(3)在馏出液中加入食盐的作用是__ ;加入无水Na2SO4的作用是_______。
(4)实验结束后,用稀NaOH溶液清洗冷凝管,反应的化学方程式为_________。(残留物以![]() 表示)
表示)
(5)为测定花椒油中油脂的含量,取20.00mL花椒油溶于乙醇中,加80.00mL0.5mol/LNaOH的乙醇溶液,搅拌,充分反应,加水配成200mL溶液。取25.00mL加入酚酞,用0.1moI/L盐酸进行滴定,滴定终点消耗盐酸20.00mL。则该花椒油中含有油脂_______ g/L。
(以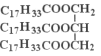 计,式量:884)。
计,式量:884)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸亚铁(FeC2O4)可作为生产电池正极材料磷酸铁锂的原料,受热容易分解,为探究草酸亚铁的热分解产物,按下面所示装置进行实验。
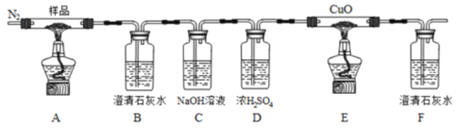
下列说法不正确的是
A.实验中观察到装置B、F中石灰水变浑浊,E中固体变为红色,则证明分解产物中有CO2和CO
B.反应结束后,取A中固体溶于稀硫酸,向其中滴加1~2滴KSCN溶液,溶液无颜色变化,证明分解产物中不含Fe2O3
C.装置C的作用是除去混合气中的CO2
D.反应结束后,应熄灭A,E处酒精灯后,持续通入N2直至温度恢复至室温
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积可变的密闭容器中发生可逆反应:2NO2(g)![]() 2NO(g)+O2(g)。能作为反应达到平衡状态的标志是
2NO(g)+O2(g)。能作为反应达到平衡状态的标志是
A.单位时间内生成n mol O2的同时生成n mol NO2
B.NO2、NO、O2三者的物质的量浓度之比为2:2:1
C.混合气体的密度不再改变
D.容器中气体压强不再变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com