
| A. | 反应Z2+2A2+═2A3++2Z-能够进行 | |
| B. | Z元素在①③反应中均被氧化 | |
| C. | 反应①的离子方程式为:16H++10Z-+2XO4-═2X2++5Z2+8H2O | |
| D. | 氧化性由强到弱的顺序是XO4-、Z2、B2、A3+ |
分析 氧化还原反应中氧化剂的氧化性大于氧化产物的氧化性,则16H++10Z-+2XO4-═2X2++5Z2↑+8H2O中氧化性为XO4->Z2,2A2++B2═2A3++2B-中氧化性为B2>A3+,2B-+Z2═B2+2Z-中氧化性为Z2>B2,以此来解答.
解答 解:A.由上述分析可知,氧化性Z2>A3+,则反应Z2+2A 2+═2A3++2Z-能发生,故A正确;
B.Z元素在(1)中化合价升高,被氧化,而在(3)中元素的化合价降低,被还原,故B错误;
C.由电子、电荷守恒,可知①的;离子方程式为16H++10Z-+2XO4-═2X2++5Z2+8H2O,故C正确;
D.由上述分析可知,氧化性由强到弱的顺序是XO4-、Z2、B2、A3+,故D正确;
故选B.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化及氧化性的比较方法为解答的关键,侧重分析与应用能力的考查,注意氧化性、还原性的比较方法及守恒法应用,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 原子的核外电子层数等于该元素所在的周期数 | |
| B. | 元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素 | |
| C. | 同一元素的各种同位素的物理性质、化学性质均相同 | |
| D. | 除氦外的稀有气体原子的最外层电子数都是8 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 已知A-F是中学化学中常见的物质,其中A、C、E、F为气体,B、D为液体,D是中学常见的强酸,D的浓溶液与铜共热可生成A:F的浓度液与X共热通常用于中学实验室制备单质C:B和X混合是实验室常温下简易制单质E的一种方法,X是一种黑色粉末,B的分子中有18个电子.反应中部分生成物略去,试回答下列问题:
已知A-F是中学化学中常见的物质,其中A、C、E、F为气体,B、D为液体,D是中学常见的强酸,D的浓溶液与铜共热可生成A:F的浓度液与X共热通常用于中学实验室制备单质C:B和X混合是实验室常温下简易制单质E的一种方法,X是一种黑色粉末,B的分子中有18个电子.反应中部分生成物略去,试回答下列问题: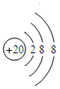 ,
,查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑥ | B. | ②④⑤ | C. | ②③④ | D. | ②④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| n(SO32-):n(HSO3-) | 91:9 | 1:1 | 1:91 |
| pH | 8.2 | 7.2 | 6.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
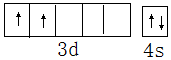
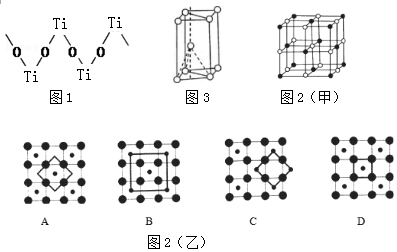
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com