




| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| A”¢Ņ׊Ī³ÉŅ»¼ŪĄė×Ó |
| B”¢“ÓÉĻµ½ĻĀµ„ÖŹµÄŃõ»ÆŠŌÖš½„¼õČõ |
| C”¢“ÓÉĻµ½ĻĀĒā»ÆĪļµÄ·ŠµćÖš½„Éżøß |
| D”¢“ÓÉĻµ½ĻĀĒā»ÆĪļµÄĪȶØÖš½„¼õČõ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ

| ŹµŃ鱹ŗÅ | ·“Ó¦Īļ | “߻ƼĮ |
| ¢Ł | 10mL 2% H2O2ČÜŅŗ | ĪŽ |
| ¢Ś | 10mL 5% H2O2ČÜŅŗ | ĪŽ |
| ¢Ū | 10mL 5% H2O2ČÜŅŗ | 0.1gMnO2·ŪÄ© |
| ¢Ü | 10mL 5% H2O2ČÜŅŗ+ÉŁĮæHClČÜŅŗ | 0.1gMnO2·ŪÄ© |
| ¢Ż | 10mL 5% H2O2ČÜŅŗ+ÉŁĮæNaOHČÜŅŗ | 0.1gMnO2·ŪÄ© |

| µŚŅ»“Ī | µŚ¶ž“Ī | µŚČż“Ī | µŚĖÄ“Ī | |
| Ģå»ż£ØmL£© | 17.10 | 18.10 | 18.00 | 17.90 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
 £ØI£©ČēĶ¼ŹĒÄ³Ń§Š£ĮÖĄĻŹ¦ÖʱøNH3²¢½ųŠŠŠŌÖŹŹµŃ鏱µÄøĽų×°ÖĆ£®°“Ķ¼1°ŃŅĒĘ÷°²×°ŗĆ£¬³ĘČ”2g¹ĢĢåĀČ»Æļ§×°ČėŹŌ¹Üµ×²æ£¬ŌŁ³ĘČ”2gĒāŃõ»ÆÄĘø²øĒŌŚĀČ»Æļ§ÉĻ·½£»Į¢¼“ÓĆ“ųÓŠµĪ¹ÜµÄČū×ÓČū½ō£ØµĪ¹ÜŌ¤ĻČĪüČėŌ¼2mLÅØ°±Ė®£©£»ÉÕ±ÄŚŹ¢µĪÓŠ·ÓĢŖŹŌŅŗµÄĖ®£ŗ°ŃÅØ°±Ė®µĪČėŹŌ¹ÜĄļ£¬æÉĮ¢¼“¹Ū²ģµ½ŹŌ¹ÜÄŚ·¢Éś¾ēĮŅ·“Ó¦£¬ÓŠ“óĮæĘųÅŻ£®
£ØI£©ČēĶ¼ŹĒÄ³Ń§Š£ĮÖĄĻŹ¦ÖʱøNH3²¢½ųŠŠŠŌÖŹŹµŃ鏱µÄøĽų×°ÖĆ£®°“Ķ¼1°ŃŅĒĘ÷°²×°ŗĆ£¬³ĘČ”2g¹ĢĢåĀČ»Æļ§×°ČėŹŌ¹Üµ×²æ£¬ŌŁ³ĘČ”2gĒāŃõ»ÆÄĘø²øĒŌŚĀČ»Æļ§ÉĻ·½£»Į¢¼“ÓĆ“ųÓŠµĪ¹ÜµÄČū×ÓČū½ō£ØµĪ¹ÜŌ¤ĻČĪüČėŌ¼2mLÅØ°±Ė®£©£»ÉÕ±ÄŚŹ¢µĪÓŠ·ÓĢŖŹŌŅŗµÄĖ®£ŗ°ŃÅØ°±Ė®µĪČėŹŌ¹ÜĄļ£¬æÉĮ¢¼“¹Ū²ģµ½ŹŌ¹ÜÄŚ·¢Éś¾ēĮŅ·“Ó¦£¬ÓŠ“óĮæĘųÅŻ£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| V2O |
| ”÷ |

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
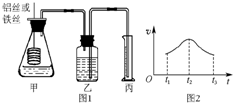 Ä³ŃŠ¾æŠ”×éÄāÓƶØĮæµÄ·½·Ø²āĮæAlŗĶFe·Ö±šÓėĖį·“Ó¦µÄæģĀż£¬Éč¼ĘĮĖČēĻĀĶ¼1ĖłŹ¾µÄ×°ÖĆ£®
Ä³ŃŠ¾æŠ”×éÄāÓƶØĮæµÄ·½·Ø²āĮæAlŗĶFe·Ö±šÓėĖį·“Ó¦µÄæģĀż£¬Éč¼ĘĮĖČēĻĀĶ¼1ĖłŹ¾µÄ×°ÖĆ£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| A”¢Ź³“×ÓĆĒāŃõ»ÆÄĘČÜŅŗµĪ¶Ø£¬æŖŹ¼Ź±ČÜŅŗµÄpHĶس£±ä»Æ»ŗĀż£¬µ±½Ó½üµĪ¶ØÖÕµćŹ±£¬pH ³öĻÖĶ»±ä£¬³ĘĪŖµĪ¶ØĶ»Ō¾ |
| B”¢½į¾§Ź±£¬Čō³ĮµķµÄ½į¾§æÅĮ£½Ļ“󣬾²ÖĆŗóČŻŅ׳Į½µµ½ČŻĘ÷µ×²æ£¬“ĖŹ±£¬½ųŠŠ·ÖĄėµÄ²Ł×÷·½·ØŹĒĒćĪö |
| C”¢³éĀĖ×°ÖĆÓɲ¼ŹĻĀ©¶·”¢ĪüĀĖĘ攢°²Č«Ę攢³éĘų±ĆµČŅĒĘ÷×é³É£¬¹¤×÷µÄÖ÷ŅŖŌĄķŹĒ³éĘų±ĆøųĪüĀĖĘæ¼õŃ¹£¬µ¼ÖĀ×°ÖĆÄŚ²æµÄŃ¹Ēæ½µµĶ£¬Ź¹¹żĀĖµÄĖŁ¶Č¼Óæģ |
| D”¢ŌŚÖ½²ćĪö·Ø·ÖĄėFe3+ŗĶCu2+µÄŹµŃéÖŠ£¬²ćĪöŗ󣬾°±Ń¬£¬ĀĖÖ½ÖŠĪŽÉ«“ų³öĻÖ£¬Ņ»¶ØŹĒĪó½«ŹŌŃłµć½žĆ»ŌŚÕ¹æŖ¼ĮÖŠ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| »ÆѧŹ½ | AgCl | Ag2CrO4 | CH3COOH | HClO | H2ClO3 |
| Ksp»ņKa | Ksp=1.8”Į10-10 | Ksp=2.0”Į10-12 | Ka=1.8”Į105 | Ka=3.0”Į10-8 | Ka1=4.1”Į10-7 Ka2=1.8”Į10-11 |
| A”¢ĻąĶ¬ÅضČCH3COONaŗĶNaClOµÄ»ģŗĻŅŗÖŠ£¬ø÷Ąė×ÓÅØ¶ČµÄ“óŠ”¹ŲĻµŹĒc£ØNa+£©£¾c£ØClO-£©£¾c£ØCH3COO-£©£¾c£ØOH-£©£¾c£ØH+£© |
| B”¢Ģ¼ĖįÄĘČÜŅŗÖŠµĪ¼ÓÉŁĮæĀČĖ®µÄĄė×Ó·½³ĢŹ½ĪŖCO2-3+Cl2+H2O=HCO-3+Cl-+HClO |
| C”¢Ļņ0.1mol?L-1CH3COOHČÜŅŗÖŠµĪ¼ÓNaOHČÜŅŗÖĮc£ØCH3COOH£©£ŗc£ØCH3COO-£©=5£ŗ9£¬“ĖŹ±ČÜŅŗpH=5 |
| D”¢ĻņÅØ¶Č¾łĪŖ1”Į10-3mol?L-1µÄKClŗĶK2CrO4»ģŗĻŅŗÖŠµĪ¼Ó1”Į10-3mol?L-1µÄAgNO3ČÜŅŗ£¬CrO2-4ĻČŠĪ³É³Įµķ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com