
 cC(g)+dD(g),达到平衡时测得B气体的浓度为0.6 mol/L,恒温下将密闭容器的容积扩大1倍,重新达到平衡时,测得B气体的浓度为0.4 mol/L,下列叙述中正确的是
cC(g)+dD(g),达到平衡时测得B气体的浓度为0.6 mol/L,恒温下将密闭容器的容积扩大1倍,重新达到平衡时,测得B气体的浓度为0.4 mol/L,下列叙述中正确的是科目:高中化学 来源: 题型:
| b |
| 2 |
| 3c |
| 2 |
| b |
| 2 |
| 3c |
| 2 |
| 1 |
| 32 |
| 1 |
| 32 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 1 |
| 2 |
| c(N2)c2(CO2) |
| c2(NO)c2(CO) |
| c(N2)c2(CO2) |
| c2(NO)c2(CO) |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
高铁酸钾(K2FeO4)具有极强的氧化性,因该物质具有“绿色”、选择性高、活性强等特点受到人们关注。
(1)高锰酸钾制备方法之一为:
①在一定温度下,将氯气通入KOH溶液中制得含有次氯酸钾的溶液;
②在剧烈搅拌条件下,将Fe(NO3)3分批加入次氯酸钾溶液中,控制反应温度,以免次氯酸钾分解;
③甲KOH至饱和,使K2FeO4充分析出,再经纯化得产品,其纯度在95%以上。
①氯碱工业中制备氯气的化学方程式是 ;
②温度过高会导致次氯酸钾自身分解生成两种化合物,产物之一是氯酸钾(KclO3),另一种产物应该是 (写化学式)。
③制备过程有一步反应如下,请配平方程式(将计量数填入方框中):
![]()
(2)为探究高铁酸钾的某种性质,进行如下两种实验:
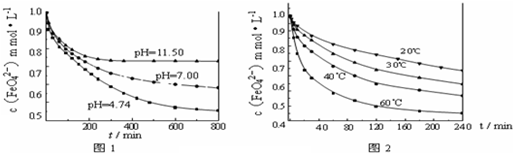
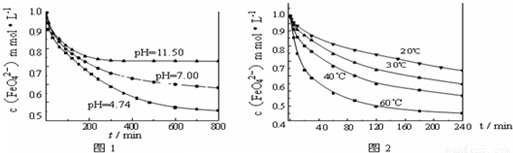
实验一:将适量K2FeO4分别溶解于pH为4.74、7.00、11.50的水溶液中,配的FeO42―浓度为1.0m mol?L―1(1 m molL―1=1×103 mol?L―1)的试样,分别静置800min,考查初始pH不同的水溶液对K2FeO4某种性质的影响,结果见图1。
实验二:将适量K2FeO4溶解于pH=4.74的水溶液中,配制成FeO42―浓度为1.0m mol?L―1的试样,将试样分别置于20℃、30℃、40℃和60℃的恒温水浴中,考查不同温度对K2FeO4某种性质的影响,结果见图2。
①实验1的目的是 ;
②实验2可得出的结论是 ;
③高铁酸钾在水中的反应为:FeO42―+10H2O![]() 4Fe(OH)3+8OH―+3O2↑
4Fe(OH)3+8OH―+3O2↑
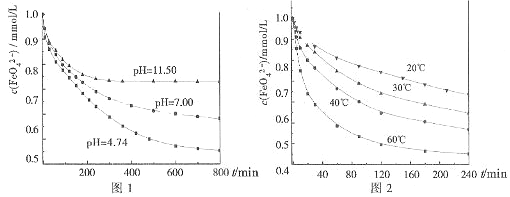
由图1可知,800min时,初始pH=11.50的溶液中,高铁酸钾的最终浓度比pH=4.74的溶液中高,主要原因是 。
查看答案和解析>>
科目:高中化学 来源:2009-2010学年浙江省金华市十校联考高三(上)期末化学模拟试卷(解析版) 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com