
| A. | 煤燃烧时产生大量CO2 | B. | 煤不完全燃烧产生大量CO | ||
| C. | 煤燃烧时产生大量SO2 | D. | 工业生产中排放大量烟尘 |
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:选择题
| A. | 铝的化学性质稳定 | |
| B. | 铝在常温时与氧气不反应 | |
| C. | 铝具有金属性,也具有非金属性 | |
| D. | 铝与氧气反应生成一层致密的氧化物薄膜 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol硫单质在过量氧气中燃烧产生NA个SO3分子 | |
| B. | 标准状况下,22.4LSO3中含有氧原子数为3NA | |
| C. | 标准状况下,18gH2O中含有氧原子数为NA | |
| D. | 5.4g铝单质与足量NaOH溶液反应,转移电子数为0.6NA |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

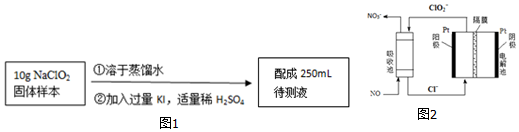
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Y的原子序数比X的大 | B. | Y的离子半径比X的离子大 | ||
| C. | Y原子的最外层电子数比X的大 | D. | Y元素的最高正价比X的大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
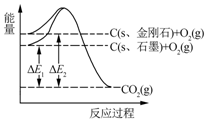
| A. | 1 mol石墨完全转化为金刚石需吸收1.9 kJ热量 | |
| B. | 石墨和金刚石的转化是物理变化 | |
| C. | 金刚石的稳定性强于石墨 | |
| D. | 1 mol金刚石和1 mol O2化学键断裂吸收的能量总和大于1 mol CO2分子中化学键断裂吸收的能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下90g乙二酸所占的体积约为22.4L | |
| B. | lmol乙二酸中含有共用电子对的数目为9NA | |
| C. | 90g乙二酸被NaC1O氧化生成CO2,转移的电子数为NA | |
| D. | 0.lmol•L-1的乙二酸溶液中,H2C2O4、C2O2-和HC2O4-的微粒数之和为0.1NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com