
酸、碱、盐都是电解质,在水中都能电离出离子。
(1)下列溶液中,c(H+)由大到小的排列顺序是 ;pH由大到小的排列顺序是 。
A.0.1 mol/L CH3COOH溶液 B.0.1 mol/L HCl C.0.1 mol/L H2SO4
(2)体积相同、物质的量浓度相同的醋酸溶液与氢氧化钠溶液混合后,溶液呈 (填“酸性”、“碱性”或“中性”);溶液中c(Na+) (填“>”“=”“<”)c(CH3COO―)。
(3)体积相同、pH相同的盐酸和醋酸溶液与氢氧化钠溶液完全中和时,两者消耗的氢氧化钠的物质的量一定 (填“相等”或“不相等”),其原因是
 _____________________________________。
_____________________________________。
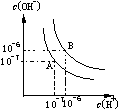
(4)水的电离平衡如右图所示,若A点表示25℃时水的电离平衡状态,当升高温度至100℃时水的电离平衡状态为B点,则此时水的离子积为 。
 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:
 酸、碱、盐都是电解质,在水中都能电离出离子.根据下列化合物:
酸、碱、盐都是电解质,在水中都能电离出离子.根据下列化合物:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com