
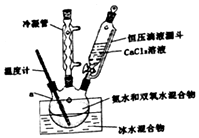
 �������ƣ�CaO2����һ�ְ�ɫ�ᾧ���ĩ��������ˮ�������ڴ��ࡢ���ѵȣ�������150�����ҿ�ʼ�ֽ�ų���������ˮ������Ӧ����H2O2�������ᷴӦ����H2O2
�������ƣ�CaO2����һ�ְ�ɫ�ᾧ���ĩ��������ˮ�������ڴ��ࡢ���ѵȣ�������150�����ҿ�ʼ�ֽ�ų���������ˮ������Ӧ����H2O2�������ᷴӦ����H2O2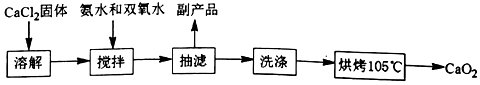
| ���� ʱ�� | ��Ʒȡ������/��g�� | ƽ�����������KMnO4��/mL |
| ����ǰ�ⶨ | a | 25.00 |
| ����һ���º�ⶨ | a | 24.00 |
���� ��1������װ�õĹ����֪��
��2���ٴ�˫��ˮ���ȶ��ԡ��÷�Ӧ�ķ�Ӧ�ȡ��¶ȶԹ������Ƶ��ܽ�ȵ�Ӱ��ȷ���������ڹ������Ƽ�����ˮ����Ӧ����������ʲ������Ҵ������ѣ�������ˮ�й��������ܽ��С���ݴ˽��н��
��3�����ݷ�Ӧ��Ҫ���裬�¶�ˮԡ���Ʒ�����
��4�������������ɫ�����Ը��������Һ�ζ�����H2O2���ζ��յ�Ϊ����ɫ�䵭��ɫ���Ұ���Ӳ���ɫ��
��5�����ݷ�Ӧ6H++2MnO4-+5H2O2=2Mn2++5O2+8H2O�������ǰ��CaO2�������������ݴ˼��㣮
��� �⣺��1������װ�õĹ����֪aΪ������ƿ��
�ʴ�Ϊ��������ƿ��
��2���������¶Ƚϸ�ʱ˫��ˮ���ֽ⣬�ᵼ�¹������Ʋ����½������¶Ƚ���ʱ�������Ƶ��ܽ�ȼ�С�������ڹ������Ƶ����������Գ�����Ӧʱ���ñ�ˮԡ�����¶���0�����ң�
�ʴ�Ϊ������H2O2���ȷֽ⣻���Ͱ��Ļӷ��������¶ȴ�ʹ����������
��A����ˮ��������������ˮ���ܽ�Ƚϴ����˹������ƵIJ��ʣ���A����
B����ˮ���������Ƽ�����ˮ�������ʶ�������ˮ��������ˮϴ�ӹ������ƣ���B��ȷ��
C���Ҵ����������Ʋ������Ҵ����������ʲ������Ҵ���������˳ɱ�����C����
D�����ѣ��������Ʋ��������ѣ�������Ҳ���������ѣ������ѳɱ��ϸߣ���D����
�ʴ�Ϊ��B��
��3��Ϊʹ��Ӧ�������裬ˮԡˮԡ����Ҫ�¶ȼƣ������¶ȼ�Ӧ��Ϊ��������
�ʴ�Ϊ���¶ȼ�Ӧ��Ϊ���������÷�Ӧ��Ҫ���Ͻ��裬�ұ�ˮԡ���������¶ȼƣ�
��4�����ݸ����������ɫ�����Ը��������Һ�ζ�����H2O2���ζ��յ�Ϊ����ɫ�䵭��ɫ���Ұ���Ӳ���ɫ��
�ʴ�Ϊ����Һ����ɫ�䵭��ɫ���Ұ���Ӳ���ɫ��
��5�����������غ�CaO2���ᷴӦ���ɵ���ͬ��������H2O2�������Ը�����ط�����Ӧ6H++2MnO4-+5H2O2=2Mn2++5O2+8H2O������ݣ�5CaO2��5H2O2��2MnO4-�������һ����ǰ�Ĺ������Ƶ���������Ϊ��0.025��0.1��2.5��72��a��100%������һ���º�Ĺ������Ƶ���������Ϊ��0.024��0.1��2.5��72��a��100%����ò�Ʒ���ȶ���Ϊ��$\frac{0.024��0.1��2.5��72��a��100%}{0.025��0.1��2.5��72��a��100%}��100%$=96%��
�ʴ�Ϊ��96%��
���� ���⿼����ʽΪ�����Ʊ�����ͼ��Ŀ���漰�к͵ζ��е������������ʵļ��鼰��ѧ��������⣬��Ŀ�ѶȽϴ�����ʱע��������йؼ���Ϣ����ȷʵ��������������������Ϊ�ۺϣ���ֿ�����ѧ���ķ�����������������ѧʵ�顢��ѧ����������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ĵ�������� | B�� | H+��Ŀ���� | ||
| C�� | c��H+������ | D�� | �����Լ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ѹ�ƵƳ����ڵ�·������ | B�� | ����ʯ��ˮ������Ư�� | ||
| C�� | �辧�������뵼����� | D�� | ����þ�����������źŵ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��pH��ֽ���0.010mol/L��ˮ��pHΪ10 | |
| B�� | ��pH��ֽ�ⶨ0.10mol/LNH4Cl��ҺΪpH��7 | |
| C�� | ȡ��10mL0.010mol/L��ˮ������2�η�̪��Һ���Էۺ�ɫ���ټ���NH4C1������������ɫ��dz | |
| D�� | ȡ��10mL0.010mol/L��ˮ������2�η�̪��Һ���Էۺ�ɫ����ϡ������������ɫ��dz |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na+��K+��OH-��Cl- | B�� | Na+��Cu2+��SO42-��NO3- | ||
| C�� | Mg2+��Na+��SO42-��Cl- | D�� | Ca2+��HCO3-��NO3-��K+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ����ͬһ�����ʵ��ǣ�������
����ͬһ�����ʵ��ǣ�������| A�� | 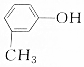 | B�� | 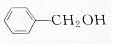 | C�� | 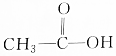 | D�� | 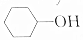 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1 mol NH3�����еĵ�����Ϊ9NA | |
| B�� | ���³�ѹ�£�22.4 L����������ԭ����Ϊ2NA | |
| C�� | 46 g NO2��N2O4�Ļ���ﺬ�еĵ�ԭ����Ϊ1NA | |
| D�� | ���ʵ���Ũ��Ϊ0.5 mol/L��MgCl2��Һ�У�����Cl- ����Ϊ NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 25��ʱ��CH3COOH��CH3COONa�Ļ����Һ������û��ҺpH=6������Һ�У�c��CH3COO-����c��Na+�� | |
| B�� | Ϊȷ��ij��H2A��ǿ�ỹ�����ᣬ�ɲ�NaHA��Һ��pH����pH��7����H2A�������pH��7����H2A��ǿ�� | |
| C�� | ����п�ֱ�͵�����������ʵ���Ũ�ȵ�����ʹ��ᷴӦʱ����H2������ȣ��ų�H2�����ʲ��� | |
| D�� | ��ͬ�¶��£��������Ȼ�������ֱ������ͬ����Ģ�����ˮ����0.1mol/L���ᡢ��0.1mol/L�Ȼ�þ��Һ����0.1 mol/L��������Һ�У�Ag+Ũ�ȣ��٣���=�ڣ��� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com