
【题目】电解法制备磷酸二氢钾(KH2PO4)装置如图所示。下列说法正确的是
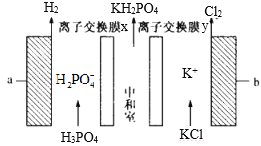
A.与 a 相连接的电源电势比 b 的高
B.离子交换膜 x、y 分别为阳离 子、阴离子交换膜
C.电解时,理论上相同时间内通过交换膜的阴、阳离子数相等
D.当外电路中通过 1mol 电子时,会有ll.2L的Cl2生成
【答案】C
【解析】
根据图示,通电的条件下,a电极上H+得电子变为H2,发生还原反应,b电极上Cl-失电子转化为Cl2,发生氧化反应,则a电极为阴极,与电源正极相连,b电极为阳极,与电源正极相连,![]() 通过离子交换膜x进入中和室,K+通过离子交换膜y进入中和室,在中和室中生成磷酸二氢钾(KH2PO4),则离子交换膜x为阴离子交换膜,离子交换膜y为阳离子交换膜,据此分析解答。
通过离子交换膜x进入中和室,K+通过离子交换膜y进入中和室,在中和室中生成磷酸二氢钾(KH2PO4),则离子交换膜x为阴离子交换膜,离子交换膜y为阳离子交换膜,据此分析解答。
A.根据分析,a电极为阴极,与电源正极相连,b电极为阳极,与电源正极相连,原电池中正极的电势高于负极,则与 b相连接的电源电势比a的高,故A错误;
B.根据分析,离子交换膜x为阴离子交换膜,离子交换膜y为阳离子交换膜,故B错误;
C.电解时,![]() 通过离子交换膜x进入中和室,K+通过离子交换膜y进入中和室,二者都带一个单位的电荷,根据得失电子守恒,理论上相同时间内通过交换膜的阴、阳离子数相等,故C正确;
通过离子交换膜x进入中和室,K+通过离子交换膜y进入中和室,二者都带一个单位的电荷,根据得失电子守恒,理论上相同时间内通过交换膜的阴、阳离子数相等,故C正确;
D.b电极上Cl-失电子转化为Cl2,电极反应为:2Cl--2e-= Cl2,当外电路中通过 2mol 电子时,会有1mol Cl2生成,标准状况下的体积为22.4L,则外电路中通过 1mol 电子时,会有标况下ll.2L的Cl2生成,题中选项未给出气体的状态条件,则生成的氯气体积不一定为11.2L,故D错误;
答案选C。


科目:高中化学 来源: 题型:
【题目】填写下列各空:
(1)写出![]() 中官能团的名称为_____;
中官能团的名称为_____;
(2)![]() 的分子式为_____,分子中一定共面的原子有_____个;
的分子式为_____,分子中一定共面的原子有_____个;
(3)有机物M(![]() )为苯的同分异构体,M的二氯代物的同分异构体有__种;
)为苯的同分异构体,M的二氯代物的同分异构体有__种;
(4)用系统命名法对下列有机物进行命名:
①CH3C(CH3)=CHCH3:_____;
②CH3CH(CH2CH3)CH(CH3)CH2CH3:_____。
(5)根据下列高分子化合物回答问题
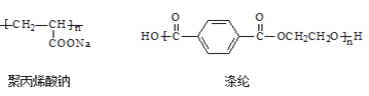
①合成聚丙烯酸钠的单体的结构简式是_____________;
②合成涤纶有两种单体,其中能和 NaHCO3 反应的单体的结构简式是_____________,其核磁共振氢谱的峰面积比是_____________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组研究在其他条件不变时,改变密闭容器中某一条件对A2(g)+3B2(g)2AB3(g)化学平衡状态的影响,得到如图所示的曲线(图中T表示温度,n表示物质的量)下列判断正确的是
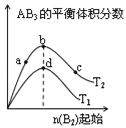
A. 图中T2一定大于T1
B. 图中b点速率一定大于d点速率
C. 达到平衡时,A2的转化率大小为:c>b>a
D. 加入催化剂可以使状态d变为状态b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】TMB是一种新型指纹检测的色原试剂,由碳、氢、氮三种元素组成,M=240g/mol。某研究性学习小组的同学欲利用下列仪器测定TMB的分子式。主要过程为在足量氧气流中将4.80 g TMB样品氧化(氮元素转化为N2),再利用吸收剂分别吸收水蒸气和CO2。请从图中选择适当的装置(装置符合气密性要求,加热装置等已略去,其他用品可自选)。
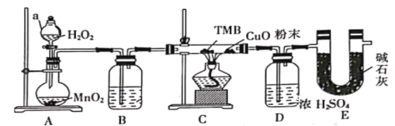
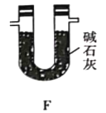
(1)写出仪器a的名称__________,A中的化学反应方程式:___________;
(2)B中试剂是___________,作用是________________ ;
(3)装置C中CuO粉末的作用为________________。
(4)理想状态下,将4.80 gTMB样品完全氧化,点燃C处酒精灯,实验结束时测得D增加3.60 g,E增加14.08 g,则TMB的分子式为____________。
(5)有同学认为,用该实验装置测得的TMB分子式不准确,应在干燥管E后再添加一个装有碱石灰的干燥管F。你认为是否需要添加F装置__________(填“需要”或“不需要”),简述理由________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】历史上曾利用“地康法”制氯气,其原理是以氯化铜作催化剂,利用氧气氧化氯化氢。如图为“地康法”制氯气的模拟装置.下列关有说法不正确的是
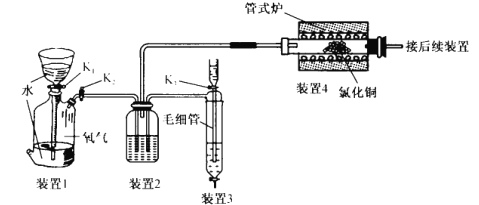
A.关闭 K2打开K1, 若漏斗中的液面不持续下降 ,则装置1的气密性良好
B.打开K3 ,将浓盐酸逐滴滴入浓硫酸中可制备反应所需要的氯化氢
C.装置 2 中盛放的是浓硫酸,通过观察气泡逸出的快慢可判断气体的通入量
D.后续需要净化氯气的装置中 ,除杂试剂依次为饱和食盐水、碱石灰
查看答案和解析>>
科目:高中化学 来源: 题型:
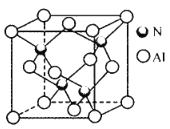
【题目】金属氮化物具有高熔点、高硬度、高化学稳定性以及良好的导热、导电性,目前已经广泛应用于磁学、电子工业 、耐高温结构陶瓷等领域 。回答下列问题
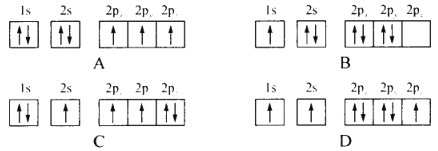
(1)下列不同状态的氮原子其能量最高的是________(填字母),基态氮原子处于最高能级的电子其电子云轮廓图形状为________
(2)第一电离能I1(N)______(填“> ”“< ”或“=”)I1(P),其原因是_____________。
(3)A和B两种金属的含氮化合物的结构如图所示:
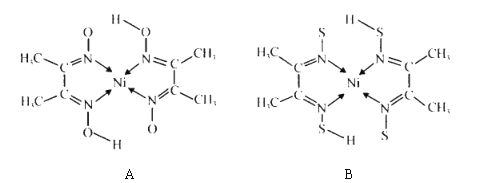
①基态 Ni 原子的核外电子排布式为[ Ar]________________。
②物质A 中碳原子的杂化方式为__________________。
③A的熔点高于 B 的,具主要原因是_______。
④B中含有的化学键类型有_____________(填字母)。
a.金属键 b. σ建
c.π键 d. 配位键
(4)氮化铝晶胞如图所示。氮原子的配位数为_______,每个铝原子周围紧邻__________个铝原子;已知立方氮化铝晶体密度为ρg cm-3,晶胞中最近的两个铝原子之间的距离为___pm(列出计算式即可,阿伏加德罗常数为6. 02×1023mol -1)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组中的反应,属于同一反应类型的是
A. 由溴丙烷水解制丙醇;由丙烯与水反应制丙醇
B. 由甲苯硝化制对硝基甲苯;由甲苯氧化制苯甲酸
C. 由氯代环己烷消去制环己烯;由丙烯加溴制![]() 二溴丙烷
二溴丙烷
D. 由乙酸和乙醇制乙酸乙酯;由苯甲酸乙酯水解制苯甲酸和乙醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有三种金属单质A、B、C,其中A的焰色反应为黄色,B、C是常见金属。三种金属单质A、B、C能与气体甲、乙、丙及物质D、E、F、G、H之间发生如下转化关系(图中有些反应的产物和反应的条件没有标出)。
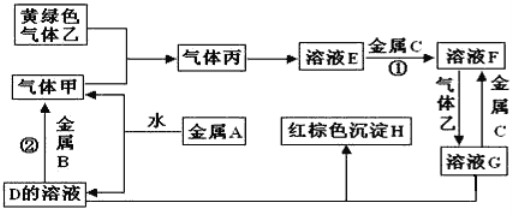
请根据以上信息回答下列问题
(1)写出下列物质的化学式:A__;H ___; G____;乙___。
(2)写出下列反应的化学方程式:
反应①_______;
反应②________。
(3)检测溶液G中金属离子的常用方法是:____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新冠肺炎疫情期间,多种含氯消毒剂如84消毒液、Cl2、NaClO2等对病毒均具有很好的消杀作用,其中亚氯酸钠(NaClO2)在工业上常以ClO2气体为原料制备,实验室制备亚氯酸钠的装置如图所示(夹持装置已略)。
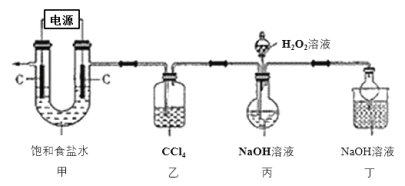
已知:①控制电压电解饱和食盐水可得到ClO2;
②Cl2易溶于CCl4;
③亚氯酸钠在不同温度下的溶解度如下表所示:
温度℃ | 20 | 40 | 60 |
溶解度/g | 6.2 | 23.4 | 48.3 |
回答下列问题:
(1)装置甲中产生ClO2的电极反应式为_____________________。
(2)装置乙中CCl4的作用为________________________________。
(3)装置丙中生成NaClO2的化学方程式为____________________________。
(4)从装置丙反应后的溶液中获得NaClO2晶体的步骤如下:
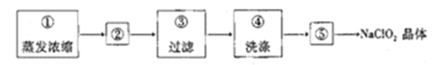
其中步骤①加热到_________________(填现象)时停止加热,步骤②是__________________。
(5)准确称取2.26gNaClO2粗品,加入盛有20.00mL刚煮沸并冷却过的水、足量10%的稀硫酸和30.00mL质量分数为40%的KI溶液(足量)的碘量瓶中,立即密封并摇晃碘量瓶至试样完全反应,再加入淀粉作指示剂用浓度为3.00mol/L的Na2S2O3溶液滴定(已知整个过程中发生的反应依次为![]() +4I-+4H+=2I2+Cl-+2H2O,
+4I-+4H+=2I2+Cl-+2H2O,![]() ),
),
①若三次平行实验测得消耗的Na2S2O3溶液的平均体积为30.00mL,则粗品的纯度为_________________%(保留三位有效数字),
②若使用的水未煮沸,则测定结果会___________________(填“偏高”“偏低”或“无影响”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com