
| A. | ①③⑤⑥ | B. | ①②⑤⑥ | C. | ②③④⑥ | D. | ③④⑤⑥ |
分析 分析操作对溶质的物质的量或溶液的体积的影响,根据c=$\frac{n}{V}$判断不当操作对所配溶液浓度影响.
解答 解:①用天平(使用游码)称量时,被称量物与砝码的位置放颠倒了,实际称量药品的质量减小,所配溶液难度偏低,故①符合;
②未冷却到室温就转移到容量瓶中定容,实际溶液体积偏低,所配溶液浓度偏高,故②不符合;
③溶液转移到容量瓶后,烧杯及玻璃棒未用蒸馏水洗涤,移入容量瓶中溶质的物质的量偏小,所配溶液浓度偏低,故③符合;
④转移溶液前容量瓶内有少量蒸馏水,对所配溶液无影响,故④不符合;
⑤定容时,仰视容量瓶的刻度线,所配溶液体积偏大,溶液浓度偏低,故⑤符合;
⑥定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线,导致溶液体积偏大,所配溶液浓度偏小,故⑥符合.
所以①③⑤⑥符合.
故选A.
点评 本题考查配制一定物质的量浓度的溶液的实验操作误差分析及对物质的量浓度的理解,难度不大,抓住c=$\frac{n}{v}$分析是解题的关键.


 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案科目:高中化学 来源: 题型:选择题
| A. | H+、Fe2+、Mg2+、Cl- | B. | Cl-、CO32-、Cu2+、Mg2+ | ||
| C. | H+、NO3-、SO42-、K+ | D. | NO3-、OH-、Ba2+、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 透闪石的化学式写成氧化物的形式为2CaO•5MgO•8SiO2•H2O | |
| B. | 透闪石中Mg的质量分数是Ca的质量分数的1.5倍 | |
| C. | 1molCa2Mg5Si8O22(OH)2与足量盐酸作用,至少需要14molHCl | |
| D. | 透闪石是一种新型无机非金属材料,难溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2C2H2(g)+5O2(g) 4CO2(g)+2H2O(l);△H=-4b kJ/mol | |
| B. | C2H2(g)+$\frac{5}{2}$O2(g) 2CO2(g)+H2O(l);△H=2b kJ/mol | |
| C. | 2C2H2(g)+5O2(g) 4CO2(g)+2H2O(l);△H=-2b kJ/mol | |
| D. | 2C2H2(g)+5O2(g) 4CO2(g)+2H2O(l);△H=b kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
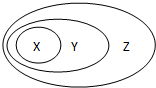 用如图表示的一些物质或概念之间的从属或包含关系中,错误的是( )
用如图表示的一些物质或概念之间的从属或包含关系中,错误的是( )| X | Y | Z | |
| A | 盐酸 | 分散系 | 混合物 |
| B | 铜 | 金属元素 | 元素 |
| C | 氧化铝 | 电解质 | 化合物 |
| D | KHSO4 | 酸 | 无机物 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com