
| 选项 | 实验 | 现象 | 结论 |
| A | 向KI溶液中加入CCl4,振荡后静置 | 液体分层,下层呈紫红色 | 碘易溶于CCl4,难溶于水 |
| B | 用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热 | 熔化后的液态铝滴落下来 | 金属铝的熔点较低 |
| C | 向含有酚酞的Na2CO3溶液中加入少量的BaCl2固体 | 溶液红色变浅 | 证明Na2CO3溶液中存在水解平衡 |
| D | 向亚硫酸钠试样中滴入盐酸酸化的Ba(ClO)2溶液 | 产生白色沉淀 | 试样已氧化变质 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.碘离子无色,且不溶于四氯化碳;
B.化铝的熔点高,像网兜一样包裹在Al的外面;
C.Na2CO3溶液水解显碱性,加氯化钡使水解平衡逆向移动;
D.滴入盐酸酸化的Ba(ClO)2溶液,HClO可氧化亚硫酸钠.
解答 解:A.向KI溶液中加入CCl4,振荡后静置,碘离子不溶于四氯化碳,题中现象及结论都不合理,故A错误;
B.Al在加热时生成氧化铝,氧化铝的熔点高,像网兜一样包裹在Al的外面,则仔细打磨过的铝箔在酒精灯上加热,铝箔熔化但不滴落,故B错误;
C.Na2CO3溶液水解显碱性,加氯化钡使水解平衡逆向移动,则由溶液颜色的变化可知Na2CO3溶液中存在水解平衡,能够达到实验目的,故C正确;
D.滴入盐酸酸化的Ba(ClO)2溶液,HClO可氧化亚硫酸钠,应溶于水,应该加加氯化钡检验是否变质,故D错误;
故选C.
点评 本题考查化学实验能力的评价,题目难度不大,涉及铝及其化合物性质、物质检验、水解平衡等知识,明确常见元素及其化合物性质为解答关键,试题培养了学生的分析能力及综合应用能力.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 常温下,pH=2的硫酸溶液中,由水电离出的H+个数为10-12NA | |
| B. | 标准状况下,1.12L二氯甲烷含氯离子数为0.2NA | |
| C. | 向过量FeI2溶液中通入Cl2,当有1mol Fe2+被氧化时,转移的电子数为3NA | |
| D. | 2molNH3与3molO2在催化剂作用下加热充分反应后,所得NO分子数小于2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验要求 | 化学试剂 |
| (1)检验酒精中是否有水 | ④ |
| (2)吸收CO中的H2O | ② |
| (3)验证味精中是否有食盐 | ① |
| (4)分离碘水中的碘 | ③ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 乙烷(乙烯):将混合气体通过酸性高锰酸钾溶液,洗气 | |
| B. | 苯(苯酚):向混合液中加入适量的浓溴水,过滤 | |
| C. | 乙酸乙酯(乙酸、乙醇):向混合液中加入饱和碳酸钠溶液,分液 | |
| D. | 硝基苯(NO2):向溶有杂质的硝基苯中加入一定量的浓氢氧化钠溶液,振荡,分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含有AgBr和AgI固体的悬浊液:c(Ag+)>c(Br-)=c(I-) | |
| B. | 25℃时,0.1mol•L-1醋酸溶液PH=a,0.01mol•L-1醋酸溶液PH=b,则b=a+1 | |
| C. | 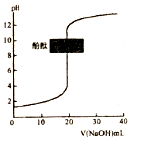 常温下,图表示以酚酞作指示剂,用0.1mol•L-1NaOH溶液滴定未知浓度的盐酸,滴定至终点时,溶液一定呈中性 | |
| D. | 向0.1mol•L-1的氨水中加入硫酸铵固体,则溶液中c(OH-)/c(NH3•H2O)减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
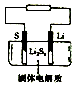 石墨烯锂硫电池是一种高效、低污染的新型二次电源,其装置如图所示.电池反应为 2Li+nS=Li2Sn.Li+可在固体电解质中迁移.下列说法不正确的是( )
石墨烯锂硫电池是一种高效、低污染的新型二次电源,其装置如图所示.电池反应为 2Li+nS=Li2Sn.Li+可在固体电解质中迁移.下列说法不正确的是( )| A. | 放电时,锂在负极上发生氧化反应 | |
| B. | 放电时,正极的电极反应式为nS+2e-+2Li+=Li2Sn | |
| C. | 充电时,锂电极为阴极,与电源负极相连 | |
| D. | 充电时,理论上阳极失去2mol电子生成32g硫 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
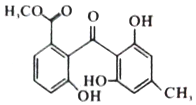
| A. | 化合物X分子式为C16H12O6 | |
| B. | 化合物X含有醚健、羰基,羟基三种官能团 | |
| C. | lmol化合物X最多可与4mol Br2发生反应 | |
| D. | lmol化合物X最多能与3mol NaOH反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| 氢氧化物 | 开始沉淀时的pH | 完全沉淀时的pH |
| Mg(OH)2 | 9.3 | 10.8 |
| Fe(OH)2 | 7.6 | 9.6 |
| Fe(OH)3 | 2.7 | 3.7 |
| Al(OH)3 | 3.7 | 4.7 |
| A. | 反应①中H2O2主要用于还原剂 | |
| B. | 滤渣1和滤渣2都不能溶于NaOH溶液 | |
| C. | 反应③发生主要反应的离子方程式:H++OH-═H2O | |
| D. | 以滤渣2为原料可以制备涂料铁红 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 放电过程中,正极的电极反应式为NiOOH+H2O+e-═Ni(OH)2+OH- | |
| B. | 放电时,电子由负极→正极→电解质溶液→负极,形成闭合回路 | |
| C. | 充电时,阴极附近溶液pH 降低 | |
| D. | 充电过程中,OH-从阳极向阴极迁移 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com