
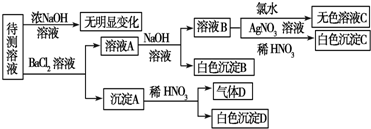
分析 由沉淀A与稀硝酸反应仍得到白色沉淀知白色沉淀D为BaSO4,故溶液中SO42-、SO32-至少有一种;由每次实验所用试剂均足量知溶液A中含有Ba2+,在加入碱后能得到白色沉淀B,则原待测溶液中一定含有HCO3-;溶液B中加入足量的氯水后仍得到无色溶液,说明原待测液中无Br-,不能确定是否有NO3-、CO32-、Cl-;
若气体D遇空气变红色时,表明D中肯定有NO,沉淀A中肯定有BaSO3;
原子序数不大于20的金属阳离子有Li+、Be2+、Na+、Mg2+、Al3+、K+、Ca2+,Al3+与HCO,SO42-、SO32-与Ca2+不能大量共存,故金属阳离子不可能是Al3+或Ca2+,由待测溶液与浓NaOH溶液混合后无明显变化知溶液中没有Mg2+,结合Mn+为常见离子且原子序数不大于20知,Mn+只能是Na+或K+,可通过焰色实验来确定是钾还是钠,以此解答该题.
解答 解:由沉淀A与稀硝酸反应仍得到白色沉淀知白色沉淀D为BaSO4,故溶液中SO42-、SO32-至少有一种;由每次实验所用试剂均足量知溶液A中含有Ba2+,在加入碱后能得到白色沉淀B,则原待测溶液中一定含有HCO3-;溶液B中加入足量的氯水后仍得到无色溶液,说明原待测液中无Br-,不能确定是否有NO3-、CO32-、Cl-;
若气体D遇空气变红色时,表明D中肯定有NO,沉淀A中肯定有BaSO3;
原子序数不大于20的金属阳离子有Li+、Be2+、Na+、Mg2+、Al3+、K+、Ca2+,Al3+与HCO,SO42-、SO32-与Ca2+不能大量共存,故金属阳离子不可能是Al3+或Ca2+,由待测溶液与浓NaOH溶液混合后无明显变化知溶液中没有Mg2+,结合Mn+为常见离子且原子序数不大于20知,Mn+只能是Na+或K+,可通过焰色实验来确定是钾还是钠,
(1)根据以上分析可知,原待测溶液中一定含有HCO3-;一定没有无Br-;沉淀D为:BaSO4,
故答案为:HCO3-;Br-;BaSO4;
(2)因为待测液加入BaCl2溶液和稀HNO3生成了BaSO4沉淀,BaSO4的生成可能来自SO42-或SO32-中的一种或两种;
若气体D遇空气变红色时,表明D中肯定有NO,沉淀A中肯定有BaSO3,生成沉淀D的离子方程式为:3BaSO3+2H++2NO3-═2NO↑+3BaSO4↓+H2O,
沉淀B为碳酸钡,反应的离子方程式为:HCO3-+Ba2++OH-═BaCO3↓+H2O,
故答案为:D;3BaSO3+2H++2NO3-═2NO↑+3BaSO4↓+H2O;HCO3-+Ba2++OH-═BaCO3↓+H2O;
(3)原子序数不大于20的金属阳离子有Li+、Be2+、Na+、Mg2+、Al3+、K+、Ca2+,Al3+与HCO,SO42-、SO32-与Ca2+不能大量共存,故金属阳离子不可能是Al3+或Ca2+,由待测溶液与浓NaOH溶液混合后无明显变化知溶液中没有Mg2+,结合Mn+为常见离子且原子序数不大于20知Mn+只能是Na+或K+,可通过焰色实验来确定是钾还是钠,方法是:做焰色反应实验,若透过蓝色钴玻璃片观察到紫色火焰,说明是钾;若不透过蓝色钴玻璃片观察到黄色火焰,则说明是钠,
故答案为:做焰色反应实验,若透过蓝色钴玻璃片观察到紫色火焰,说明是K+,若不透过蓝色钴玻璃片观察到黄色火焰,则说明是Na+.
点评 本题考查元素化合物的特性和反应,用框图设问可以考查学生正向思维、逆向思维、发散和收敛思维,能根据题眼正确判断化合物是解本题的关键,注意所加BaCl2、H2SO4、HNO3、NaOH均过量,硝酸能把亚硫酸钡氧化成硫酸钡.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
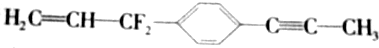 为已知结构,下列叙述中正确的是( )
为已知结构,下列叙述中正确的是( )| A. | 除苯环外的其余碳原子有可能都在同一条直线上 | |
| B. | 在同一平面上的原子最多有19个 | |
| C. | 12个碳原子不可能都在同一个平面上 | |
| D. | 12个碳原子有可能都在同一个平面上 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | D元素处于元素周期表中第二周期VIA族 | |
| B. | 四种元素的原子半径:A<B<C<D | |
| C. | B、D的最高价氧化物具有相似的物理性质和化学性质 | |
| D. | 一定条件下,B单质能置换出D单质,C单质能置换出A单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 其原子最外电子层有7个电子的元素 | |
| B. | 最高正价为+3的元素 | |
| C. | 其原子最外层电子数大于电子层的元素 | |
| D. | 最高价氧化物对应的水化物是酸的元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入过量氨水,有白色沉淀生成,则原溶液一定有Al3+ | |
| B. | 向某溶液中滴加稀盐酸,生成的无色无味气体能使澄清的石灰水变浑浊,则原溶液中一定含有CO32- | |
| C. | 加入盐酸酸化的BaCl2溶液,有白色沉淀生成,则原溶液一定有SO42- | |
| D. | 向Ca(ClO)2溶液通入CO2,溶液变浑浊,再加入品红溶液,红色褪去 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
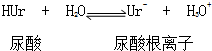 ②Ur-(aq)+Na+(aq)?NaUr(s)
②Ur-(aq)+Na+(aq)?NaUr(s)| A. | 反应的△H>0 | B. | 反应的△H=0 | ||
| C. | 升高温度平衡向正反应方向移动 | D. | 降低温度平衡向正反应方向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
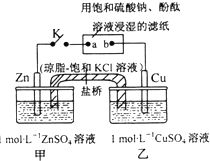
| A. | Zn极上发生还原反应 | |
| B. | 电子沿Zn→a→b→Cu路径流动 | |
| C. | 片刻后,乙池中c(Cu2+)减小,c(SO42-)基本不变,溶液不再保持电中性 | |
| D. | 片刻后可观察到滤纸a点变红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCO3-离子在该溶液中一定不能大量共存 | |
| B. | 该溶液的pH一定是13 | |
| C. | 向该溶液中加入铝片后,一定能生成氢气 | |
| D. | 若该溶液的溶质只有一种,它一定是酸或碱 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com