


 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案 小学期末标准试卷系列答案
小学期末标准试卷系列答案科目:高中化学 来源: 题型:阅读理解
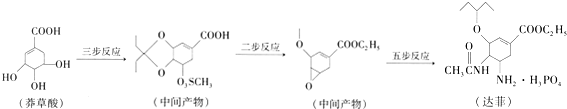
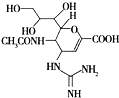
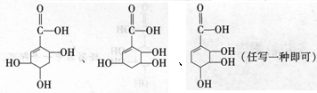



查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
现有六种元素A、B、C、D、E、F均为周期表中前20号元素,且原子序数依次增大。已知A和B是形成化合物种类最多的两种元素;B元素和C元素通常形成电子数为14或22的化合物。D元素的原子半径是短周期主族元素中最大的;E元素在地壳中含量居第二位;F是组成人体骨骼的牙齿的主要元素。
请回答以下问题:
(1)请画出F的离子结构示意图: ;由C、A两种元素形成的18电子化合物的电子式为 ;
(2)工业上制取E单质的化学方程式为: ;
(3)由以上六种元素两两组合所形成的化合物中,既含有离子键又含有非极性共价键的常见化合物有 和 (填化学式);它们都能与水反应生成气体,写出其中一个属于非氧化化还原反应的化学方程式 ;
(4)由A、B两种元素形成的正四面体分子是一种常见的气体燃料。通常状况下1g该物质完全燃烧生成液态水时所释放的能量为51.25kg/mol,请写出表示其燃烧热的热化学方程式: ;
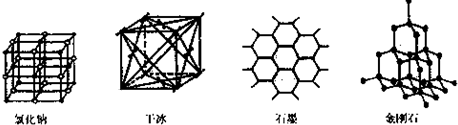
(5)下图是中学常见的几种晶体结构。有关说法正确的是 (填选项)。
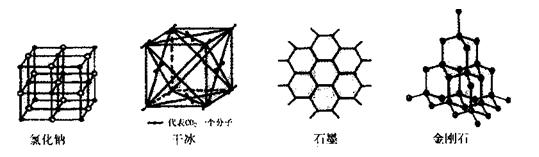
A.氯化钠的晶体结构中,和钠离子最近且等距离的氯离子组成了一个正八面体
B.干冰晶体是CO2分子通过范德华力结合形成的
C.石墨晶体中碳原子数与所形成的共从键数目之比为2:3
D.金刚石晶体是由五个碳原子形成的正四面体分子构成的
查看答案和解析>>
科目:高中化学 来源:浙江省模拟题 题型:填空题

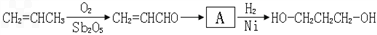
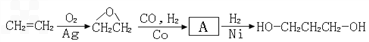
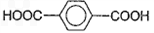 )为原料可以合成聚酯PTT,写出其化学方程式 ______________。
)为原料可以合成聚酯PTT,写出其化学方程式 ______________。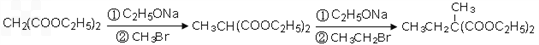
 ,再转化为
,再转化为 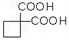 。
。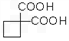 的同分异构体不可能属于__________。
的同分异构体不可能属于__________。 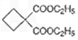 ,必须先合成哪些物质?(用合成该物质的化学方程式回答) __________。
,必须先合成哪些物质?(用合成该物质的化学方程式回答) __________。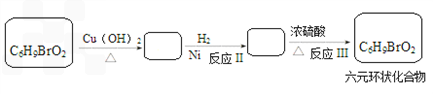
查看答案和解析>>
科目:高中化学 来源: 题型:
(10)(1)(6分)2mol CO2中含______ mol碳原子__________个氧原子(以NA为阿伏加德罗常数的值),标准状况下的体积为___________L,质量是______________g。1 mol·L-1的CaCl2 溶液0.5L,Cl- 离子的物质的量浓度为___________、Ca2+物质的量为 。
(2))(4分)有以下几种物质①干燥的食盐晶体 ②液态氯化氢 ③水银 ④蔗糖 ⑤醋酸 ⑥KNO3溶液 ⑦氨气 ⑧碳酸钙 ⑨二氧化硫 填空回答(填序号):
(1)以上物质中属于强电解质的是 ;
(2)以上物质中属于非电解质的是 ;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com