
在一定温度下发生可逆反应A(g)+3 B(g)  2C(g),下列叙述中不能判断该反应达到平衡状态的是( )
2C(g),下列叙述中不能判断该反应达到平衡状态的是( )
A.C的生成速率与C的分解速率相等
B.单位时间内生成amolA,同时生成3amolB
C.A、B、C的浓度不再变化
D.单位时间内消耗amolA,同时生成3amolB
 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案科目:高中化学 来源: 题型:
一定条件下,可逆反应N2 + 3H2 2NH3达到化学平衡状态,下列说法一定正确的是
2NH3达到化学平衡状态,下列说法一定正确的是
A.每1 mol N≡N断裂的同时有2 mol N—H生成
B.N2、H2、NH3的浓度之比为1:3:2
C.N2减少的速率和NH3减少的速率之比为1:2
D.气体体积为初始体积的1/2
查看答案和解析>>
科目:高中化学 来源: 题型:
运用物质结构的知识完成下列问题。
(1)第一电离能介于B、N之间的第二周期元素有 ▲ (填元素符号)。
(2)配离子[TiCl(H2O)5]2+的中心离子化合价为 ▲ ,配体的化学式为 ▲ 。
(3)BF3与一定量水形成(H2O)2·BF3晶体Q,Q在一定条件下可转化为R:

Q R
①晶体Q中不存在的作用力为 ▲ (填字母)。
A.共价键 B.离子键 C.配位键 D.范德华力 E.氢键
②R中阳离子的空间构型为 ▲ 。
(4)硼砂是含结晶水的四硼酸钠,其阴离子Xm—(含B、O、H三种元素)的球棍模型如下图3所示。则m= ▲ (填数字)。
(5)以四氯化钛、碳化钙、叠氮酸盐(如NaN3)作原料,可以生成碳氮化钛化合物,其结构是用碳原子取代氮化钛晶胞(结构如下图4)所有顶点的氮原子,这种碳氮化钛化合物的化学式为 ▲ 。


图3 图4
(6)部分化学键的键能见下表:
| 化学键 | Si—O | Si—Cl | H—H | H—Cl | Si—Si | Si—C |
| 键能/ kJ·mol—1 | 460 | 360 | 436 | 431 | 176 | 347 |
①比较下列两组物质的熔点高低 (填“>”或“<”)
SiC______ Si; SiCl4 ______ SiO2
②工业上高纯硅可通过下列反应制取:SiCl4 (g) + 2H2(g)  Si(s) + 4HCl(g)
Si(s) + 4HCl(g)
计算该反应的反应热△H = ___________ kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
在如图所示的装置中,a的金属性比氢要强,b为碳棒,关于此装置的各种叙述不正确的是 ( )
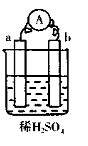
A.碳棒上有气体放出,溶液pH变大
B.a是负极,b是正极
C.导线中有电子流动,电流从a极到b极
D.a极上发生了氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
关于如图所示①、②两个装置的叙述,正确的是( )

A.装置名称:①是原电池,②是电解池
B.硫酸浓度变化:①增大,②减小
C.电极反应式:①中阳极:4OH---4e-=2H2O+O2↑②中正极:Zn--2e-=Zn2+
D.离子移动方向:①中H+向阴极方向移动 ②中H+向负极方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C均为短周期元素,A、B同周期,A、C的最低价阴离子分别为A2-、C-,A2-离子半径大于C-,B2+与C-具有相同的电子层结构。下列叙述中一定不正确的是( )
A. 它们的原子序数A>B>C B. 它们的原子半径C>B>A
C. 它们的离子半径A2->C->B2+ D. 它们的最外层电子数C>A>B
查看答案和解析>>
科目:高中化学 来源: 题型:
已知常温下在溶液中可发生如下两个离子反应:
Ce4++Fe2+===Fe3++Ce3+
Sn2++2Fe3+===2Fe2++Sn4+
由此可以确定Fe2+、Ce3+、Sn2+三种离子的还原性由强到弱的顺序是 ( )
A.Sn2+、Fe2+、Ce3+ B.Sn2+、Ce3+、Fe2+
C.Ce3+、Fe2+、Sn2+ D.Fe2+、Sn2+、Ce3+
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录如下,则卡片上描述合理的是( )。
①Cu为负极,Zn为正极
②Cu极上有气泡产生,发生还原反应
③SO42- 向Cu极移动
④若有0.5 mol电子流经导线,则可产生0.25 mol气体
⑤电子的流向是:Cu―→Zn
⑥正极反应式:Cu+2e-===Cu2+,发生氧化反应
A.①②③ B.②④⑥ C.③④⑤ D.②④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com