
| A. | Br2在反应中表现还原性 | B. | SO2在反应中被还原 | ||
| C. | Br2在反应中失去电子 | D. | 1mol Br2在反应中得到2mol电子 |
分析 化学反应为Br2+SO2+2H2O═2HBr+H2SO4,Br元素的化合价由0降低为-1价,S元素的化合价由+4价升高到+6价,以此来解答.
解答 解:A.因Br元素的化合价由0降低为-1价,Br2在反应中作氧化剂,表现氧化性,故A错误;
B.S元素的化合价由+4价升高到+6价,SO2作还原剂,被氧化,故B错误;
C.Br元素的化合价由0降低为-1价,则Br2在反应中得到电子,故C错误;
D.因Br元素的化合价由0降低为-1价,Br2在反应中作氧化剂,则1mol氧化剂在反应中得到1mol×2×(1-0)=2mol,故D正确;
故选D.
点评 本题考查氧化还原反应,明确反应中元素的化合价的变化是解答本题的关键,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 金属性最强的为铍 | B. | 原子半径最小的是锂 | ||
| C. | 单质与氢气最容易反应的元素是氟 | D. | 单质化学性质最稳定的碳 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=5的硝酸溶液或AlCl3溶液中,由水电离出的C(H+)均为10-9mol•L-1 | |
| B. | 将PH=3的硫酸溶液和PH=11的氨水等体积混合后,混合液pH<7 | |
| C. | 在c(OH-):c(H+)=l:1012的溶液中,Na+、Ca2+、NO3-、I-能大量共存 | |
| D. | CH3COONa溶液和盐酸混合呈中性的溶液中:c(Na+)<c(C1-)=c(CH3COOH) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素周期表中只有第2列元素的原子最外层有2个电子 | |
| B. | 除短周期外,其他周期均有 18 个元素 | |
| C. | 副族元素中没有非金属元素 | |
| D. | 碱金属元素是指ⅠA 族的所有元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 某科研小组公司开发了Li-SO2Cl2军用电池,其示意图如图所示,已知电池反应为:2Li+SO2Cl2═2LiCl+SO2↑;下列叙述中错误的是( )
某科研小组公司开发了Li-SO2Cl2军用电池,其示意图如图所示,已知电池反应为:2Li+SO2Cl2═2LiCl+SO2↑;下列叙述中错误的是( )| A. | 电池工作时负极材料是Li,发生氧化反应 | |
| B. | 将电解质溶液改为LiCl的水溶液,电池性能会更好 | |
| C. | 电池工作时电子流向:锂电极→导线→负载→碳棒 | |
| D. | 电池工作过程中,石墨电极反应式为SO2Cl2+2e-═2Cl-+SO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯和甲苯互为同系物,都能使高锰酸钾褪色 | |
| B. | 对二甲苯与氢气完全加成的产物的一氯代物有3种 | |
| C. | 等物质的量的苯和苯甲酸完全燃烧消耗氧气的量不相等 | |
| D. | 淀粉、油脂、蛋白质的水解产物都是非电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
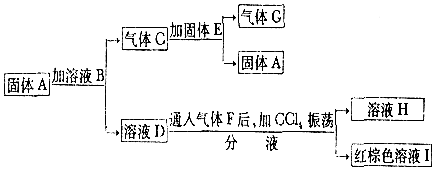
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com