
碳酸钡是一种重要的无机盐产品,广泛应用于工业陶瓷、光学玻璃、建筑等行业。碳化法生产碳酸钡的工艺流程示意图如下:

已知:重晶石的主要成分是BaSO4;Ba(HS)2溶液呈弱碱性;2BaS+2H2O=Ba(OH)2+Ba(HS)2。
回答下列问题:
(1)煅烧时发生反应的化学方程式为 ,该反应的氧化产物的电子式为 ;当温度过高时,尾气中有毒气体的含量会升高,原因是 (用化学方程式表示)。
(2)为了提高浸取速率,可采取的措施是 (任写一种)。
(3)碳化时发生反应的离子方程式为 。
(4)脱硫过程是用Na2CO3溶液将BaCO3浆液中含有的BaS2O3除去:CO32-+BaS2O3=BaCO3+S2O32-,该反应的平衡常数为 【已知Ksp(BaCO3)=2.5×10-9,Ksp(BaS2O3)=1.6×10-5】。
(5)Ba(HS)2溶液中离子浓度由大到小的顺序为 。
(6)BaCO3不能用于医疗用的“钡餐”,原因是 。
科目:高中化学 来源:2016-2017学年四川省高一12月月考化学卷(解析版) 题型:选择题
下列物质能通过化合反应得到的是①NaAlO2;②NaHCO3;③Fe(OH)3 ④FeCl3
A.只有①②④ B.只有②③④ C.只有①③④ D.全部
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高一上月考三化学卷(解析版) 题型:填空题
某研究小组取一定质量的镁铝合金材料投入200mL稀硫酸中,待固体全部溶解后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量(n)与加入Na0H溶液的体积(F)的关系如图所示。请回答下列问题:
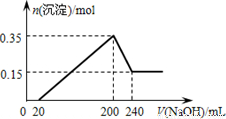
(1)加入NaOH溶液于20mL时,发生反应的离子方程式为_____________________。
(2)加入NaOH溶液体积为220mL时,沉淀的成分及其物质的量是___________。
(3)该合金材料中,镁、铝的物质的量之比为___________。
(4)H2SO4的物质的量浓度为____________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高一上月考三化学卷(解析版) 题型:选择题
实验室需配制一种仅含四种离子(不包括水电离出的离子)的无色落液,且在溶液中四种离子的物质的量浓度均为1mol/L。下列四个离子组能达到要求的是( )
A.Na+、K+、SO42-、Cl- B.Cu2+、K+、SO42-、NO3-
C.H+、K+、HCO3-、Cl- D.Mg2+、Na+、Cl-、SO42-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高一上月考三化学卷(解析版) 题型:选择题
下列各组物质,按化合物、单质、混合物的顺序排列的是( )
A.烧碱、液态氧、碘酒 B.生石灰、白磷、熟石灰
C.干冰、铁、氯化氢 D.空气、氮气、胆矾
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省南昌市等五校高二上联考二化学试卷(解析版) 题型:选择题
在一定条件下在固定容器中进行的可逆反应2M(g)+N(g) Q(g) △H>0,达到平衡状态,若升高温度,则对于该混合气体下列说法正确的是( )
Q(g) △H>0,达到平衡状态,若升高温度,则对于该混合气体下列说法正确的是( )
A.密度增大 B.平均相对分子质量增大 C总分子数增大 D.平衡逆向移动
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省南昌市等五校高二上联考二化学试卷(解析版) 题型:选择题
在不同温度下,水溶液中c(H+)与c(OH-)有如图所示关系。下列条件关于离子共存说法中正确的是( )
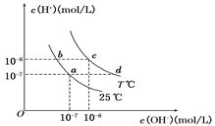
A.a点对应的溶液中大量存在:Fe3+、Na+、SCN-、SO42—
B.b点对应的溶液中大量存在:Na+、Fe3+、HCO3-、I-
C.c点对应的溶液中大量存在:Na+、Ca2+、Cl-、CO32—
D.d点对应的溶液中大量存在:Na+、K+、SO32—、Cl-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省四地六校高一上学期12月月考化学试卷(解析版) 题型:选择题
下列反应中,水既不是氧化剂又不是还原剂的是( )
A.2F2+2H2O===4HF+O2
B.NaH+H2O===NaOH+H2↑
C.2Na+2H2O===2NaOH+H2↑
D.2Na2O2+2H2O===4NaOH+O2↑
查看答案和解析>>
科目:高中化学 来源:2016-2017学年天津静海一中高一12月学业调研化学卷(解析版) 题型:选择题
向 10 mL 0.2 mol/L 的氯化铝溶液中逐滴加入未知浓度的氢氧化钡溶液,测得加入 15 mL 和加入 45 mL 时,所得沉淀一样多。则原氢氧化钡溶液的浓度为
A. 0.03 mol/L B. 0.16 mol/L C. 0.04 mol/L D. 0.08 mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com