
| A. | 这是一个氧化还原反应,Na2O2既是氧化剂,又是还原剂 | |
| B. | 这是一个氧化还原反应,Na2O2是氧化剂,CO2是还原剂 | |
| C. | 这是一个氧化还原反应,Na2O2是还原剂,CO2是氧化剂 | |
| D. | 这是一个置换反应,有单质O2产生 |
科目:高中化学 来源: 题型:解答题
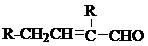
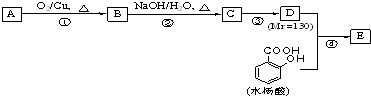
 、HOCH2CH2C≡C-C≡C-COOH、
、HOCH2CH2C≡C-C≡C-COOH、 (其中两种).
(其中两种). .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 前者多 | B. | 后者多 | C. | 一样多 | D. | 无法判断 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCl | B. | FeCl2 | C. | KOH | D. | Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验 | 现象 | 结论 |
| A | 常温下,将光亮的铁钉投入足量浓硝酸中,充分反应后滴加KSCN溶液 | 有大量红棕色气体产生,溶液变为血红色 | 铁还原浓硝酸生产NO2,铁被氧化为Fe3+ |
| B | 将氨气缓缓通入到少量AlCl3溶液中 | 先出现沉淀,后沉淀溶解 | Al(OH)3是两性氢氧化物,可溶解在碱溶液中 |
| C | 向乙酸钠溶液中滴入酚酞,微热 | 溶液先出现红色,后红色变深 | CH3COO-水解使溶液显碱性,水解反应是吸热反应 |
| D | 将装满氯水的圆底烧瓶倒置在盛有水的水槽中,日光照射 | 烧瓶内有气泡生成 | 日光照射时,溶解在水中的Cl2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol Na2O2中含有的阴离子数为2NA | |
| B. | 标准状况下,由H2O2制得2.24LO2转移的电子数目为0.4NA | |
| C. | 常温常压下,8g O3含有4 NA个电子 | |
| D. | 常温下,1L pH=2的H2SO4溶液中含有的H+数目为0.02NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
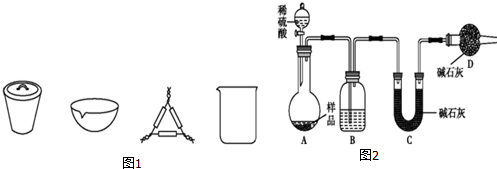
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | AgNO3 | B. | HCl | C. | BaCl2 | D. | NaOH |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com