
| 弱酸化学式 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | 1.8×l0-5 | 4.9×l0-10 | K1=4.3×l0-7 K2=5.6×l0-11 |
| A. | 等物质的量浓度的各溶液pH关系为:pH(NaCN)>pH(Na2CO3)>pH(CH3COONa) | |
| B. | 将a mol•L-1 HCN溶液与a mol•L-1 NaOH溶液等体积混合,混合液中:c(OH-)>c(H+),c(Na+)>c(CN-) | |
| C. | 冰醋酸中逐滴加水,溶液的导电性、醋酸的电离程度、pH均先增大后减小 | |
| D. | NaHCO3和Na2CO3混合液中,一定有c(Na+)+c(H+)=c(OH-)+c(HCO3-)+c(CO32-) |
分析 A、根据盐的水解规律:越弱越水解来分析,酸性顺序是:醋酸>氢氰酸>碳酸氢根,盐的水解规律:越弱越水解,所以水解能力:碳酸钠>氰化钠>醋酸钠;
B、根据溶液混合所发生的反应后溶液的组成来判断离子浓度的大小,amol•L-1HCN溶液与amol•L-1NaOH溶液等体积混合,则生成的是NaCN溶液,是强碱弱酸盐;
C、溶液的导电性和离子浓度大小有关,电离度和溶液的浓度有关,pH大小值取决于溶液的氢离子浓度大小;
D、根据溶液中的电荷守恒来分析,溶液中存在c(Na+)、c(H+),阴离子c(OH-)、c(HCO3-)、c(CO32-),阴阳离子所带电荷总数相同.
解答 解:A、根据表中酸的电离平衡常数,可以知道酸性顺序是:醋酸>氢氰酸>碳酸氢根,盐的水解规律:越弱越水解,所以水解能力:碳酸钠>氰化钠>醋酸钠,即pH(Na2CO3)>pH(NaCN)>pH(CH3COONa),故A错误;
B、amol•L-1HCN溶液与amol•L-1NaOH溶液等体积混合,则生成的是NaCN溶液,是强碱弱酸盐,溶液显碱性,c(OH-)>c(H+),c(Na+)>c(CN-)成立,故B正确;
C、冰醋酸原来没有水,然后加水溶于水电离,到达冰醋酸全部电离后,导电性最大,PH最小,继续加水,虽然总的电离的分子多了,但是氢离子和醋酸根离子浓度下降很快,导电性下降,PH增加,趋向7,无限稀释后,导电性极弱,PH≈7,所以冰醋酸中逐滴加水,溶液导电性先增强后减弱,根据越稀越电离的规律,则电离度逐渐增大,开始阶段是电离阶段,氢离子浓度逐渐增大,pH减小,达到电离平衡以后,再稀释,氢离子浓度减小,pH增大,即pH均先减小后增大,故C错误;
D、NaHCO3和Na2CO3混合溶液中,溶液存在电荷守恒:c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-),故D错误;
故选B.
点评 本题重点考查学生弱电解质的电离平衡、盐类水解原理、电解质溶液中电荷守恒应用等知识,可以根据所学内容来回答,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 铁与稀盐酸反应 2Fe+6H+═2Fe3++3H2↑ | |
| B. | 硝酸银溶液中加入铜粉 Ag++Cu═Cu2++Ag | |
| C. | 氧化铜与盐酸反应 O2-+2H+═H2O | |
| D. | 碳酸镁跟稀硫酸反应:MgCO3+2H+═Mg2++H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
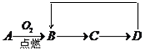 A-D是含同一元素的四种物质,相互之间有如图的转化关系,其中A是单质,D是最高价氧化物的水合物.那么A不可能是( )
A-D是含同一元素的四种物质,相互之间有如图的转化关系,其中A是单质,D是最高价氧化物的水合物.那么A不可能是( )| A. | S | B. | Si | C. | Al | D. | Fe |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
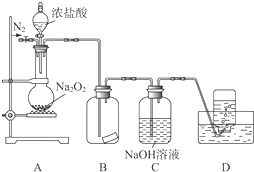 某研究性学习小组,为了探究过氧化钠的强氧化性,设计了如图的实验装置.
某研究性学习小组,为了探究过氧化钠的强氧化性,设计了如图的实验装置.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na→NaOH→NaHCO3→NaCl | B. | Al→Al2O3→Al(OH)3→AlCl3 | ||
| C. | Fe→Fe(OH)2→FeCl2→FeCl3 | D. | Si→SiO2→H2SiO3→Na2SiO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol•L-1CH3COONa溶液与0.1 mol•L-1HCl溶液等体积混合:c(Na+)=c(Cl-)>c(CH3COO-)>c(H+) | |
| B. | 0.1 mol•L-1NH4Cl溶液与0.1 mol•L-1氨水等体积混合(pH>7):c(NH3•H2O)>c(NH4+)>c(Cl-)>c(OH-) | |
| C. | 0.1 mol•L-1Na2CO3溶液与0.1 mol•L-1NaHCO3溶液等体积混合:$\frac{2}{3}$c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) | |
| D. | 0.1 mol•L-1Na2C2O4溶液与0.1 mol•L-1HCl溶液等体积混合(H2C2O4为二元弱酸):2c(C2O42-)+c(HC2O4-)+c(OH-)=c(Na+)+c(H+) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com