
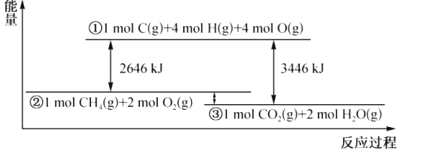
【题目】甲烷与氧气反应过程中的能量变化如图所示。下列有关说法中正确的是( )
A.CH4(g)的能量大于CO2(g)和H2O(g)的能量总和
B.反应CH4(g)+2O2(g)=CO2(g)+2H2O(1) △H=-800kJmol-1
C.若破坏1molO2(g)中的化学键需吸收热量493kJ,则破坏1molC-H键需吸收热量415kJ
D.在反应CH4(g)+2O2(g)═CO2(g)+2H2O(g)中,放出热量400kJ,有1molO-H键生成
【答案】C
【解析】
从图中可以提取以下信息:1molCH4(g)+2molO2(g)断裂所有共价键,需要吸收2646kJ的热量;1molC(g)+4molH(g)+4molO(g)结合成1molCO2(g)+2molH2O(g),能放出3446kJ的热量。
A.从图中看出,CH4(g)和O2的总能量大于CO2(g)和H2O(g)的能量总和,但CH4(g)的能量不一定大于CO2(g)和H2O(g)的能量总和,A不正确;
B.图中信息告诉我们,反应CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-800kJmol-1,B不正确;
C.若破坏1molO2(g)中的化学键需吸收热量493kJ,则破坏1molC-H键需吸收热量![]() kJ=415kJ,C正确;
kJ=415kJ,C正确;
D.在反应CH4(g)+2O2(g)═CO2(g)+2H2O(g)中,放出热量400kJ,则生成1molH2O,有2molO-H键生成,D不正确;
故选C。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】某化学兴趣小组探究铝与稀盐酸反应速率的影响因素,用等质量的铝和等体积、等浓度的足量稀盐酸反应,得到的3组实验数据如下:
实验编号 | 铝的形状 | 反应温度/℃ | 收集100mLH2所需的时间 |
① | 铝粉 | 20 | 21 |
② | 铝片 | 20 | 82 |
③ | 铝片 | 30 | 35 |
回答下列问题:
(1)写出铝与稀盐酸反应的化学方程式______________________。
(2)探究温度对该反应速率影响的对比实验是③和_______ (填实验编号),得出的实验结论是________。
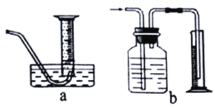
(3)若将该实验中“收集100mL H2所需时间改为“测量相同时间内生成H2的体积”,可选用的排水量气装置为下图中的______________(填装置代号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右下表为元素周期表的一部分,其中X、Y、Z、W为短周期元素,W元素的核电荷数为X元素的2倍。下列说法正确的是( )

A. X、W、Z元素的原子半径及它们的气态氢化物的热稳定性均依次递增
B. Y、Z、W元素在自然界中均不能以游离态存在,它们的最高价氧化物的水化物的酸性依次递增
C. YX2晶体熔化、液态WX3气化均需克服分子间作用力
D. 根据元素周期律,可以推测T元素的单质具有半导体特性,T2X3具有氧化性和还原性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W在元素周期表中的相对位置如下图所示,其中W原子的质子数是其最外层电子数的三倍,下列说法不正确的是( )
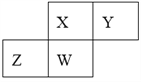
A. 原子半径:W>Z>Y>X
B. 最高价氧化物对应水化物的酸性:X>W>Z
C. 最简单气态氢化物的热稳定性:Y>X>W>Z
D. 元素X、Z、W的最高化合价分别与其主族序数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列实验装置进行相应实验,能达到实验目的的是 ( )
A.  用图所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体
用图所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体
B.  用图所示装置除去Cl2中含有的少量HCl
用图所示装置除去Cl2中含有的少量HCl
C.  用图所示装置分离CCl4萃取碘水后已分层的有机层和水层
用图所示装置分离CCl4萃取碘水后已分层的有机层和水层
D.  用图所示装置制取少量纯净的CO2气体
用图所示装置制取少量纯净的CO2气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列五个转化,其中不能通过一步反应实现的是 ( )
①SiO2![]() Na2SiO3②CuSO4
Na2SiO3②CuSO4![]() CuCl2③SiO2
CuCl2③SiO2![]() H2SiO3④CuO
H2SiO3④CuO![]() Cu(OH)2
Cu(OH)2
⑤Na2O2![]() Na2SO4
Na2SO4
A.①②B.③④
C.②③④D.②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机化合物的同分异构体数目判断正确的是( )
A. 分子式为C5H10,含碳碳双键的烯烃为6种
B. 分子式为C8H10,含苯环的有机物为3种
C. 分子式为C5H12O,且能与Na反应的有机物为8种
D. 分子式为C5H10O2,且能与Na2CO3反应的有机物为10种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知 会发生反应变为
会发生反应变为![]() (R与R′可以为烃基,也可以为H),则写出下列物质与NaOH水溶液充分反应后所得有机物的结构简式。
(R与R′可以为烃基,也可以为H),则写出下列物质与NaOH水溶液充分反应后所得有机物的结构简式。
(1)CH3Cl:___________
(2)CH2Cl2:______________
(3)CHCl3:_________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人们常常利用化学反应中的能量变化为人类服务。
⑴化学反应中的能量变化,主要表现为热量的变化。
①下列反应中,既属于氧化还原反应,又属于放热反应的是_________。
A.Ba(OH)2·8H2O与NH4Cl混合搅拌 B.铝与氧化铁在高温下反应 C.铝与盐酸反应 D.NaOH与稀硫酸反应
②氢气在氯气中燃烧产生苍白色火焰。在反应过程中,破坏1 mol 氢气中的化学键消耗的能量为Q1kJ,破坏1 mol 氯气中的化学键消耗的能量为Q2kJ,形成1 mol 氯化氢中的化学键释放的能量为Q3kJ。下列关系式中正确的是_________。
A.Q1+Q2>Q3B.Q1+Q2<2Q3C. Q1+Q2<Q3D.Q1+Q2>2Q3
⑵电能是现代社会应用最广泛的能源之一。如下图所示的原电池装置中:

①负极材料是_______,正极上能够观察到的现象是_______________________,
②正极的电极反应式是______________。
③原电池工作一段时间后,若消耗锌6.5 g,则放出气体________L(标况下)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com