
【题目】四氯化钛(TiCl4)是制取航天工业材料——钛合金的重要原料。实验室以TiO2和CCl4为原料树取液态TiCl4的装置如图所示(部分夹持装置省略)。
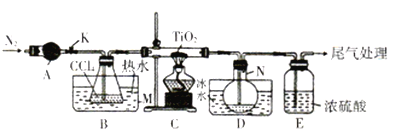
已知:有关物质的性质如下表:
物质 | 熔点/℃ | 沸点/℃ | 其他 |
CCl4 | -23 | 76 | 与TiCl4互溶 |
TiCl4 | -25 | 136 | 遇潮湿空气产生白雾,在550 ℃时能被氧气氧化 |
请回答下列问题:
(1)仪器A的名称是________,仪器A中盛装的试剂是___________。
(2)CCl4的电子式为__________。
(3)装置C处硬质玻管中反应的化学方程式为__________________。
(4)TiCl4遇潮湿空气会产生TiO2,反应的化学方程式为________________。
(5)仪器N中收集到的物质主要有___________(写化学式),从产物中分离出TiCl4的实验方法是_____________。
(6)TiCl4还可由TiO2、焦炭和氯气在加热条件下制得,生成体积比为2∶1的CO和CO2混合气体,该反应中氧化剂与还原剂的物质的量之比为________。请设计实验方案验证产物气体中有CO:_______________。
【答案】 球形干燥管或干燥管 碱石灰或生石灰、氢氧化钠,氯化钙等 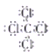 TiO2+CCl4
TiO2+CCl4![]() TiCl4+CO2 TiCl4+2H2O=TiO2+4HCl CCl4、TiCl4 蒸馏 4:3 将产物气体依序通入足量的NaOH溶液→干燥剂→灼热的CuO→澄清石灰水,若最终澄清石灰水变浑浊,灼热的CuO固体由黑色变红色,则产物中有CO
TiCl4+CO2 TiCl4+2H2O=TiO2+4HCl CCl4、TiCl4 蒸馏 4:3 将产物气体依序通入足量的NaOH溶液→干燥剂→灼热的CuO→澄清石灰水,若最终澄清石灰水变浑浊,灼热的CuO固体由黑色变红色,则产物中有CO
【解析】试题分析:氮气把CCl4蒸汽赶入C中与TiO2反应生成TiCl4和CO2;根据TiCl4的沸点是136℃,用冰水冷凝收集TiCl4,TiCl4遇水蒸气易水解,所以实验开始和结束都要用干燥装置;
解析:(1)仪器A的名称是球形干燥管,仪器A的目的是干燥氮气,A中盛装的试剂是碱石灰。
(2)CCl4是共价化合物,原子最外层都满足8电子结构,CCl4的电子式为: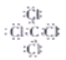 。
。
(3)装置C处CCl4蒸汽在加热条件下与TiO2反应生成TiCl4和CO2,反应的化学方程式为:TiO2+CCl4![]() TiCl4+CO2。
TiCl4+CO2。
(4)TiCl4遇潮湿空气会发生水解反应生成TiO2和氯化氢,反应的化学方程式为:TiCl4+2H2O=TiO2+4HCl。
(5)CCl4、TiCl4的沸点都大于0℃,仪器N中收集到的物质主要有CCl4、TiCl4 ,根据沸点不同,用蒸馏法从CCl4、TiCl4中分离出TiCl4。
(6)TiCl4还可由TiO2、焦炭和氯气在加热条件下制得,生成体积比为2∶1的CO和CO2混合气体,反应的方程式为2TiO2+3C+4Cl2=2TiCl4+2CO+CO2,反应中氯气是氧化剂,碳是还原剂,氧化剂与还原剂的物质的量之比为4∶3;将产物气体依序通入足量的NaOH溶液→干燥剂→灼热的CuO→澄清石灰水,若最终澄清石灰水变浑浊,灼热的CuO固体由黑色变红色,则产物中有CO。


科目:高中化学 来源: 题型:
【题目】能在有机物的分子中引入羟基官能团的反应类型有:(a)酯化反应,(b)取代反应,(c)氧化反应,(d)加成反应,(e)水解反应。其中正确的组合有
A. (a)(b)(c) B. (d)(e) C. (b)(d)(e) D. (b)(c)(d)(e)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(2015·天津理综,3,6分)下列说法不正确的是( )
A.Na与H2O的反应是熵增的放热反应,该反应能自发进行
B.饱和Na2SO4溶液或浓硝酸均可使蛋白质溶液产生沉淀,但原理不同
C.FeCl3和MnO2均可加快H2O2分解,同等条件下二者对H2O2分解速率的改变相同
D.Mg(OH)2固体在溶液中存在平衡:Mg(OH)2(s) ![]() Mg2+(aq)+2OH-(aq),该固体可溶于NH4Cl溶液
Mg2+(aq)+2OH-(aq),该固体可溶于NH4Cl溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物M(C25H44O8)是一种新型治疗高血压病的药物,工业上用淀粉、烃A为基本原料合成M的路线如下图所示。
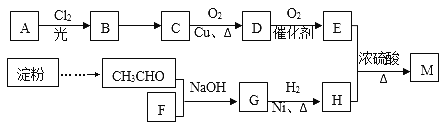 已知:
已知:
I.烃A在质谱图中的最大质荷比为72,B分子中核磁共振氢谱有2个峰且面积比为9:2,35%-40%的F的水溶液被称为福尔马林。
II.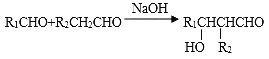
(1)A的名称为__________(系统命名法),B的结构简式为_______________,F的分子式为_____________;
(2)B→C的反应条件是______________,G的官能团名称是_____________;
(3)D与银氨溶液反应的方程式_____________________;
(4)E与H反应生成M的方程式___________________;
(5)E有多种同分异构体,其中能发生银镜反应且属于酯类的同分异构体共有____________种,其中核磁共振氢谱有2个峰的物质结构简式为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某Na2CO3、NaAlO2的混合溶液中逐滴加入1 mol/L的盐酸,测得溶液中CO32-、HCO3-、AlO2-、Al3+的物质的量与加入盐酸溶液的体积变化关系如图所示,则下列说法正确的是( )

A.a曲线表示的离子方程式为AlO2-+H++H2O==Al(OH)3↓
B.原混合溶液中的CO32-与AlO2-的物质的量之比为1∶2
C.V1∶V2=l∶5
D.M点时生成的CO2为0.05 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有些中国古文或谚语包含了丰富的化学知识,下列解释不合理的是
选项 | 古文或谚语 | 化学解释 |
A | 粉身碎骨浑不怕,要留清白在人间 | 发生了化学变化 |
B | 以曾青涂铁,铁赤色如铜 | 化合反应 |
C | 煮豆燃豆箕 | 化学能转化为热能 |
D | 雷雨肥庄稼 | 自然固氮 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.铬单质硬度大,耐腐蚀,是重要的合金材料。
(1)基态铬原子的价电子轨道表示式为________________;CrO2Cl2常温下为深红色液体,能与CCl4互溶,据此判断CrO2Cl2的晶体类型属于_________________。
(2)配合物CrCl3·6H2O的配位数为6,它有三种不同组成、不同颜色的固体,其中一种为浅绿色固体,该固体与足量硝酸银溶液反应时,0.5mol固体可生成1mol氯化银沉淀,则这种浅绿色固体的配体个数比(Cl-:H2O)为_____________。
II.砷化镓为第三代半导体材料,晶胞结构如图所示:

(3)砷化镓可由(CH3)3Ga和AsH3在700℃下反应制得,反应的化学方程式为__________。
(4)AsH3分子的立体构型为__________,其中As原子的杂化方式是______。1个(CH3)3Ga分子中含有_________个σ键,砷的第一电离能_______(填“>”或“<”)镓的第一电离能。
(5)砷化镓晶休中砷和镓的最近原子核间距为a nm,砷化镓的摩尔质量为bg·mol-1,阿伏加德罗常数值为NA,则砷化镓晶体的密度表达式是_____________g·cm-3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T℃时在2L密闭容器中使X(g)与Y(g)发生反应生成Z(g),反应过程中X、Y、Z的物质的量变化如图1所示;若保持其他条件不变,温度分别为T1和T2,Y的百分含量与时间的关系如图2所示。下列分析不正确的是( )

A.容器中发生的反应可表示为:3X(g)+Y(g)2Z(g)
B. 0~3min内,v(X)=0.1 mol/(Lmin)
C.若改变条件,使反应进程如图3所示,则改变的条件可能是增大压强
D.达平衡后,升高温度,v正、v逆都增大,且再次平衡前v正>v逆
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于金属铬的叙述中不正确的是( )
A. 铬元素在周期表中处于第四周期VIB族
B. 铬原子的外围电子层排布为3d44s2
C. 铬原子中,质子数为24
D. 铬元素位于元素周期表的d区,是过渡元素
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com