
·ÖĪö µČĪļÖŹµÄĮæµÄHAŗĶNaOHĒ”ŗĆ·“Ӧɜ³ÉNaA£¬ŅņĪŖc£ØNa+£©£¾c£ØA-£©£¬øł¾ŻµēŗÉŹŲŗćÖŖc£ØH+£©£¼c£ØOH-£©£¬ČÜŅŗ³Ź¼īŠŌ£¬
£Ø1£©øĆČÜŅŗÖŠA-Ė®½āµ«³Ģ¶Č½ĻŠ”£»
£Ø2£©ČĪŗĪµē½āÖŹČÜŅŗÖŠ¶¼“ęŌŚµēŗÉŹŲŗć£¬øł¾ŻĪļĮĻŹŲŗć¼ĘĖćc£ØHA£©+c£ØA-£©£»
£Ø3£©Ėį»ņ¼īŅÖÖĘĖ®µēĄė£¬ŗ¬ÓŠČõĄė×ÓµÄŃĪ“Ł½ųĖ®µēĄė£»
£Ø4£©25”ꏱ£¬Čē¹ūČ”0.2mol•L-1 HAČÜŅŗÓė0.1mol•L-1 NaOHČÜŅŗµČĢå»ż»ģŗĻ£¬ČÜŅŗÖŠČÜÖŹĪŖµČĪļÖŹµÄĮæÅØ¶ČµÄNaAŗĶHA£¬²āµĆ»ģŗĻČÜŅŗµÄpH£¼7£¬ČÜŅŗ³ŹĖįŠŌ£¬ĖµĆ÷ĖįµÄµēĄė³Ģ¶Č“óÓŚĖįøłĄė×ÓĖ®½ā³Ģ¶Č£»
£Ø5£©A£®Čō·“Ó¦ŗóČÜŅŗ³ŹÖŠŠŌ£¬ŌņČÜŅŗÖŠ“ęŌŚc£ØH+£©=c£ØOH-£©=10-7 mol•L-1£»
B£®ČōV1=V2£¬ŅŖøł¾ŻĖį¼īÅضČĻą¶Ō“óŠ”Č·¶ØČÜŅŗĖį¼īŠŌ£»
C£®Čō·“Ó¦ŗóČÜŅŗ³ŹĖįŠŌ£¬ŌņČÜŅŗæÉÄÜŹĒĖįŗĶŃĪČÜŅŗ£»
D£®Čē¹ūČÜŅŗ³Ź¼īŠŌ£¬ŌņČÜŅŗæÉÄÜŹĒ¼īŗĶŃĪČÜŅŗ£¬Ņ²æÉÄÜÖ»ŹĒŃĪČÜŅŗ£®
½ā“š ½ā£ŗµČĪļÖŹµÄĮæµÄHAŗĶNaOHĒ”ŗĆ·“Ӧɜ³ÉNaA£¬ŅņĪŖc£ØNa+£©£¾c£ØA-£©£¬øł¾ŻµēŗÉŹŲŗćÖŖc£ØH+£©£¼c£ØOH-£©£¬ČÜŅŗ³Ź¼īŠŌ£¬
£Ø1£©øĆČÜŅŗÖŠA-Ė®½āµ«³Ģ¶Č½ĻŠ”£¬ĖłŅŌ“ęŌŚc£ØHA£©£¼c£ØA-£©£¬¹Ź“š°øĪŖ£ŗ£¼£»
£Ø2£©ČĪŗĪµē½āÖŹČÜŅŗÖŠ¶¼“ęŌŚµēŗÉŹŲŗć£¬¶žÕß»ģŗĻŹ±ČÜŅŗĢå»żŌö“óŅ»±¶£¬ČÜŅŗÅØ¶Č½µĪŖŌĄ“µÄŅ»°ė£¬øł¾ŻĪļĮĻŹŲŗćµĆc£ØHA£©+c£ØA-£©=0.1 mol•L-1£¬¹Ź“š°øĪŖ£ŗ0.1 mol•L-1£»
£Ø3£©Ėį»ņ¼īŅÖÖĘĖ®µēĄė£¬ŗ¬ÓŠČõĄė×ÓµÄŃĪ“Ł½ųĖ®µēĄė£¬øĆČÜŅŗÖŠŗ¬ÓŠČõĄė×ÓµÄŃĪ£¬ĖłŅŌ“Ł½ųĖ®µēĄė£¬HAŅÖÖĘĖ®µēĄė£¬ŌņŗĻČÜŅŗÖŠÓÉĖ®µēĄė³öµÄc£ØOH-£©£¾0.2mol•L-1 HAČÜŅŗÖŠÓÉĖ®µēĄė³öµÄc£ØH+£©£¬¹Ź“š°øĪŖ£ŗ£¾£»
£Ø4£©25”ꏱ£¬Čē¹ūČ”0.2mol•L-1 HAČÜŅŗÓė0.1mol•L-1 NaOHČÜŅŗµČĢå»ż»ģŗĻ£¬ČÜŅŗÖŠČÜÖŹĪŖµČĪļÖŹµÄĮæÅØ¶ČµÄNaAŗĶHA£¬²āµĆ»ģŗĻČÜŅŗµÄpH£¼7£¬ČÜŅŗ³ŹĖįŠŌ£¬ĖµĆ÷ĖįµÄµēĄė³Ģ¶Č“óÓŚĖįøłĄė×ÓĖ®½ā³Ģ¶Č£¬
¹Ź“š°øĪŖ£ŗ£¾£»
£Ø5£©A£®Čō»ģŗĻČÜŅŗ³ŹÖŠŠŌ£¬ŌņČÜŅŗMÖŠc£ØH+£©=c£ØOH-£©=2”Į10-7 mol•L-1£¬ĖłŅŌČÜŅŗMÖŠc£ØH+£©+c£ØOH-£©=2”Į10-7 mol•L-1£¬¹ŹÕżČ·£»
B£®Čē¹ū¶žÕßĢå»żĻąµČ£¬Čē¹ūĖįŹĒĒæĖį£¬Ōņ»ģŗĻČÜŅŗ³ŹÖŠŠŌ£¬Čē¹ūĖįŹĒČõĖį£¬Ōņ»ģŗĻČÜŅŗ³ŹĖįŠŌ£¬¹Ź“ķĪó£»
C£®Čē¹ūČÜŅŗ³ŹĖįŠŌ£¬ŌņČÜŅŗŹĒĖįŗĶŃĪČÜŅŗ£¬ĖįŹĒČõĖį£¬ĖįÅØ¶Č“óÓŚĒāŃõ»ÆÄĘÅØ¶Č£¬ĖłŅŌV1²»Ņ»¶Ø“óÓŚV2£¬¹Ź“ķĪó£»
D£®Čē¹ūČÜŅŗ³Ź¼īŠŌ£¬ŌņČÜŅŗæÉÄÜŹĒ¼īŗĶŃĪČÜŅŗ£¬Ņ²æÉÄÜÖ»ŹĒŃĪČÜŅŗ£¬ŌņV1Ņ»¶ØŠ”ÓŚV2£¬¹ŹÕżČ·£»
¹ŹŃ”AD£®
µćĘĄ ±¾Ģāæ¼²éĖį¼ī»ģŗĻČÜŅŗ¶ØŠŌÅŠ¶Ļ£¬ĪŖøßĘµæ¼µć£¬Éę¼°ŃĪĄąĖ®½ā”¢Čõµē½āÖŹµÄµēĄė£¬Ć÷Č·ČÜŅŗÖŠČÜÖŹ¼°ĘäŠŌÖŹŹĒ½ā±¾Ģā¹Ų¼ü£¬ÄѵćŹĒ£Ø5£©ĢāĖį¼īĢå»żÅŠ¶Ļ£¬²ÉÓĆÄęĻņĖ¼Ī¬·½·Ø·ÖĪö½ā“š£¬ĢāÄæÄѶČÖŠµČ£®


 ×ß½ųĪÄŃŌĪÄĻµĮŠ“š°ø
×ß½ųĪÄŃŌĪÄĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 Ņ»¶ØĪĀ¶ČĻĀ£¬ČżÖÖĢ¼ĖįŃĪMCO3£ØM£ŗMg2+”¢Ca2+”¢Mn2+£©µÄ³ĮµķČܽāĘ½ŗāĒśĻßČēĶ¼ĖłŹ¾£®ŅŃÖŖ£ŗpM=-lgc£ØM£©£¬pc£ØCO32-£©=-lgc£ØCO32-£©£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒBD£®
Ņ»¶ØĪĀ¶ČĻĀ£¬ČżÖÖĢ¼ĖįŃĪMCO3£ØM£ŗMg2+”¢Ca2+”¢Mn2+£©µÄ³ĮµķČܽāĘ½ŗāĒśĻßČēĶ¼ĖłŹ¾£®ŅŃÖŖ£ŗpM=-lgc£ØM£©£¬pc£ØCO32-£©=-lgc£ØCO32-£©£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒBD£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĻņĘÆ°×·Ū×ĒŅŗÖŠĶØČė¹żĮæµÄCO2 | |
| B£® | Ļņ“ųÓŠŃõ»ÆĤµÄĀĮʬ֊¼ÓČėŃĪĖį | |
| C£® | Ļņŗ¬ÓŠ1molCa£ØHCO3£©2µÄČÜŅŗÖŠ¼ÓČė1molNa2O2 | |
| D£® | Ļņŗ¬ÓŠ1molKAl£ØSO4£©2µÄČÜŅŗÖŠ¼ÓČė2molBa£ØOH£©2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | c£ØNH${\;}_{4}^{+}$£©£ŗc£ØNH3•H2O£©±ČÖµŌö“ó | B£® | ĖłÓŠĄė×ÓÅØ¶Č¾ł¼õŠ” | ||
| C£® | c£ØOH-£©£ŗc£ØNH3•H2O£©±ČÖµ¼õŠ” | D£® | µēĄė³£ŹżŌö“ó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ³ĪĒåĶøĆ÷µÄČÜŅŗÖŠ£ŗMnO${\;}_{4}^{-}$”¢SO${\;}_{4}^{2-}$”¢K+”¢Fe3+ | |
| B£® | c£ØH+£©=1”Į10-13mol/LµÄČÜŅŗÖŠ£ŗMg2+”¢Cu2+”¢SO42-”¢NO3- | |
| C£® | 3%H2O2ČÜŅŗÖŠ£ŗFe2+”¢H+”¢SO${\;}_{4}^{2-}$”¢Cl- | |
| D£® | 0.1 mol•L-1µÄNa2SO3ČÜŅŗÖŠ£ŗK+”¢H+”¢SO${\;}_{4}^{2-}$”¢NO${\;}_{3}^{-}$ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ĶĘ²ā | ²Ł×÷ŗĶĻÖĻó | ½įĀŪ |
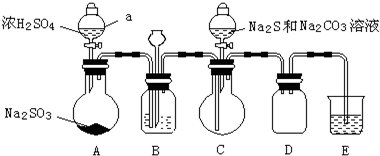
| ŌÓÖŹÖŠµÄÕżŃĪ³É·ÖæÉÄÜÓŠ£ŗ Na2S”¢Na2CO3 Na2SO4 ¼°Na2SO3 | ¢ŁČ”Wg²śĘ·Åä³ÉĻ”ČÜŅŗ£» ¢ŚĻņČÜŅŗÖŠµĪ¼Ó¹żĮæBaCl2ČÜŅŗ£¬ÓŠ°×É«³ĮµķÉś³É£¬¹żĀĖ£¬µĆ³ĮµķŗĶĀĖŅŗ£» ¢ŪĻņ³ĮµķÖŠ¼ÓČė¹żĮæŃĪĖį£¬³ĮµķĶźČ«Čܽā£¬²¢ÓŠ“Ģ¼¤ŠŌĘųĪ¶µÄĘųĢå²śÉś£® | ²śĘ·ŌÓÖŹÖŠ£ŗ Ņ»¶Øŗ¬ÓŠNa2SO3£¬ æÉÄÜŗ¬ÓŠNa2CO3£¬ Ņ»¶Ø²»ŗ¬ÓŠNa2S”¢Na2SO4£® |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

| A£® | ±“ŵõ„·Ö×ÓÖŠÓŠČżÖÖŗ¬Ńõ¹ŁÄÜĶÅ | |
| B£® | ÓĆFeCl3 ČÜŅŗ²»ÄÜĒų±šŅŅõ£Ė®ŃīĖįŗĶ¶ŌŅŅõ£°±»ł·Ó | |
| C£® | ŅŅõ£Ė®ŃīĖįŗĶ¶ŌŅŅõ£°±»ł·Ó¾łÄÜÓėNaHCO3 ČÜŅŗ·“Ó¦ | |
| D£® | 1mol±“ŵõ„Óė×ćĮæNaOH ČÜŅŗ¹²ČČ×ī¶ąæÉĻūŗÄ5molNaOHÄĘ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com