
| A. | N2和Cl2两种分子中,每个原子的最外层都具有8电子稳定结构 | |
| B. | 某物质在熔融态能导电,则该物质中一定含有离子键 | |
| C. | 干冰是分子晶体,其溶于水生成碳酸的过程只需克服分子间作用力 | |
| D. | MgF2晶体中的化学键是共价键 |
分析 A.根据原子中的最外层电子和形成的共用电子对判断;
B.金属单质在熔融状态时能导电;
C.发生化学变化是克服化学键;
D.活泼金属与活泼非金属原子间形成离子键.
解答 解:A.N2中N原子中的最外层电子为5,形成3个共用电子对,所以每个原子的最外层都具有8电子稳定结构,Cl2中Cl原子中的最外层电子为7,形成1个共用电子对,所以每个原子的最外层都具有8电子稳定结构,故A正确;
B.金属单质在熔融状态时能导电,金属中含有金属键,所以某物质在熔融态能导电,则该物质中不一定含有离子键,故B错误;
C.干冰是分子晶体,其溶于水生成碳酸的过程克服分子间作用力,由于发生化学变化,还克服化学键,故C错误;
D.MgF2晶体中的化学键是离子键,故D错误.
故选A.
点评 本题考查了分子间作用力、晶体类型的判断、化学键等,题目难度不大,侧重于基础知识的考查,注意把握8电子稳定结构的判断.


科目:高中化学 来源: 题型:解答题
 过渡元素铁可形成多种配合物,如:[Fe(CN)6]4-、Fe(OCN)64-等.
过渡元素铁可形成多种配合物,如:[Fe(CN)6]4-、Fe(OCN)64-等. Mg2FeH6+Mg.
Mg2FeH6+Mg.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4 L氯气与过量的氢氧化钠溶液完全反应转移的电子数为2 NA | |
| B. | 18gD216O中含有的中子数为9 NA | |
| C. | 标准状况下,22.4L H2O中含有的共用电子对数为2NA | |
| D. | 常温常压下,11.2L的NO2和CO2混合气体含有氧原子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 60g二氧化硅中含有SiO2分子的数目为NA | |
| B. | 标准状况下,5.6 LCO2与足量Na2O2反应转移的电子数为0.5NA | |
| C. | Zn与足量的浓硫酸反应生成标况下22.4L气体时,转移2NA电子 | |
| D. | 1L 0.1mol/L的Na2CO3溶液中含有的阴离子总数小于0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可利用农作物秸秆制取燃料乙醇 | |
| B. | 可将回收的地沟油加工制成生物柴油 | |
| C. | 向燃煤中加入一些生石灰后可减少温室气体的排放 | |
| D. | 废旧钢材焊接前,可依次用饱和Na2CO3、NH4Cl溶液处理焊点 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,11.2L NH3所含的原子数为2NA | |
| B. | 常温常压下,80g SO3含有的氧原子数为3NA | |
| C. | 标准状况下,22.4L H2中所含原子数为NA | |
| D. | 1 mol HCl气体中的粒子数与0.5 mol/L盐酸中溶质粒子数相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
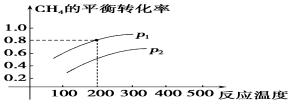
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com