
 ,与N3-互为等电子体的分子为N2O(写一种);
,与N3-互为等电子体的分子为N2O(写一种);分析 (1)N原子2s轨道容纳2个电子,且自旋方向相反,2p能级3个轨道各容纳1个电子,且自旋方向相同;原子个数相等、价电子数相等的微粒互为等电子体;
(2)HF分子之间有氢键,沸点较高;
(3)根据相似相溶的原理,非极分子易溶于非极性溶剂;
(4)配合物也叫络合物,为一类具有特征化学结构的化合物,由中心原子或离子(统称中心原子)和围绕它的称为配位体(简称配体)的分子或离子,完全或部分由配位键结合形成,配位体:提供孤电子对的分子或离子;配位原子:配体中,提供电子对的原子;中心原子、金属原子:一般指接受电子对的原子;配位数:中心原子周围的配位原子个数;
解答 解:(1)N原子2s轨道容纳2个电子,且自旋方向相反,2p能级3个轨道各容纳1个电子,且自旋方向相同,故基态氮原子的L层电子排布图为: ,
,
原子个数相等、价电子数相等的微粒互为等电子体,N3-中原子个数是3、价电子数是15,所以其等电子体有N2O、CO2、CS2;故答案为: ; N2O;
; N2O;
(2))HF分子之间有氢键,沸点较高,所以首先液化的物质是HF,故答案为:HF;
(3)根据相似相溶的原理,非极分子易溶于非极性溶剂,能与非极性溶剂CCl4、CS2等互溶,说明CrO2Cl2 是非极性分子,故答案为:非极性;
(4)[TiCl(H2O)5]Cl2•H2O中,中心离子是Ti3+,提供空轨道接受孤对电子,H2O、Cl-提供孤电子对为配体,2个氨气分子,所以配位数为6,外界是Cl-,内界是:[TiCl(H2O)5]2+,
故答案为:H2O、Cl-;6.
点评 本题考查配合物的成键情况,注意配体、中心离子、外界离子以及配位数的判断,把握相关概念,相似相溶判断分子的极性,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | NaCl固体(CaCl2):溶解,加Na2CO3溶液、过滤后加适量盐酸,最后蒸发结晶 | |
| B. | KCl固体(MnO2):溶解、过滤、蒸发结晶 | |
| C. | NaCl溶液(I2):加酒精,萃取、分液 | |
| D. | KNO3溶液(I2):加四氯化碳,萃取、分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分液、萃取、蒸馏 | B. | 分液、蒸馏、萃取 | C. | 萃取、蒸馏、分液 | D. | 蒸馏、萃取、分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 8种 | B. | 10种 | C. | 11种 | D. | 13种 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
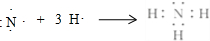 ;
;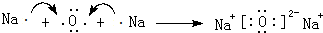 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蒸发结晶操作时,当有大量晶体析出时停止加热,用余热蒸干 | |
| B. | 蒸馏操作时,应使温度计水银球插入液态混合物中 | |
| C. | 分液操作时,分液漏斗中下层液体从下口流出,上层液体从上口倒出 | |
| D. | 萃取操作时,萃取剂要和原溶剂互不相溶,且不能与溶质和溶剂反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com