
【题目】PTT是近几年来迅速发展起来的新型热塑性聚酯材料,具有优异性能,能作为工程塑料、纺织纤维和地毯等材料而得到广泛应用.其合成路线可设计为: 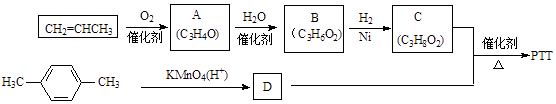
其中A、B、C均为链状化合物,A能发生银镜反应,B中不含甲基.请回答下列问题:
(1)A、B的结构简式分别为、
(2)写出一种满足下列条件的A的同系物的结构简式
①分子式为C4H6O ②含有1个﹣CH3
(3)1mol C可与足量钠反应生成L H2(标准状况).
(4)由物质C与D反应生成PTT的化学方程式为 , 反应类型为 .
【答案】
(1)CH2=CHCHO;HOCH2CH2CHO
(2)![]()
(3)22.4
(4)![]() ;
;![]()
【解析】解:A、B、C均为链状化合物,A能发生银镜反应,则A是醛,A的不饱和度= ![]() =2,则A的不饱和度为2,A的结构简式为CH2=CHCHO,A发生加成反应生成B,B中不含甲基,则B结构简式为HOCH2CH2CHO,B发生加成反应生成C,C结构简式为HOCH2CH2CH2OH,对二甲苯被酸性高锰酸钾溶液氧化生成对二苯甲酸,则D结构简式为
=2,则A的不饱和度为2,A的结构简式为CH2=CHCHO,A发生加成反应生成B,B中不含甲基,则B结构简式为HOCH2CH2CHO,B发生加成反应生成C,C结构简式为HOCH2CH2CH2OH,对二甲苯被酸性高锰酸钾溶液氧化生成对二苯甲酸,则D结构简式为 ![]() ,CD发生缩聚反应生成PTT,(1)通过以上分析知,A结构简式为CH2=CHCHO,B结构简式为HOCH2CH2CHO,所以答案是:CH2=CHCHO;HOCH2CH2CHO;(2)分子式为C4H6O,含有1个﹣CH3的醛类物质的结构可能是
,CD发生缩聚反应生成PTT,(1)通过以上分析知,A结构简式为CH2=CHCHO,B结构简式为HOCH2CH2CHO,所以答案是:CH2=CHCHO;HOCH2CH2CHO;(2)分子式为C4H6O,含有1个﹣CH3的醛类物质的结构可能是 ![]() ,所以答案是:
,所以答案是: ![]() ;(3)中有2个羟基,都可以和钠反应,所以1摩尔C与足量的钠反应生成1摩尔氢气,体积为22.4升,所以答案是:22.4;(4)D为对苯二甲酸,和C可以发生缩聚反应,方程式为:
;(3)中有2个羟基,都可以和钠反应,所以1摩尔C与足量的钠反应生成1摩尔氢气,体积为22.4升,所以答案是:22.4;(4)D为对苯二甲酸,和C可以发生缩聚反应,方程式为:![]()
, 反应类型是缩聚反应,
所以答案是: ![]() ;缩聚反应.
;缩聚反应.


 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:
【题目】下列关于烯烃、炔烃的叙述中,正确的是
A. 某物质的名称为2-乙基-1-丁烯,它的结构简式为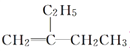
B. CH3—CH===CH—C≡C—CF3分子结构中6个碳原子可能都在一条直线上
C. 相同物质的量的乙炔与苯分别在足量的氧气中完全燃烧,消耗氧气的量相同
D. β—月桂烯的结构如图![]() 所示,该物质与等物质的量溴发生加成反应的产物(不考虑立体异构)理论上最多有5种
所示,该物质与等物质的量溴发生加成反应的产物(不考虑立体异构)理论上最多有5种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水中溶氧量(DO)是衡量水体自净能力的一个指标,通常用每升水中溶解氧分子的质量表示,单位mgL﹣1 . 我国《地表水环境质量标准》规定,生活饮用水源的DO不能低于5mgL﹣1 . 某化学小组同学设计了下列装置(夹持装置略),测定某河水的DO.
Ⅰ.测定原理:
碱性条件下,O2将Mn2+氧化为MnO(OH)2:①2Mn2++O2+4OH﹣═2MnO(OH)2↓
酸性条件下,MnO(OH)2将I﹣氧化为I2:②MnO(OH)2+I﹣+H+→Mn2++I2+H2O(未配平)
用Na2S2O3标准溶液滴定生成的I2;③2S2O32﹣+I2═S4O62﹣+2I﹣
Ⅱ.测定步骤:
a.安装装置,检验气密性,充N2排尽空气后,停止充N2 .
b.向烧瓶中加入200mL水样.
c.向烧瓶中依次迅速加入1mL MnSO4无氧溶液(过量)、2mL碱性KI无氧溶液(过量)开启搅拌器,至反应①完全.
d.搅拌并向烧瓶中加入2mL H2SO4无氧溶液,至反应②完全,溶液为中性或弱酸性.
e.从烧瓶中取出40.00mL溶液,以淀粉作指示剂,用0.01000molL﹣1 Na2S2O3溶液进行滴定,记录数据.f…
g.处理数据(忽略氧气从水样中的逸出量和加入试剂后水样体积的变化).
回答下列问题:
(1)配制以上无氧溶液时,除去所用溶剂水中氧的简单操作为 .
(2)在橡胶塞处加入水样及有关试剂应选择的仪器是 .
①滴定管 ②注射器 ③量筒
(3)搅拌的作用是 .
(4)配平反应②的方程式,其化学计量数依次为 .
(5)步骤f为 .
(6)步骤e中达到滴定终点的标志为 . 若某次滴定消耗Na2S2O3溶液4.50mL,水样的DO=mgL﹣1(保留一位小数).作为饮用水源,此次测得DO是否达标:(填“是”或“否”)
(7)步骤d中加入H2SO4溶液反应后,若溶液pH过低,滴定时会产生明显的误差,写出产生此误差的原因(用离子方程式表示,至少写出2个) .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E是原子序数依次增大的五种短周期元素.B、E同主族,且满足最高正化合价+最低负化合价=0;A与C、D与C之间都能形成原子个数比分别为2:1和1:1的两种化合物.试解答下列有关问题.
(1)在A2C2分子中含有的化学键是和 .
(2)C与D形成的化合物的电子式为 .
(3)实验室可用由B、C、D组成的化合物为反应物之一制取由A、C、D组成的化合物,反应的化学方程式为 .
(4)写出E单质与A、C、D形成的化合物的水溶液反应的离子方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SiO2在自然界中广泛存在,它是制备现代通讯材料(写该材料名称)的主要原料;以SiO2为原料,在工业上制备单质硅的化学方程式为;在常温下,SiO2可与一种酸发生反应,该反应的化学方程式为 . 该反应的重要应用是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】配制一定物质的量浓度的溶液是高中化学一个重要实验.实验室要配制1mol/L的稀硫酸溶液100mL,回答下列有关问题:
(1)配制时,必须用到下列仪器中的 . 
(2)配制时两次用到玻璃棒,两次的作用分别是和 .
(3)配制时,正确的操作顺序是(用字母表示,每个字母只能用一次);A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶
B.用一定规格的量筒准确量取所需浓硫酸的体积,缓缓注入水中,用玻璃棒慢慢搅动,使其充分溶解
C.将已冷却的溶液沿玻璃棒注入100mL的容量瓶中
D.将容量瓶盖紧,摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1~2cm处
(4)配制过程中出现以下情况,使所配溶液浓度偏低的有(填代号).①没有洗涤烧杯和玻璃棒.②如果加水超过了刻度线,取出水使液面恰好到刻度线.③容量瓶没有干燥.④定容时仰视刻度线.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无水MgBr2可用作催化剂.实验室采用镁屑与液溴为原料制备无水MgBr2 , 装置如图1,主要步骤如下:
步骤1 三颈瓶中装入10g镁屑和150mL无水乙醚;装置B中加入15mL液溴.
步骤2 缓慢通入干燥的氮气,直至溴完全导入三颈瓶中.
步骤3 反应完毕后恢复至常温,过滤,滤液转移至另一干燥的烧瓶中,冷却至0℃,析出晶体,再过滤得三乙醚溴化镁粗品.
步骤4 室温下用苯溶解粗品,冷却至0℃,析出晶体,过滤,洗涤得三乙醚合溴化镁,加热至160℃分解得无水MgBr2产品.
已知:①Mg与Br2反应剧烈放热;MgBr2具有强吸水性.
②MgBr2+3C2H5OC2H5MgBr23C2H5OC2H5
请回答:
(1)仪器A的名称是 . 实验中不能用干燥空气代替干燥N2 , 原因是 .
(2)如将装置B改为装置C(图2),可能会导致的后果是 .
(3)步骤3中,第一次过滤除去的物质是 .
(4)有关步骤4的说法,正确的是 .
A.可用95%的乙醇代替苯溶解粗品
B.洗涤晶体可选用0℃的苯
C.加热至160℃的主要目的是除去苯
D.该步骤的目的是除去乙醚和可能残留的溴
(5)为测定产品的纯度,可用EDTA(简写为Y)标准溶液滴定,反应的离子方程式:
Mg2++Y4﹣═MgY2﹣
①滴定前润洗滴定管的操作方法是 .
②测定时,先称取0.2500g无水MgBr2产品,溶解后,用0.0500molL﹣1的EDTA标准溶液滴定至终点,消耗EDTA标准溶液26.50mL,则测得无水MgBr2产品的纯度是(以质量分数表示).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于可逆反应A(g)+3B(g)2C(g),在不同条件下的化学反应速率如下,其中表示反应速率最快的是( )
A.V(A)=0.5 mol/(Lmin)
B.V(B)=1.2 mol/(Lmin)
C.V(C)=0.4 mol/(Lmin )
D.V(C)=1.1 mol/(Lmin)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】运用化学反应原理研究NH3的性质具有重要意义.请回答下列问题:
(1)利用对苯醌质子电池可检测氨气,其电池反应原理为2NH3+![]() (对苯醌)═N2H4+
(对苯醌)═N2H4+![]() (对苯酚),N2H4的结构式为 , 该电池正极的电极反应式为 .
(对苯酚),N2H4的结构式为 , 该电池正极的电极反应式为 .
(2)25℃时.将nmolL﹣1的氨水与0.1molL﹣1的盐酸等体积混合.
①当混合溶液中,c(NH4+)=c(Cl﹣)时.则溶液的pH= .
②当混合溶液中,c(NH4+)>c(Cl﹣)时.则反应的情况可能为 .
a.盐酸不足.氨水剩余 b.氨水与盐酸恰好完全反应 c.盐酸过量
(3)在0.5L恒容密闭容器中,一定量的N2与H2进行反应:N2(g)+3H2(g)2NH3(g)△H=bkJmol﹣1 , 其化学平衡常数K值和温度的关系如下:
温度/℃ | 200 | 300 | 400 |
K | 1.0 | 0.86 | 0.5 |
①写出该反应的化学平衡常数的表达式: , b(填“大于”、“小于”或“等于”)0.
②400℃时,测得某时刻氨气、氮气、氢气的物质的量分别为3mol、2mol、1mol时,此时刻该反应的v正(N2)(填“大于”、“小于”或“等于”)v逆(N2).
(4)已知:①4NH3(g)+3O2(g)═2N2(g)+6H2O(g)△H=﹣1266.8kJmol﹣1
②N2(g)+O2(g)═2NO(g)△H=180.5kJmol﹣1
写出氨高温催化氧化的热化学方程式 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com