
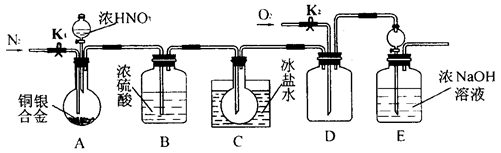
 N2O4,故在通风橱从冰盐水中取出烧瓶,观察到烧瓶中液体或固体迅速消失,瓶中充满红棕色气体,即可证明
N2O4,故在通风橱从冰盐水中取出烧瓶,观察到烧瓶中液体或固体迅速消失,瓶中充满红棕色气体,即可证明

科目:高中化学 来源:不详 题型:单选题
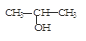 与NaOH的醇溶液共热制备CH3—CH═CH2
与NaOH的醇溶液共热制备CH3—CH═CH2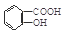 与适量NaHCO3溶液反应制备
与适量NaHCO3溶液反应制备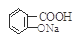
| A.只有① | B.只有①④ | C.只有①③④ | D.都不能 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
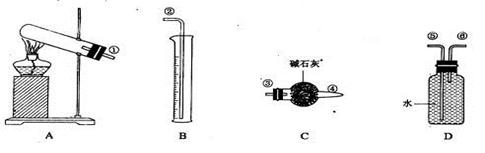 |
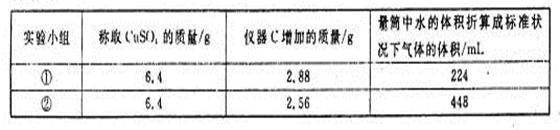
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.向Fe(NO3)2溶液中滴加稀硫酸 | B.将HC1通入NaAlO2溶液中 |
| C.加热溶有SO2的品红溶液 | D.向碳酸氢钠溶液中滴加氢氧化钠溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
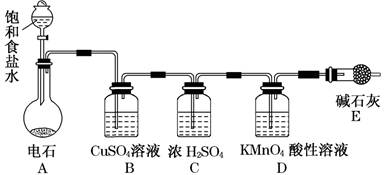
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用托盘天平称量25.20g氯化钠固体 |
| B.用250ml容量瓶配制150mL一定浓度的盐酸溶液 |
| C.用一束强光照射经过煮沸的三氯化铁溶液有光亮的通路,说明已生成氢氧化铁胶体 |
| D.过量的铁丝在氯气中点燃,可制取氯化亚铁 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
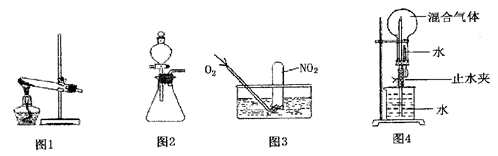
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
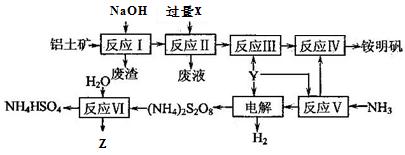
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com