
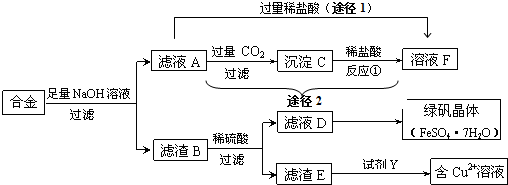
���� ������������ͭ�Ĺ�ҵ���ϼ������������ܽ⣬ֻ�������������Ʒ�Ӧ����ƫ�����ƺ���������������BΪ����ͭ���پ�ϡ���ᷴӦ���˵���ҺDΪ������������һ��ת�����̷�������EΪͭ���ʣ���ͭ��ϡ���ᷴӦ���ɺ�ͭ������Һ����ҺA��Ϊƫ��������Һ���ӹ������ᾭ;��1�����Ȼ�����Һ������ҺAͨ����������̼��;��2���ɳ���C������CΪ���������������ᷴӦ�����Ȼ�����Һ��
��1���������Ϸ������Ͻ���Ϻ���������ͭ������ֻ��������������������Һ��Ӧ��
��2���������ʵ����ʽ�Ͽ�ͼת����ϵ�����ò�Ʒ���н��
��3����Ϊ�̷������ǽᾧˮ�������Ҫ����ҺD�еõ��̷����壬����ֱ�����ɣ�������е�ʵ����������ǣ�����Ũ������ȴ�ᾧ�����ˡ���Ȼ���
��4������������E�ijɷ�Ӧ����ͭ��Ҫ�õ���Cu2+����Һ���Լ�Y�����ܺ�ͭ��Ӧ����Cu2+���ɣ�
��� �⣺������������ͭ�Ĺ�ҵ���ϼ������������ܽ⣬ֻ�������������Ʒ�Ӧ����ƫ�����ƺ���������������BΪ����ͭ���پ�ϡ���ᷴӦ���˵���ҺDΪ������������һ��ת�����̷�������EΪͭ���ʣ���ͭ��ϡ���ᷴӦ���ɺ�ͭ������Һ����ҺA��Ϊƫ��������Һ���ӹ������ᾭ;��1�����Ȼ�����Һ������ҺAͨ����������̼��;��2���ɳ���C������CΪ���������������ᷴӦ�����Ȼ�����Һ��
��1���������Ϸ������Ͻ���Ϻ���������ͭ������ֻ��������������������Һ��Ӧ�����ӷ���ʽ��2Al+2OH-+2H2O=2AlO2-+3H2����
�ʴ�Ϊ��2Al+2OH-+2H2O=2AlO2-+3H2����
��2��;��1������Ӧ��NaAlO2+4HCl=AlCl3+NaCl+2H2O�����������ᣬ�Ȼ������ʣ�;��2�Ƶõ��Ȼ�����Һ���ȸߣ�
�ʴ�Ϊ��2��;��2�Ƶõ��Ȼ�����Һ���ȸߣ�;��1��ȡ��AlCl3��Һ�л���NaCl���ʣ�
��3����Ϊ�̷������ǽᾧˮ�������Ҫ����ҺD�еõ��̷����壬����ֱ�����ɣ�������е�ʵ����������ǣ�����Ũ������ȴ�ᾧ�����ˡ���Ȼ���
�ʴ�Ϊ������Ũ����
��4������������E�ijɷ�Ӧ����ͭ��Ҫ�õ���Cu2+����Һ���Լ�Y�������ǿ�������ܺ�ͭ��Ӧ����Cu2+��Ũ������ͭҪ�ڼ��ȵ������²ŷ�Ӧ����ֻ��ϡ������ϣ���Ӧ����ʽΪ3Cu+8HNO3�T3Cu��NO3��2+2NO��+4H2O��
�ʴ�Ϊ��A��3Cu+8HNO3�T3Cu��NO3��2+2NO��+4H2O��
���� ������Ҫ�����˴ӹ�ҵ��������ȡ�����ע��ӿ�ͼת�����ҳ�������Ϣ�������йصĻ�ѧ��Ӧ���н�𣬲�����ѧ���ķ���������ʵ�������Ŀ��飬Ϊ�߿��������ͣ�ע�����ʵ��IJ���ԭ���Ͳ��裬�Ѷ��еȣ�


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �Ҵ��������������Ӧ | |
| B�� | �Ҵ���140��ʱ��ˮ�������� | |
| C�� | ����������ˮ�ⷴӦ | |
| D�� | �Ҵ���H2SO4���廯�ƹ�����ȡ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ���� | NaHSO3 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
| pH | 5.8 | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 11.3 |
| ��� | Ba��OH��2��Һ���/mL | �������/mL | ���ҺpH |
| 1 | 22.00 | 0 | 10 |
| 2 | 22.00 | 18.00 | 9 |
| 3 | 22.00 | 22.00 | 8 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
| ��g�� | ������L�� |
| 0.575 | 0.14 |
| 1.15 | 0.28 |
| 2.3 | 0.56 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ˮ�м���KHSO4��Һ | B�� | ��ˮ���ȵ�100�棬ʹpH=6 | ||
| C�� | ��ˮ�м���Na3PO4��Һ | D�� | ��ˮ�м���ZnSO4���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1molOH-�����к�������ĿΪ10NA | |
| B�� | 0.5L 0.2mol•L-1��NaCl��Һ�к��е�Na+����0.1NA | |
| C�� | ������ΪNA��CO��C2H4����������ԼΪ22.4 L������ԼΪ28 g | |
| D�� | 1 mol Na������O2��Ӧ������Na2O��Na2O2�Ļ�����ʧȥNA������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1molNa2O2�����к������Ӹ���Ϊ2NA | |
| B�� | 1molSiO2�к�Si-O����ĿΪ2NA | |
| C�� | ��״���£�22.4L��Ȳ�к��м���Ϊ2NA | |
| D�� | 1molNaHCO3��������������Ϊ2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������֮��1��1 | B�� | �ܶ�֮��4��11 | C�� | �ܶ�֮��11��16 | D�� | ���֮��11��16 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na2O2����ǿ�������ԣ������������� | |
| B�� | Na2CO3��Һ�ʼ��ԣ���������;߱�������� | |
| C�� | ������۵�ߡ�Ӳ�ȴ����������뵼����� | |
| D�� | ͭ�Ľ��������Ա����IJ���ں��������װ����ͭ���Լ����丯ʴ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com