
| A. | 硫酸(H2SO4) | B. | 铁(Fe) | C. | 红磷(P) | D. | 氮化硼(BN) |
分析 化学式能真实表示物质分子组成的是分子晶体,常见的分子晶体有:所有非金属氢化物、部分非金属单质(金刚石、晶体硅等除外)、部分非金属氧化物(二氧化硅等除外)、几乎所有的酸、绝大多数的有机物晶体,以此进行判断.
解答 解:A.硫酸形成的晶体为分子晶体,H2SO4能够真实表示硫酸的分子组成,故A正确;
B.Fe为金属晶体,晶体中存在金属阳离子和自由移动的电子,不存在分子,故B错误;
C.红磷是无数P原子按照一定规律排列而成的,P不能表示红磷的分子组成,故C错误;
D.NB为原子晶体,不存在NB分子,故D错误;
故选A.
点评 本题考查物质名称、化学式的关系及判断,题目难度中等,侧重于学生的分析能力的考查,掌握常见物质晶体类型及常见分子晶体是解答的关键.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
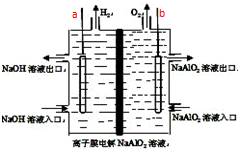 工业上利用离子膜电解偏铝酸钠溶液制备高品质的氢氧化铝,装置如图所示(a、b为电源的电极):该电池的总反应方程式为:4NaAlO2+10H2O$\frac{\underline{\;通电\;}}{\;}$ 4Al(OH)3↓+4NaOH+O2↑+2H2↑.电解池阳极室发生的电极反应式是4AlO2-+6H2O-4e-=4Al(OH)3↓+O2↑,该离子膜为阳离子交换膜(填“阴”或“阳”)
工业上利用离子膜电解偏铝酸钠溶液制备高品质的氢氧化铝,装置如图所示(a、b为电源的电极):该电池的总反应方程式为:4NaAlO2+10H2O$\frac{\underline{\;通电\;}}{\;}$ 4Al(OH)3↓+4NaOH+O2↑+2H2↑.电解池阳极室发生的电极反应式是4AlO2-+6H2O-4e-=4Al(OH)3↓+O2↑,该离子膜为阳离子交换膜(填“阴”或“阳”)查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 实验方案 | 实验现象 | 结论 |
| 将白色晶体溶于水,并滴2滴淀粉溶液 | 得到无色溶液 | |
| 取少量溶液于试管A中,加入足量的1mol•L-1H2SO4 | 溶液呈蓝色 | 溶液中含IO3- |
| 另取少量溶液于试管B中,滴入几滴酚酞溶液 | 溶液变红 | 溶液中含大量OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
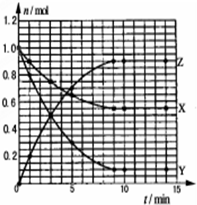 某温度时,在2L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随时间的变化如图所示,则下列说法错误的是( )
某温度时,在2L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随时间的变化如图所示,则下列说法错误的是( )| A. | 反应的化学方程式是X+2Y?2Z | |
| B. | 该反应在0-3min时间内产物Z的平均反应速率0.083mol•L-1•min-1 | |
| C. | 由图象知该反应吸收能量 | |
| D. | 其他条件不变,升高温度,若正反应速率增大,则逆反应速率将减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 12 mol | B. | 14 mol | C. | 16 mol | D. | 18 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 15g甲基(-CH3)所含有的电子数是10NA | |
| B. | 常温常压下,30g甲醛所含有的原子数目为4NA | |
| C. | 标准状况下,1L戊烷充分燃烧后生成的气态产物的分子数为5/22.4 NA | |
| D. | 常温常压下,1mol丙烷所含有的共价键数目为12NA |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | NH4HCO3溶于过量的浓KOH溶液中:NH4++HCO3-+2OH-=CO32-+NH3↑+2 H2O | |
| B. | 用浓盐酸检验氨:NH3+HCl=NH4Cl | |
| C. | 钢铁发生吸氧腐蚀时,铁作负极被氧化:Fe-3e-=Fe3+ | |
| D. | 用铜做电极电解CuSO4溶液:2Cu2++2H2O$\frac{\underline{\;电解\;}}{\;}$2Cu+O2↑+4H+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com