
【题目】叠氮化钠(NaN3)是制备医药、炸药的一种重要原料,采用“亚硝酸甲酯——水合肼法”制备叠氮化钠的生产流程如下:
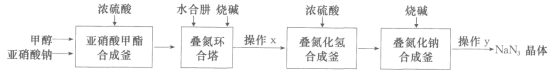
回答下列问题:
(1)亚硝酸甲酯合成釜中生成的亚硝酸甲酯(CH3ONO)易转化为气态进入叠氮环合塔,写出生成CH3ONO的化学反应方程式:___。
(2)叠氮环合塔中生成叠氮化钠的反应方程式为___。
(3)水合肼(N2H4·H2O)的性质类似一水合氨,与硫酸反应可以生成酸式盐,该盐的化学式为___;叠氮环合塔中滴加的烧碱溶液要适当过量,目的是__ ;生产流程中操作x为加热、浓缩,此时所得浓缩液的溶质中含钠的化合物有Na2SO4和___。
(4)该生产过程中可循环使用的物质是___。
(5)生产中有HN3生成,请设计实验证明HN3为弱酸:___。
(6)化工生产中,多余的NaN3常使用次氯酸钠溶液处理,在酸性条件下,二者反应可生成无毒的气体。若处理6.5gNaN3,理论上需加入0.5mol·L-1的NaClO溶液___mL。
【答案】2CH3OH+2NaNO2+H2SO4=2CH3ONO+Na2SO4+2H2O N2H4+CH3ONO+NaOH=NaN3+CH3OH+2H2O (N2H6)(HSO4)2 提高亚硝酸甲酯和水合肼的转化率,抑制叠氮化钠水解 NaN3、NaOH 甲醇 使用pH试纸测定NaN3溶液的酸碱性,若该溶液显碱性,说明HN3为弱酸(也可采用其他方法,如测定0.1 mol/LHN3的pH,若pH大于1,说明HN3为弱酸) 100
【解析】
本题是一道无机制备类信息题,各步骤的反应物和产物已经标出,故难度较低,顺水推舟即可。
(1)根据装置图可以发现亚硝酸甲酯合成釜有三种原料:浓硫酸、甲醇和亚硝酸钠,浓硫酸可以酸化亚硝酸钠,并为酯化反应提供催化剂,得到甲醇的无机酸酯和水,据此写出反应方程式即可:![]() ;
;
(2)叠氮环合塔中加入了水合肼与烧碱,烧碱可以使第一步得到的亚硝酸甲酯水解,产生甲醇和亚硝酸钠,同时亚硝酸钠和肼里的氮元素发生归中反应得到产物叠氮化钠,据此写出方程式即可:![]() ;
;
(3)既然水合肼的性质类似一水合氨,在水中应该能电离产生![]() 和
和![]() ,因此它的硫酸酸式盐的化学式为
,因此它的硫酸酸式盐的化学式为![]() ;叠氮环合塔中适当滴加过量的烧碱有两个作用,一方面可以提高亚硝酸甲酯和水合肼的转化率,另一方面可以抑制叠氮化钠这个强碱弱酸盐的水解;加热浓缩后,溶液中的阴离子有
;叠氮环合塔中适当滴加过量的烧碱有两个作用,一方面可以提高亚硝酸甲酯和水合肼的转化率,另一方面可以抑制叠氮化钠这个强碱弱酸盐的水解;加热浓缩后,溶液中的阴离子有![]() 和
和![]() ,因此含钠的化合物有
,因此含钠的化合物有![]() 、
、![]() 和
和![]() ;
;
(4)由于在亚硝酸甲酯合成釜里形成了酯,在叠氮环合塔中酯又水解,因此整个过程中甲醇是可以循环利用的;
(5)若要证明![]() 为弱酸,可以用pH试纸来检测
为弱酸,可以用pH试纸来检测![]() 溶液的pH,根据“有弱就水解”的规则,若溶液显碱性,则证明
溶液的pH,根据“有弱就水解”的规则,若溶液显碱性,则证明![]() 为弱酸,其它合理的方法也可以;
为弱酸,其它合理的方法也可以;
(6)根据描述,![]() 应该被氧化为无毒的
应该被氧化为无毒的![]() 。同时
。同时![]() 被还原为
被还原为![]() ,因此每个
,因此每个![]() 在反应中需要失去1个电子,每个
在反应中需要失去1个电子,每个![]() 在反应中可以得到2个电子,二者的物质的量之比为2:1
在反应中可以得到2个电子,二者的物质的量之比为2:1![]() 的物质的量
的物质的量![]() ,则需要
,则需要![]() 的物质的量为0.05mol,因此需要次氯酸钠溶液体积
的物质的量为0.05mol,因此需要次氯酸钠溶液体积![]() 。
。


 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案 黄冈创优卷系列答案
黄冈创优卷系列答案科目:高中化学 来源: 题型:
【题目】在一定温度下,当过量的Mg(OH)2固体在水溶液中达到平衡时:Mg(OH)2(s)![]() Mg2+(aq)+2OH-(aq),要使Mg(OH)2固体增加,c(OH-)增加,可采取的措施是
Mg2+(aq)+2OH-(aq),要使Mg(OH)2固体增加,c(OH-)增加,可采取的措施是
A.加适量的水B.通入少量HCl气体
C.加少量NaOH固体D.加少量MgSO4固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图中甲池的总反应式为![]() 。
。
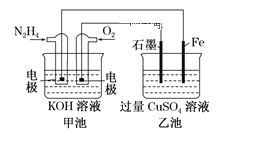
(1)甲池中负极上的电极反应式为_____________________。
(2)乙池中石墨电极上电极反应式为_________________________________。
(3)要使乙池恢复到电解前的状态,应向溶液中加入适量的 _______________。
A.CuO B.Cu(OH)2 C.CuCO3 D.CuSO4
(4)若将乙池中两个电极改成等质量的Fe和Cu,实现在Fe上镀Cu,当甲中消耗1.6gN2H4时,乙池中两个电极质量差为_________________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物Y具有抗菌、消炎作用,可由X制得。
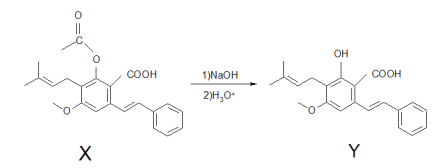
下列有关化合物X、Y的说法正确的是
A.X与NaOH溶液能反应,与Na2CO3溶液、 NaHCO3溶液均不反应
B.Y与乙醇发生酯化反应可得到X
C.X、Y均不能与酸性KMnO4溶液反应
D.室温下X、Y分别与足量Br2加成的产物分子中手性碳原子数目相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列原子或原子团,请按要求选择两个,写出符合要求的有机物的结构简式:﹣CH3、﹣OH、﹣CHO、﹣COOH、﹣Br、﹣H、﹣CH2CH3、![]()
(l)分子结构为正四面体的是:___;
(2)能使FeCl3溶液显紫色的是:___;
(3)在NaOH乙醇溶液中能发生消去反应的是:____;
(4)1mol该有机物与足量的银氨溶液反应,有4molAg生成的是:___;
(5)相对分子质量是60,能和NaHCO3反应放出CO2的是:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,A、B、C、D、E、F、G均为有机物,它们之间有如下转化关系(部分产物和反应条件已略去)。已知B分子中含有苯环,其蒸气密度是同温同压下H2密度的59倍,1molB最多可以和4molH2发生加成反应,B的苯环上的一个氢原子被硝基取代所得的产物有三种。E和G都能够发生银镜反应。F分子中含有羟基和羧基,在一定条件下可以聚合生成高分子化合物。
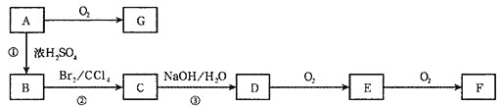
请回答下列问题:
(1)A的结构简式____________。
(2)反应①的反应类型是________。
(3)E与银氨溶液反应的化学方程式为_______。
(4)等物质的量的A与F发生酯化反应,所生成有机物的结构简式为________。
(5)A的一种同分异构体与浓H2SO4共热,也生成B和水,该同分异构体的结构简式为________。
(6)E有多种同分异构体,其中属于酯类且具有两个对位取代基的同分异构体共有_____种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】经实验测定某固体样品中只含有Na2O2和Na2CO3。现称取该样品13.1g,加入水充分反应后产生1.12L(标准状况下)气体,所得溶液体积为500mL。试计算:
(1)该样品含有Na2O2的质量分数为_________。
(2)反应后溶液中Na+的物质的量浓度为_________mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同学们已经学习了同位素、同系物、同素异形体、同分异构体,你能区别这些概念吗?下面列出了几组物质,请将物质的合适组号填写在下表中。
①![]() 和
和![]()
②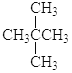 和
和![]()
③CH4和CH3CH2CH3;④金刚石与石墨;⑤氕、氘与氚;⑥16O、17O和18O;⑦乙醇(CH3CH2OH)和甲醚(CH3OCH3);⑧氧气(O2)与臭氧(O3)。
类别 | 同位素 | 同系物 | 同素异形体 | 同分异构体 |
组号 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:H2O(g)=H2O(l) ΔH=Q1 kJ·mol-1
C2H5OH(g)=C2H5OH(l)ΔH=Q2 kJ·mol-1
C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(g)ΔH=Q3 kJ·mol-1
若使46 g液体酒精完全燃烧,最后恢复到室温,则放出的热量为
A. -(3Q1-Q2+Q3) kJB. -0.5(Q1+Q2+Q3) kJ
C. -(0.5Q1-1.5Q2+0.5Q3) kJD. -(Q1+Q2+Q3) kJ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com