
�ྦྷ����̫���ܹ����ҵ����Ҫԭ�ϡ�
��1����ʯӢɰ����ȡ�ֹ裬����ط�Ӧ���Ȼ�ѧ����ʽ���£�

�ٷ�ӦSiO2��s��+2C��s��=Si��s��+2CO��g���ġ�H= kJ��mol-1���ú�a��b�Ĵ���ʽ��ʾ����
��SiO�Ƿ�Ӧ�����е��м�����������ʱ��SiO��NaOH��Һ��Ӧ������֮һ�ǹ����ƣ��Ļ�ѧ����ʽ�� ��
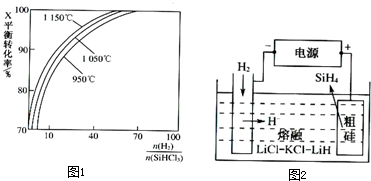
��2���ֹ��ᴿ��������֮һ���Ƚ��ֹ���HCl�Ƶ�SiHCl3�����ᴿ������H2��ԭ��SiHCl3��g��+H2��g�� Si��s��+3HCl��g����ͬ�¶ȼ���ͬn��H2��/n��SiHCl3��ʱ����Ӧ��X��ƽ��ת���ʹ�ϵ��ͼ��
Si��s��+3HCl��g����ͬ�¶ȼ���ͬn��H2��/n��SiHCl3��ʱ����Ӧ��X��ƽ��ת���ʹ�ϵ��ͼ��

��X�� ���H2������SiHCl3������
��������Ӧ��ƽ�ⳣ��K��1150�棩 K��950�棩��ѡ�>������<������=����
��3��SiH4�����飩�������ߴ��ྦྷ���Ƿdz�����ķ�����
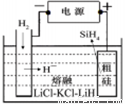
���ôֹ���ԭ�ϣ����ε�ⷨ��ȡ����ԭ����ͼ10�����ʱ�����ĵ缫��ӦʽΪ ��
�ڹ��̫���������N��Si����Ԫ����ɵĻ�����Y���ۻ����ϣ�������SiH4��NH3������������������õ�����֪Y��Si����������Ϊ60%��Y�Ļ�ѧʽΪ ��
��1����2a+b �� SiO+2NaOH=Na2SiO3+H2��
��2����SiHCl3 �ڣ�
��3��Si - 4e- + 4H- = SiH4�� Si3N4
��������
���������(1)����ʽ����ʽ��2����ʽ���ã���2������������ԭ��Ӧ���ϼ�����ȷ����ԭ����ΪH2�� SiO+2NaOH=Na2SiO3+H2������3�����ź�������ֵ���������ĺ�������Xת�����������Ը�������SiHCl3����ͬ��ֵʱ���¶�Խ�ߣ�SiHCl3ת����Խ������ӦΪ���ȷ�Ӧ���¶�Խ��KֵԽ��3�����ʱ�ֹ��ܽ��Ͻ����е�H-����ΪSi - 4e- + 4H- = SiH4��������������ϵ�������ʵ�����ϵȷ����ѧʽ��
���㣺���黯ѧ��Ӧԭ���з�Ӧ�ȵļ��㡢ƽ���ƶ��жϡ��绯ѧ֪ʶ���й����⡣


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| n(H2) | n(SiHCl3) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�콭��ʡ�����и�����ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ������
�ྦྷ����̫���ܹ����ҵ����Ҫԭ�ϡ�
��1����ʯӢɰ����ȡ�ֹ裬����ط�Ӧ���Ȼ�ѧ����ʽ���£�
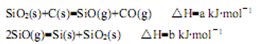
�ٷ�ӦSiO2��s��+2C��s��=Si��s��+2CO��g���ġ�H= kJ��mol-1���ú�a��b�Ĵ���ʽ��ʾ����
��SiO�Ƿ�Ӧ�����е��м�����������ʱ��SiO��NaOH��Һ��Ӧ������֮һ�ǹ����ƣ��Ļ�ѧ����ʽ�� ��
��2���ֹ��ᴿ��������֮һ���Ƚ��ֹ���HCl�Ƶ�SiHCl3�����ᴿ������H2��ԭ��SiHCl3��g��+H2��g�� Si��s��+3HCl��g����ͬ�¶ȼ���ͬn��H2��/n��SiHCl3��ʱ����Ӧ��X��ƽ��ת���ʹ�ϵ��ͼ��
Si��s��+3HCl��g����ͬ�¶ȼ���ͬn��H2��/n��SiHCl3��ʱ����Ӧ��X��ƽ��ת���ʹ�ϵ��ͼ��

��X�� ���H2������SiHCl3������
��������Ӧ��ƽ�ⳣ��K��1150�棩 K��950�棩��ѡ�>������<������=����
��3��SiH4�����飩�������ߴ��ྦྷ���Ƿdz�����ķ�����
���ôֹ���ԭ�ϣ����ε�ⷨ��ȡ����ԭ����ͼ10�����ʱ�����ĵ缫��ӦʽΪ ��
�ڹ��̫���������N��Si����Ԫ����ɵĻ�����Y���ۻ����ϣ�������SiH4��NH3������������������õ�����֪Y��Si����������Ϊ60%��Y�Ļ�ѧʽΪ ��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ���㽭ʡģ���� ���ͣ���ѡ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��ģ���� ���ͣ���ѡ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com