
����Ŀ����ҵ����һ����CO2�������״�ȼ�ϵķ�����CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g); ��H=-49.0kJ/mol��ij�¶��£���6molCO2��8molH2����2L���ܱ������У����H2�����ʵ�����ʱ��仯��ͼʵ����ʾ��ʵ�ߣ���ͼ������a��1,6����ʾ����1minʱH2�����ʵ�����6mol��
CH3OH(g)+H2O(g); ��H=-49.0kJ/mol��ij�¶��£���6molCO2��8molH2����2L���ܱ������У����H2�����ʵ�����ʱ��仯��ͼʵ����ʾ��ʵ�ߣ���ͼ������a��1,6����ʾ����1minʱH2�����ʵ�����6mol��
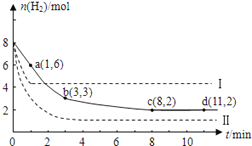
��1����һ������H2��ƽ����Ӧ������________��ʽ��������¶��µĻ�ѧƽ�ⳣ��K=______
��2������ʱ���ƽ����Ӧ����������_______
A.0-1min B.1-3min C.3-8min D.8-11min
��3�����ı�ijһʵ�������ٽ�������ʵ����H2�����ʵ�����ʱ��仯��ͼ��������ʾ������I��Ӧ��ʵ�������ı���__________�����ߢ��Ӧ��ʵ�������ı����_____________��
��4������d��ʱ����ϵ�ڳ���2molCO2��2molH2O����ʱV��_____V�������ڣ�С�ڣ����ڣ�
��5����֪��
��CO(g)+1/2O2(g)=CO2(g); ��H1=-283.0kJ/mol
��H2(g)+1/2O2(g)=H2O(g); ��H2=-241.8kJ/mol
��CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g); ��H3=-192.2kJ/mol
�ڹ�ҵ�ϳ���CO��H2�ϳɼ״����÷�Ӧ���ȷ���ʽΪ_____________
��6����ͼ�Ǽ״�ȼ�ϵ��ԭ��ʾ��ͼ���ش��������⣺��ظ����ĵ缫��Ӧ�ǣ�__________��

���𰸡� 1mol/(L��min) K=(1��1)/(2��1)=0.5 A ���� ����ѹǿ������CO2Ũ�� С�� CO(g)+2H2(g) ![]() CH3OH(g) ��H=-574.4kJ/mol CH3OH+8OH--6e-=CO32-+6H2O
CH3OH(g) ��H=-574.4kJ/mol CH3OH+8OH--6e-=CO32-+6H2O
��������(1)��һ������H2��ƽ����Ӧ������ =1mol/(L��min) �� CO2(g)+3H2(g)
=1mol/(L��min) �� CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)��ʼ���ʵ���/mol6 8 00���ʵ����仯/mol262 2ƽ�����ʵ���/mol 4 2 22
CH3OH(g)+H2O(g)��ʼ���ʵ���/mol6 8 00���ʵ����仯/mol262 2ƽ�����ʵ���/mol 4 2 22
K=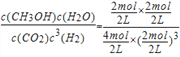 =0.5L2mol-2��(2)�ֱ���㲻ͬʱ���ڵķ�Ӧ���ʣ�0��1min�ڣ�v(H2)=1mol/(L��min) ��1��3min�ڣ�v(H2)=
=0.5L2mol-2��(2)�ֱ���㲻ͬʱ���ڵķ�Ӧ���ʣ�0��1min�ڣ�v(H2)=1mol/(L��min) ��1��3min�ڣ�v(H2)= ![]() =0.75mol/(Lmin)��3��8min�ڣ�v(H2)=
=0.75mol/(Lmin)��3��8min�ڣ�v(H2)= ![]() =0.1mol/(Lmin)��8min��ﵽ��ѧƽ��״̬�����淴Ӧ������ȣ��ۺ�����Ϊ�㣻����0��1min�ڷ�Ӧ�������8��11min��Ӧ������С���ʴ�ΪA��(3)����I��Ӧ��������ת�������������ʵ����٣�Ӧ�������¶ȣ���÷�Ӧ���ȣ������¶�ƽ�������ƶ���������������ת����������I�������¶ȣ���������Ӧ��������ת�������������ʵ����࣬������ѹǿƽ�������ƶ�����Ӧ������ѹǿ�����������̼Ũ��Ҳ��ʹƽ��������У�
=0.1mol/(Lmin)��8min��ﵽ��ѧƽ��״̬�����淴Ӧ������ȣ��ۺ�����Ϊ�㣻����0��1min�ڷ�Ӧ�������8��11min��Ӧ������С���ʴ�ΪA��(3)����I��Ӧ��������ת�������������ʵ����٣�Ӧ�������¶ȣ���÷�Ӧ���ȣ������¶�ƽ�������ƶ���������������ת����������I�������¶ȣ���������Ӧ��������ת�������������ʵ����࣬������ѹǿƽ�������ƶ�����Ӧ������ѹǿ�����������̼Ũ��Ҳ��ʹƽ��������У�
(4) ����d��ʱ����ϵ�ڳ���2molCO2��2molH2O����ʱQc=![]() =
= =
=![]() L2mol-2��K����ʱƽ�������ƶ�����V��С��V����
L2mol-2��K����ʱƽ�������ƶ�����V��С��V����
(5)��֪����CO(g)+1/2O2(g)=CO2(g); ��H1=-283.0kJ/mol����H2(g)+1/2O2(g)=H2O(g); ��H2=-241.8kJ/mol����CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g); ��H3=-192.2kJ/mol�����ݸ�˹���ɿ�֪��+����2-���ɵ� CO(g)+2H2(g) ![]() CH3OH(g)���� ��H=(-283.0kJ/mol)+(-241.8kJ/mol)��2-(-192.2kJ/mol)=-574.4kJ/mol��CO��H2�ϳɼ״����ȷ���ʽΪ CO(g)+2H2(g)
CH3OH(g)���� ��H=(-283.0kJ/mol)+(-241.8kJ/mol)��2-(-192.2kJ/mol)=-574.4kJ/mol��CO��H2�ϳɼ״����ȷ���ʽΪ CO(g)+2H2(g) ![]() CH3OH(g) ��H=-574.4kJ/mol ��
CH3OH(g) ��H=-574.4kJ/mol ��
(6)�״�ȼ�ϵ���У�ͨ��������b��Ϊԭ��ص������������õ��ӵĻ�ԭ��Ӧ���ڼ��Ի����£��缫��ӦʽΪ��2H2O+4e-+O2�T4OH-��ͨ��״���a��Ϊԭ��صĸ���������ʧ���ӵ�������Ӧ���缫��ӦʽΪ��CH3OH+8OH--6e-�TCO32-+6H2O��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ϊһ������Դ�ڻ�ѧ����Ӧ�ù㷺����ش��������⣺
(1)��¯ұ�������У������ڴ���Ӧ���в���ˮú��(CO��H2)��ԭ���������йط�ӦΪ��
CH4(g)+CO2(g)![]() 2CO(g)+2H2(g) ��H=260kJmol��1
2CO(g)+2H2(g) ��H=260kJmol��1
��֪��2CO(g)+O2(g)![]() 2CO2(g) ��H=��566kJmol��1
2CO2(g) ��H=��566kJmol��1
��CH4��O2��Ӧ����CO��H2���Ȼ�ѧ����ʽΪ ��
(2)��ͼ��ʾ��װ����Ϊ����ȼ�ϵ��(�������ҺΪKOH��Һ)��ͨ��װ����ʵ�������϶�ͭ��
��b���缫�Ϸ����ĵ缫��Ӧʽ�� ��
����ƽ�����װ������KOH��Һ��Ũ�� (��д���������С�����䡱)��װ������Cu�缫�Ϸ����ĵ缫��Ӧʽ�� ��
���ڴ˹���������ȫ��Ӧ��װ���������������仯12.8g����װ���������������ļ��� L(��״����)��

��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ��ˮ�г�����һ������Cr2O72����CrO42�������ǻ�����༰��̬ϵͳ�����ܴ���˺���������д������÷��Ĺ�������ΪCrO42��![]() Cr2O72��
Cr2O72��![]() Cr3+
Cr3+![]() Cr(OH)3�� ���е���������ƽ�⣺2CrO42������ɫ��+2H+
Cr(OH)3�� ���е���������ƽ�⣺2CrO42������ɫ��+2H+![]() Cr2O72������ɫ��+H2O
Cr2O72������ɫ��+H2O
��1����ƽ����ϵ��pH=2������Һ�� ɫ��
��2����˵����������Ӧ��ƽ��״̬���� ����ѡ���ţ�
a��Cr2O72����CrO42����Ũ����ͬ b��v��(Cr2O72��)=2v��(CrO42��)
c����Һ����ɫ���� d����Һ��pHֵ����
��3��д����������Cr2O72��ת��ΪCr3+�����ӷ���ʽ�� ��
��4����Cr2(SO4)3��Һ�У��μ�NaOH����pH=4.6ʱ����ʼ����Cr(OH)3����������pH�����ߣ��������࣬����pH��13ʱ��������ʧ����������ɫ��[Cr��OH��4]�����ӣ���ƽ���ϵ���£�H++[Cr(OH)4]��������ɫ��![]() Cr��OH��3��s������ɫ��+H2O
Cr��OH��3��s������ɫ��+H2O ![]() Cr3+����ɫ��+H2O +3OH��������0.05mol��L��1��Cr2(SO4)3��Һ50mL�У���������0.6mol��L��1��NaOH��Һ����ַ�Ӧ����Һ�пɹ۲쵽������Ϊ ��
Cr3+����ɫ��+H2O +3OH��������0.05mol��L��1��Cr2(SO4)3��Һ50mL�У���������0.6mol��L��1��NaOH��Һ����ַ�Ӧ����Һ�пɹ۲쵽������Ϊ ��
��5����Na[Cr��OH��4]��Na2Cr2O7��Ϻ����Һ�м���H2SO4�ữ����Ԫ���� ��ʽ���ڣ���д���ӷ��ţ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������Ԫ��X��Y��Z��W��ԭ������������������Ԫ���γɵĵ�������Ϊm��n��p��q��r��t��u����ЩԪ����ɵĶ�Ԫ���������uΪ�γ��������Ҫ����֮һ��25��ʱ��0.01mol��L-1��v��Һ�У�c��OH-��/c��H+��=1.0��1010���������ʵ�ת����ϵ��ͼ��ʾ������˵����ȷ����
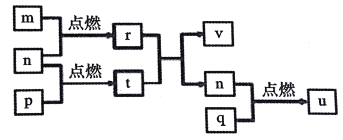
A. ԭ�Ӱ뾶�Ĵ�С��W>Z>Y>X
B. Z�ֱ���Y��W��ɵĻ������л�ѧ�����Ϳ�����ͬ
C. v������ˮ�ĵ����u�ܴٽ�ˮ�ĵ���
D. ճ��q���Թܿ��þƾ�ϴ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڳ����ܽ�ƽ����ܶȻ�����������˵������ȷ����
A��������Na2SO4��Һ���뵽����ʯ��ˮ�У��а�ɫ����������˵��Ksp[Ca(OH)2]����Ksp(CaSO4)
B��Kspֻ�����ܵ���ʵ����ʺ��¶��йأ�������Һ�е�����Ũ����
C����֪25��ʱ��Ksp[Fe(OH)3]=4.0��10-38�����¶��·�ӦFe(OH)3+3H+![]() Fe3++3H2O��ƽ�ⳣ��K=4.0��10-4
Fe3++3H2O��ƽ�ⳣ��K=4.0��10-4
D����֪25��ʱ��Ksp[Mg(OH)2]=1.8��10-11����MgCl2��Һ�м��백ˮ����û��Һ��pH=11������Һ�е�c(Mg2+)Ϊ1.8��10-5molL-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������������أ��ֲ�Ӧ�ÿ���������ʹ���������������Ľṹ���Ա�ʾΪ��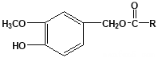 (RΪ����)������һ���������������J�ĺϳ�·�����£�
(RΪ����)������һ���������������J�ĺϳ�·�����£�
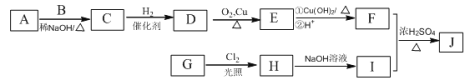
��֪��
��A��B��EΪͬϵ�����B����Է�������Ϊ44��A��B�˴Ź���������ʾ�����������������ȷֱ�Ϊ9��1��3��1��
�ڻ�����J�ķ���ʽΪC15H22O4��
��
�ش��������⣺
��1��G������������� �� ��
��2����C����D�ķ�Ӧ����Ϊ ��D�Ļ�ѧ����Ϊ ��
��3���ٵĻ�ѧ����ʽΪ ��
��4��J�Ľṹ��ʽΪ ��
��5��G��ͬ���칹���У������ϵ�һ�ȴ���ֻ��һ�ֵĹ��� ��(���������칹)���˴Ź���������ʾ2������ (д�ṹ��ʽ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X��Y��Z��M��WΪ���ֶ�����Ԫ����X��Y��Z��ԭ���������ε�����ͬ����Ԫ�أ�������������֮��Ϊ15��X��Z���γ�XZ2������Ѿ��M�γɵ���̬�������ڱ�״���µ��ܶ�Ϊ0.76g��L-1�� W����������X��Y��Z��M����Ԫ��������֮�͵�![]() ������˵����ȷ����
������˵����ȷ����
A. ԭ�Ӱ뾶��W>Z>Y>X>M
B. YZ2����ˮ�γɵ���Һ���н�ǿ��������
C. ��X��Y��Z��M����Ԫ���γɵĻ�����һ���������Ӽ������й��ۼ�
D. 1 molWM��������ˮ����ȫ��Ӧ��ת��2mol����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1�� ��ú��Ϊȼ�Ͽ�ͨ����������;����
;��I��ֱ��ȼ��C(s)+O2(g)�TCO2(g)������Q1kJ��
;��II�����Ƴ�ˮú����C(s)+H2O(g)�TCO(g)+H2(g)������Q2kJ��
��ȼ��ˮú����2CO(g)+O2(g)�T2CO2(g)
2H2(g)+O2(g)�T2H2O(g)��������Q3kJ��
�Իش��������⣺
���ж�����;���ų�������С��;��I ______������ڡ��������ڡ���С�ڡ���;��II
��Q 1��Q 2 ��Q 3 ����ѧ��ϵʽ��________________________��
����֪1 g������ȫȼ������Һ̬ˮʱ�ų�����143 kJ��18 gˮ�������Һ̬ˮ�ų�44 kJ��������
��������������±��������x��ֵΪ_____________��
O===O | H��H | H��O(g) | |
1 mol��ѧ������ʱ��Ҫ���յ�����/kJ | 496 | 436 | x |
�ܼ���úͨ��;������Ϊȼ�ϵ����壺______________________________

��2����ѧ��Ӧ����Ϊ�ɼ����Ѻ��¼��γɵĹ��̡���ͼΪ���ף�P4����P4O6���ӵķ��ӽṹʾ��ͼ����������������±���ʾ����ӦP4 +3O2 = P4O6�������仯Ϊ��__________________��
O===O | P��P | P��O | |
1 mol��ѧ������ʱ��Ҫ���յ�����/kJ | 496 | 198 | 360 |
��3�����б仯�����ڷ��ȷ�Ӧ����______
A��Ba(OH)2��8H2O������NH4Cl����ķ�Ӧ
B��þ���������̼��Ӧ
C���ɱ�����Ϊ����
D��̼��Ƹ��¶���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ƽ�а������±����л���A��B���й���Ϣ��
A | B |
����ʹ������Ȼ�̼��Һ��ɫ �ڱ���ģ��Ϊ�� ������ˮ��һ�������·�Ӧ���ɴ� | ����C��H����Ԫ����� �����ģ��Ϊ�� |
���ݱ�����Ϣ�ش��������⣺
��1��д��A�ĵ���ʽ_____________________��
��2��д����һ�������£�A���ɸ߷��ӻ�����Ļ�ѧ��Ӧ����ʽ________________________________��
��3��A�����������ӳɷ�Ӧ�����ɷ���C��C�ڷ�����ɺͽṹ�����Ƶ��л�����һ���ࣨ�׳ơ�ͬϵ��������Ǿ�����ͨʽCnH2n��2����n��_____ ʱ�������л��↑ʼ����ͬ���칹�塣
��4��B���е�������_____________________������ţ���
����ɫ��ζҺ�� ���ж� �۲�����ˮ ���ܶȱ�ˮ��
��������KMnO4��Һ����ˮ��Ӧʹ֮��ɫ ���κ������²���������Ӧ
��5��д����Ũ���������£�B��Ũ���ᷴӦ�Ļ�ѧ����ʽ��_____________________________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com