
【题目】某化学兴趣小组为探究元素性质的递变规律,设计了如下系列实验。
I.将 NaOH溶液与 NH4Cl 溶液混合生成 NH3·H2O,从而验证NaOH的碱性大于NH3·H2O,继而可以验证Na的金属性大于N,你认为此设计是否合理?并说明理由:_________。
II.根据下图所示装置图回答以下问题。
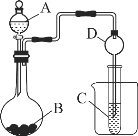
(1)实验室中现有药品Na2S、KMnO4、浓盐酸,某同学验证氯的非金属性大于硫,请写出试管中发的离子反应方程式______
(2)甲同学根据元素非金属性与对应最高价含氧酸之间关系,设计了如图装置来一次性完成N、C、Si三种非金属元素的非金属性强弱比较的实验研究;写出选用物质的名称:A__,B__,C___;上述反应的离子方程式_____;_____。
【答案】不合理,NH3·H2O并非为N的最高价氧化物对应的水化物 S2-+Cl2=S+2Cl- 稀硝酸 碳酸钙或其它碳酸盐 硅酸钠溶液 CaCO3+2H+=Ca2++2CO2↑+H2O SiO32-+CO2+H2O═H2SiO3↓+CO32-
【解析】
Ⅰ.元素的最高价氧化物的水化物的碱性越强,元素的金属性越强;
Ⅱ.(1)KMnO4与浓盐酸反应生成氯气,氯气置换出Na2S中的硫;
(2)要证明非金属性:N>C>Si,硝酸与碳酸钙反应生成二氧化碳、二氧化碳和硅酸钠反应生成难溶性的硅酸来证明。
Ⅰ.将NaOH溶液与NH4Cl溶液混合生成NH3H2O,可以说明NaOH的碱性大于NH3H2O,但不能说明Na的金属性大于N,因为要验证金属性的强弱,必须通过比较最高价氧化物所对应的水化物的碱性来进行比较,而NH3H2O不是氮元素的最高价氧化物的水化物。
(1)试管中氯气与Na2S反应生成氯化钠和硫,反应的离子反应方程式是S2-+Cl2=S+2Cl-;
(2)硝酸与碳酸钙反应生成二氧化碳、二氧化碳和硅酸钠反应生成难溶性的硅酸,可以证明非金属性:N>C>Si;则选用物质的名称:A是稀硝酸,B是碳酸钙,C是硅酸钠溶液;稀硝酸与碳酸钙反应的离子方程式是CaCO3+2H+=Ca2++2CO2↑+H2O;二氧化碳与硅酸钠溶液反应的离子方程式是SiO32-+CO2+H2O═H2SiO3↓+CO32-。


科目:高中化学 来源: 题型:
【题目】下列叙述中,不能用勒夏特列原理解释的是
A. 合成氨工业使用催化剂,可提高氨的日产量
B. 合成氨工业通常采用高压,以提高原料的利用率
C. 工业生产硫酸的过程中使用过量的氧气,以提高二氧化硫的转化率
D. 氯气在饱和食盐水中的溶解度比在水中的小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是
A.焰色反应是化学变化
B.CO2通入CaCl2溶液中会产生白色沉淀
C.Fe3+遇KSCN溶液会产生红色沉淀
D.25 ℃,Na2CO3在水中的溶解度比NaHCO3大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学为检验溶液中是否含有常见的四种无机离子,进行了下图所示的实验操作。其中检验过程中产生的气体能使湿润的红色石蕊试纸变蓝。由该实验能得到的正确结论是( )
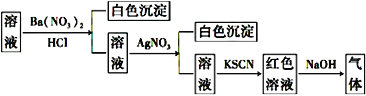
A. 原溶液中一定含有SO42-B. 原溶液中一定含有NH4+
C. 原溶液中一定含有Cl-D. 原溶液中一定含有Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水资源开发利用的部分过程如图所示:

下列说法不正确的是
A. 海水淡化的常用方法有蒸馏法、 电渗析法和离子交换法
B. 可通过分液的方法分离溴单质和苯的混合物
C. 提纯时,所加试剂可依次为 BaCl2、 NaOH、 Na2CO3、盐酸
D. 精盐、 NH3和 CO2是侯德榜制碱工业的主要原料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】16.8gFe跟一定量浓 HNO3 反应,Fe 全部溶解,共收集NO、NO2的总体积为 11.2 L(标准状况),所得溶液中 H+的物质的量为0.02mol,请回答:
(1)反应中被还原的硝酸为_______mol。
(2)生成的 NO 与 NO2 的物质的量之比为______。
(3)写出该反应的离子方程式:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验原理、装置、操作或结论的描述,错误的是( )

A. 图1所示装置可实现甲烷与氯气在光照条件下的取代反应
B. 图2所示装置可分离CH3CH2OH和CH3COOC2H5的混合液
C. 图3所示装置可用锌粒与稀硫酸反应制备氢气
D. 图4所示装置可说明浓H2SO4具有脱水性、强氧化性,SO2具有漂白性、还原性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学—选修有机化学基础]
化合物F是合成抗心律失常药—多非利特的中间体,以苯为原料合成F的路线如下:

已知:①CH3CH=CH2![]() CH3CHBrCH3 ②CH3CH=CH2
CH3CHBrCH3 ②CH3CH=CH2![]() CH3CH2CH2Br
CH3CH2CH2Br
试回答下列问题
(1)苯→A转化的反应类型是 。
(2)化合物C→D转化的反应条件通常是 ,化合物D (填“存在”、“不存在”)顺反异构,已知化合物C的核磁共振氢谱显示有四种峰,且峰的面积比为2︰2︰1︰3,则C的结构简式为 。
(3)写出E→F转化的化学方程式 。
(4)化合B的同分异构体有多种,满足以下条件的同分异构体共有 种。
①属于芳香族化合物
②分子结构中没有甲基,但有氨基
③能发生银镜反应和水解反应,并且与NaOH反应的物质的量之比为1︰2
(5)苯乙酮( )常用作有机化学合成的中间体,参照上述合成F的部分步骤,设计一条以苯为起始原料制备苯乙酮的合成路线 。
)常用作有机化学合成的中间体,参照上述合成F的部分步骤,设计一条以苯为起始原料制备苯乙酮的合成路线 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将1.0mol/L 盐酸滴入20mL 10mol/L氨水中,溶液pH随加入盐酸体积变化的曲线如右图所示。下列有关说法正确的是

A. a点,c(NH4+)=c(OH-)
B. b点,c(NH4+)>c(Cl-)>c(NH3·H2O)
C. c点,pH=7
D. d点,c(NH4+)+c(NH3·H2O)=c(Cl-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com