
在标准状况下,①6.72 L CH4气体 ②3.01×1023个HCl气体分子 ③13.6 g H2S气体 ④0.2 mol NH3,按下列要求对这四种气体的关系从大到小进行排列(用上述数字序号表示):
(1)标准状况下四种气体的体积 .
(2)四种气体的质量 .
 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案科目:高中化学 来源: 题型:
下表为某有机物与各种试剂反应的现象,则这种有机物可能是( )
| 试剂 | 钠 | 溴水 | NaHCO3 |
| 现象 | 放出气体 | 退色 | 不反应 |
A.CH2===CH—COOH B.CH2===CH—CH3
C.CH3COOCH2CH3 D.CH2===CH—CH2—OH
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素甲、乙、丙、丁的原子序数依次增大,甲和乙形成的气态化合物的水溶液呈碱性,乙位于第ⅤA族,甲和丙位于同一主族,丁原子的最外层电子数与电子层数相等。下列判断正确的是( )
A.原子半径:丙>乙>丁
B.单质的还原性:丁>丙>甲
C.甲、乙、丙的氧化物均为共价化合物
D.乙、丙、丁的最高价氧化物对应的水化物能相互反应
查看答案和解析>>
科目:高中化学 来源: 题型:
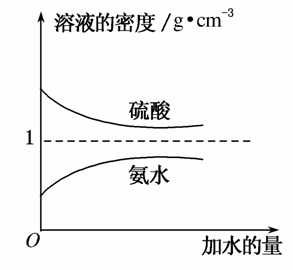
已知硫酸、氨水的密度与所加水量的关系如图所示,现有硫酸与氨水各一份,请根据表中信息,回答下列问题:
| 溶质的物质的量浓度/mol·L-1 | 溶液的密度 /g·cm-3 | |
| 硫酸 | c1 | ρ1 |
| 氨水 | c2 | ρ2 |
(1)表中硫酸的质量分数为________(不写单位,用含c1、ρ1的代数式表示)。
(2)物质的量浓度为c1 mol·L-1的硫酸与水等体积混合(混合后溶液体积变化忽略不计),所得溶液的物质的量浓度为________ mol·L-1。
(3)物质的量浓度为c2 mol·L-1的氨水与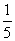 c2 mol·L-1的氨水等质量混合,所得溶液的密度________(填“大于”、“小于”或“等于”,下同)ρ2 g·cm-3,所得溶液的物质的量浓度________
c2 mol·L-1的氨水等质量混合,所得溶液的密度________(填“大于”、“小于”或“等于”,下同)ρ2 g·cm-3,所得溶液的物质的量浓度________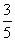 c2 mol·L-1(混合后溶液的体积变化忽略不计)。
c2 mol·L-1(混合后溶液的体积变化忽略不计)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列条件中,两种气体所含原子数一定相等的是 ( )
A.同质量、不同密度的N2和CO
B.同温度、同体积的H2和N2
C.同体积、同密度的C2H6和NO
D.同压强、同体积的N2O和CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
甲、乙、丙、丁为4种短周期元素,在周期表中,甲与乙、丙、丁在周期表中的位置关系如右图所示(原子序数:乙>丙).丁的原子序数与乙、丙原子序数之和相等,4种元素原子的最外层电子数之和为24.下列判断正确的是( )

|
| A. | 元素甲的简单气态氢化物稳定性比乙的强 |
|
| B. | 元素乙在周期表中的位置为第2周期,VIA族 |
|
| C. | 元素丙和元素丁的最高价氧化物对应的水化物均为强酸 |
|
| D. | 4种元素的简单阴离子半径从大到小顺序为:丁>乙>丙>甲 |
查看答案和解析>>
科目:高中化学 来源: 题型:
N2(g)+3H2(g) 2NH3(g) △H<0。当反应达到平衡时,下列措施能提高N2转化率的是
2NH3(g) △H<0。当反应达到平衡时,下列措施能提高N2转化率的是
① 降温 ② 恒压通入惰性气体 ③ 增加N2的浓度 ④ 加压
A.①④ B.①② C.②③ D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
用实验确定某酸HA是弱电解质。两同学的方案是:
甲:①称取一定质量的HA配制0.1 mol·L-1的溶液100 mL;
②用pH试纸测出该溶液的pH,即可证明HA是弱电解质。
乙:①用已知物质的量浓度的HA溶液、盐酸,分别配制pH=1的两种酸溶液各100 mL;
②分别取这两种溶液各10 mL,加水稀释为100 mL;
③各取相同体积的两种稀释液装入两只试管,同时加入纯度相同的锌粒,观察现象,即可证明HA是弱电解质。
(1)在两个方案的第①步中,都要用到的定量仪器是____________________。
(2)甲方案中,说明HA是弱电解质的理由是测得溶液的pH______1(选填“>”、“<”或“=”);乙方案中,说明HA是弱电解质的现象是_______。
a.装HCl 溶液的试管中放出H2的速率快
溶液的试管中放出H2的速率快
b.装HA溶液的试管中放出H2的速率快
c.两只试管中产生气体速率一样快
(3)请你评价:乙方案中难以实现之处或不妥之处_________________________。
(4)请你再提出一个合理而比较容易进行的方案(药品可任取),作简明扼要表述:___________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com