
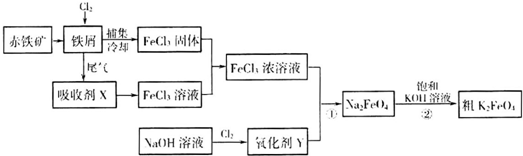
| 放电 |
| 充电 |
| 3×74.5×206.25t×96% |
| 2×396 |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:


| NaOH(aq) |
| △ |
 +H2O(R1、R2、R3为烃基或氢原子)
+H2O(R1、R2、R3为烃基或氢原子) 中含有酚羟基所用的试剂是
中含有酚羟基所用的试剂是查看答案和解析>>
科目:高中化学 来源: 题型:
 有机合成在制药工业上有着极其重要的地位.现用硝基苯制取苯胺,再用苯胺
有机合成在制药工业上有着极其重要的地位.现用硝基苯制取苯胺,再用苯胺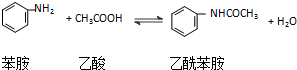
| 物 质 | 相对分 子质量 | 状 态 | 熔点 (℃) | 沸点 (℃) | 溶 解 度(g) | |
| 水 | 乙 醇 | |||||
| 苯 胺 | 93 | 无色液体 | -6 | 184 | 3.42(20℃) | 任意比混溶 |
| 冰醋酸 | 60 | 无色液体 | 17 | 118 | 任意比混溶 | 任意比混溶 |
| 乙酰苯胺 | 135 | 白色片 状固体 | 114 | 304 | 0.56(20℃)、3.45(50℃) 5.20(100℃) | 36.9(20℃) |

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

| A、气体甲的摩尔质量为44 |
| B、沉淀甲是硅酸和硅酸钙的混合物 |
| C、K+、CO32-、A102-和SiO32-一定存在于溶液X中 |
| D、SO42-一定不存在于溶液X中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
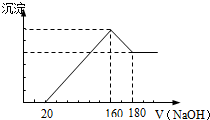 将一定质量的镁铝合金投入100mL一定浓度的盐酸中,合金完全溶解.向所得溶 液中滴加浓度为5mol/L的NaOH溶液,生成的沉淀跟加入的NaOH溶液的体积关系如图.(横坐标体积单位是mL,纵坐标质量单位是g)反应过程中涉及的化学方程式
将一定质量的镁铝合金投入100mL一定浓度的盐酸中,合金完全溶解.向所得溶 液中滴加浓度为5mol/L的NaOH溶液,生成的沉淀跟加入的NaOH溶液的体积关系如图.(横坐标体积单位是mL,纵坐标质量单位是g)反应过程中涉及的化学方程式查看答案和解析>>
科目:高中化学 来源: 题型:
| A、物质燃烧不一定是放热反应 |
| B、放热反应不需要从外界吸收任何能量就能发生 |
| C、在一个确定的化学反应中,反应物总能量总是高于生成物总能量 |
| D、化学反应除了生成新的物质外,还伴随着能量的变化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com