
| A. | 由于分子中氢原子数:H2SO4>HClO4,故酸性:H2SO4>HClO4 | |
| B. | 硅处于金属与非金属的过渡位置,硅可用作半导体材料 | |
| C. | 由于氮元素的最低化合价只有-3价,故NH5这种物质不可能存在 | |
| D. | Cl-、S2-、Ca2+、K+半径逐渐减小 |
分析 A、非金属性Cl>S,对应最高价氧化物的水化物的酸性为HClO4>H2SO4;
B、处于金属与非金属交界处的元素表现一定的金属性、非金属性;
C、可以存在离子化合物NH4H;
D、电子层结构相同,核电荷数越大离子半径越小,电子层越多离子半径越大.
解答 解:A.非金属性Cl>S,对应最高价氧化物的水化物的酸性为HClO4>H2SO4,与氢原子数无关,故A错误;
B.Si处于金属与非金属交界处,表现一定的金属性、非金属性,可用作半导体材料,故B正确;
C.可以存在离子化合物NH4H,化学式为NH5,故C错误;
D.电子层结构相同,核电荷数越大离子半径越小,故离子半径:S2->Cl->K+>Ca2+,故D错误,
故选B.
点评 本题考查酸性强弱、元素周期表、微粒半径比较等,难度不大,注意理解掌握微粒半径比较.


 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、Fe2+、NO3- | B. | Na+、Mg2+、NO3- | C. | Cu2+、Ba2+、Cl- | D. | K+、Na+、HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
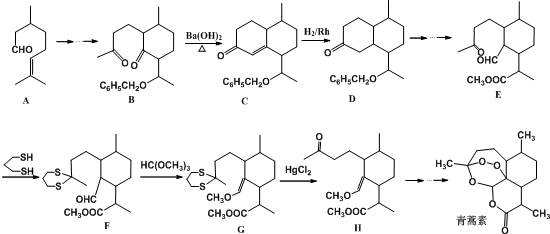
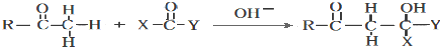
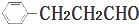 )的路线流程图.路线流程图示例如图:
)的路线流程图.路线流程图示例如图: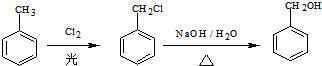
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
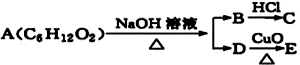 ,已知C能与NaHCO3反应产生气体,且C、E均不发生银镜反应,则A的可能结构有( )
,已知C能与NaHCO3反应产生气体,且C、E均不发生银镜反应,则A的可能结构有( )| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 18 g H2O含有10NA个质子 | |
| B. | 25℃时,PH=13的NaOH溶液中含有的OH- 数目为0.1NA | |
| C. | 标准状况下,22.4 L氨水含有NA个NH3分子 | |
| D. | 56 g铁片投入足量浓H2SO4中生成NA个SO2分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将N2和过量的O2在高温或放电的条件下反应得到红棕色的气体,说明NO为红棕色气体 | |
| B. | 在AgNO3溶液中加入锌粉,能置换出银,说明Ag+的还原性比Zn2+强 | |
| C. | 用干净的铂丝蘸取少量溶液在酒精灯外焰上灼烧,发现火焰呈黄色,则溶液中一定不含K+ | |
| D. | 浓硫酸放入蔗糖中,能使蔗糖炭化,说明浓硫酸具有脱水性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com