
【题目】氢氧化亚铁的制备:在一支试管中加入少量的硫酸亚铁溶液,然后滴入氢氧化钠溶液。
(1)观察到的实验现象是_________。
(2)用化学方程式表示产生上述现象的原因:_______________、________________
(3)在制取氢氧化亚铁时,可将吸有氢氧化钠溶液的长胶头滴管伸入到硫酸亚铁液面下,再挤出氢氧化钠溶液的目的是_________。
(4)下列各图所示的实验中能较长时间看到Fe(OH) 2 白色沉淀的是_______。
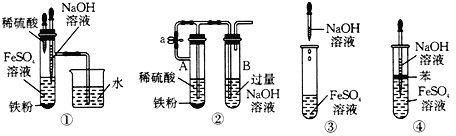
【答案】试管中先有白色沉淀生成,然后迅速变为灰绿色,最终变为红褐色 FeSO4+2NaOH=Na2SO4+Fe(OH)2↓ 4Fe(OH)2+O2+2 H2O=4Fe(OH)3 防止氢氧化钠滴入时带入的空气将生成的氢氧化亚铁氧化成氢氧化铁 ①②④
【解析】
(1)硫酸亚铁与氢氧化钠反应生成氢氧化亚铁白色沉淀和硫酸钠,氢氧化亚铁被空气中的氧气反应生成氢氧化铁;
(2)上述反应的方程式为FeSO4+2NaOH=Na2SO4+Fe(OH)2↓,4Fe(OH)2+O2+2 H2O=4Fe(OH)3;
(3)生成的氢氧化亚铁在溶液中生成,可减少与空气中氧气的接触,较长时间的观察氢氧化亚铁;
(4)装置①中Fe与稀硫酸生成的氢气能把试管中的空气排净;
装置②中开始时,Fe与稀硫酸生成的氢气能把试管中的空气排净,当有Fe剩余时,夹住止水夹a,可使试管A中的硫酸亚铁溶液进入试管B;
装置③中无法阻止空气中的氧气氧化生成的氢氧化亚铁;
装置④中,苯起到液封的作用,可阻止溶液与空气接触。
(1)硫酸亚铁与氢氧化钠反应生成氢氧化亚铁白色沉淀和硫酸钠,氢氧化亚铁被空气中的氧气反应生成氢氧化铁,观察到的现象为试管中先有白色沉淀生成,然后迅速变为灰绿色,最终变为红褐色;
(2)上述反应的方程式为FeSO4+2NaOH=Na2SO4+Fe(OH)2↓,4Fe(OH)2+O2+2 H2O=4Fe(OH)3;
(3)生成的氢氧化亚铁在溶液中生成,可减少与空气中氧气的接触,较长时间的观察氢氧化亚铁,则目的为防止氢氧化钠滴入时带入的空气将生成的氢氧化亚铁氧化成氢氧化铁;
(4)装置①中Fe与稀硫酸生成的氢气能把试管中的空气排净,防止氧气氧化氢氧化亚铁,符合题意,①正确;
装置②中开始时,Fe与稀硫酸生成的氢气能把试管中的空气排净,当有Fe剩余时,夹住止水夹a,可使试管A中的硫酸亚铁溶液进入试管B,可有效防止氧气氧化氢氧化亚铁,符合题意,②正确;
装置③中无法阻止空气中的氧气氧化生成的氢氧化亚铁,与题意不符,③错误;
装置④中,苯起到液封的作用,可阻止溶液与空气接触,效防止氧气氧化氢氧化亚铁,符合题意,④正确;
答案为①②④。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】在某温度下,可逆反应mA(g) + nB(g) ![]() pC(g) + qD(g)的平衡常数为K,下列说法正确的是( )
pC(g) + qD(g)的平衡常数为K,下列说法正确的是( )
A. K值越小,达到平衡时,反应物的转化率越大
B. K值越大,达到平衡时,生成物的含量越大
C. 反应物的转化率越大,达到平衡时,K值越大
D. 温度越高,达到平衡时,K值越大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对如图所示的实验装置中各部分仪器的主要作用的叙述正确的是( )

A.大烧杯d:防止在a发生破裂后使药品外溢
B.量气管b:读出反应前后与水面相平的刻度
C.水准管c:可方便地向整个装置中添加液体
D.温度计e:搅拌烧杯中的液体并且测量温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用常见烃A与某些烃的含氧衍生物可以制备PI(聚2-甲基-1,3-丁二烯)和PVB塑料。流程如图:
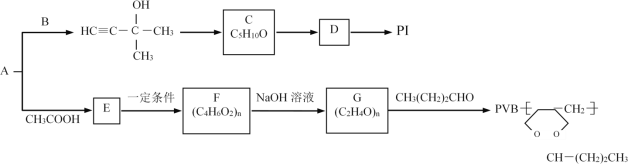
完成下列填空:
(1)A的名称是___,B的结构简式为___,C→D的反应条件是___,D→PI的反应类型是___。
(2)E中所含官能团的名称是___,写出符合下列条件的E的所有同分异构体的结构简式:___。
a.能发生银镜反应和水解反应
b.能与氢气发生加成反应
c.分子结构中含有一个甲基
(3)写出F→G的化学反应方程式:___。
(4)试用电石和乙醛等原料(无机试剂任选)制取1,3-丁二烯(合成正丁橡胶的原料),写出合成路线___。
(合成路线常用的表示方式为:A![]() B……
B……![]() 目标产物)
目标产物)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室可用如下方法制取Cl2,根据相关信息,回答下列问题:
(1)在该反应中,HCl表现的性质有______、________.
①MnO2 +4HCl(浓)![]() Cl2↑+ MnCl2+ 2H2O
Cl2↑+ MnCl2+ 2H2O
(2)若反应中有0.1mol的氧化剂被还原,则被氧化的物质为________(填化学式),被氧化物质的物质的量为 _____,同时转移电子数为_____(用NA表示)。
(3)将(2)生成的氯气与 0.2mol H2 完全反应,生成的气体在标准状况下所占体积为_________,将此产物溶于水配成100mL溶液,此溶液的物质的量浓度为_______。
(4)②KClO3+6HCl(浓)=3Cl2↑+KCl+3H2O③2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
若要制得相同质量的氯气,①②③三个反应中电子转移的数目之比为____。
(5)已知反应4HCl(g)+O2  2Cl2+2H2O(g),该反应也能制得氯气,则MnO2、O2、KMnO4三种物质氧化性由强到弱的顺序为_______。
2Cl2+2H2O(g),该反应也能制得氯气,则MnO2、O2、KMnO4三种物质氧化性由强到弱的顺序为_______。
(6)将不纯的NaOH样品2.50 g(样品含少量Na2CO3和水),放入50.0 mL 2.00mol/L盐酸中,充分反应后,溶液呈酸性,中和多余的酸又用去40.0 mL 1.00 mol/L的NaOH溶液。蒸发中和后的溶液,最终得到固体的质量为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年诺贝尔化学奖颁给了三位为锂离子电池发展作出重要贡献的科学家。用太阳能电池给磷酸铁锂锂离子电池充电示意图如图所示,阳极反应式为:LiFePO4-xe-=xLi++Li1-xFePO4。下列叙述错误的是

A.晶体硅能将太阳能转化为电能,但硅太阳能电池不属于原电池
B.该锂电池放电时负极反应为:LixC6-xe-=xLi++Li1-xC6
C.该锂电池放电时,电子通过外电路由铝箔流向钢箔
D.磷酸铁锂锂离子电池充放电过程通过Li+迁移实现,Fe、C、P元素化合价均不发生变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】间氯苯甲醛是新型农药、医药等有机合成的中间体,是重要的有机化工产品。实验室制取间氯苯甲醛的过程如下。
Ⅰ.Cl2的制备
舍勒发现氯气的方法至今还用于实验室制备氯气。本实验中利用该方法制备Cl2。
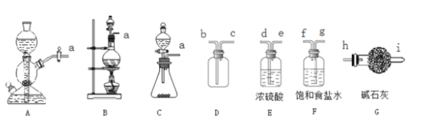
(1)该方法可以选择图中的_____(填字母标号)为Cl2发生装置,反应中氧化剂和还原剂的物质的量之比为_______。
(2)选择图中的装置收集一瓶纯净干燥的Cl2,接口的连接顺序为a→___________(按气流方向,填小写字母标号)
(3)试用平衡移动原理解释用饱和食盐水除去Cl2中混有的HCl的原因:_____________________。
Ⅱ.间氯苯甲醛的制备
反应原理:
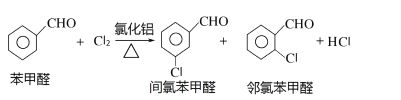
实验装置和流程如图所示:
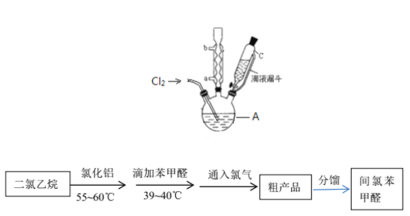
(4)图中仪器A的名称是_____________。
(5)间氯苯甲醛的制备过程中,二氯乙烷的作用是________________________;该实验要求无水操作,理由是____________________________________________;该实验有两次恒温过程,为控制反应温度仪器A处可采用________加热的方法。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种微生物燃料电池如图所示,下列关于该电池说法正确的是

A.a电极发生还原反应,做原电池的正极
B.b电极反应式为:2NO3-+10e-+12H+=N2↑+6H2O
C.H+由右室通过质子交换膜进入左室
D.标准状况下,电路中产生6moLCO2同时产生22.4L的N2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将3.9 g Mg、Al合金溶于一定物质的量浓度的HCl溶液400 mL中,刚好完全反应,经检测合金和盐酸都无剩余,再向反应后的溶液中加入1mol/L的NaOH溶液后,生成沉淀。如果加入一定量的NaOH溶液至沉淀量最大时,溶液的总体积刚好为合金溶解时体积的两倍,假设完全反应(不考虑体积变化),试求:
(1)生成的沉淀的最大值是多少_________?
(2)原合金中Mg的质量百分含量_________(计算结果保留一位小数点)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com