
【题目】某温度时,在一个0.5L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.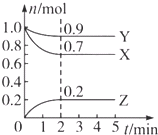
根据图中数据回答下列问题:
(1)该反应的化学方程式为 .
(2)反应开始至2min,以气体Z表示的平均反应速率为 .
(3)用物质X表示的化学反应速率为0.2molL﹣1s﹣1与用物质Y表示的化学反应速率为0.1molL﹣1s﹣1 , 哪个快?
a.前者b.后者c.一样快d.无法比较
(4)若X、Y、Z均为气体,2min后反应达到平衡,反应达平衡时:
①此时体系的压强是开始时的倍;
②达平衡时,容器内混合气体的平均相对分子质量比起始投料时(填“增大”“减小”或“相等”).
【答案】
(1)3X+Y=2Z
(2)0.2mol?L﹣1?min﹣1
(3)b
(4)0.9;增大
【解析】(1)由图象可以看出,X、Y的物质的量逐渐减小,Z的物质的量逐渐增大,则X、Y为反应物,Z为生成物,2min后,X、Y的物质的量为定值且不为零,为可逆反应,相同时间内物质的量的变化比值为:△n(X):△n(Y):△n(Z)=(1.0﹣0.7)mol:(1.0﹣0.9)mol:0.2mol=3:1:2,则化学方程式为3X+Y ![]() 2Z,所以答案是:3X+Y
2Z,所以答案是:3X+Y ![]() 2Z;(2)反应开始至2min,气体Z的平均反应速率为v=
2Z;(2)反应开始至2min,气体Z的平均反应速率为v= ![]() =0.05mol/(L.min),
=0.05mol/(L.min),
所以答案是:0.05mol/(L.min);(3)根据速率之比等于化学计量数之比换算成用X物质表示的速率来,前者物质X表示的化学反应速率为0.2molL﹣1s﹣1 , 后者用物质Y表示的化学反应速率为0.1molL﹣1s﹣1换算成用X表示速率为:0.3molL﹣1s﹣1 , 故后者反应快,所以答案是:b;(4)①反应达平衡时,气体的总物质的量为:0.9mol+0.7mol+0.2mol=1.8mol,起始时气体的总物质的量为1.0mol+1.0mol=2.0mol,反应达平衡时,此时容器内的压强与起始压强之比为1.8mol:2.0mol=9:10,此时体系的压强是开始时的 0.9倍,
所以答案是:0.9.
②平衡时,混合气体的平均摩尔质量为 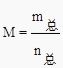 ,气体的总质量不变,总物质的量减少,混合气体的平均摩尔质量增大,所以答案是:增大.
,气体的总质量不变,总物质的量减少,混合气体的平均摩尔质量增大,所以答案是:增大.
【考点精析】根据题目的已知条件,利用反应速率的定量表示方法和化学平衡的计算的相关知识可以得到问题的答案,需要掌握反应速率的单位:mol/(L·min)或mol/(L·s) v=△c-△t;反应物转化率=转化浓度÷起始浓度×100%=转化物质的量÷起始物质的量×100%;产品的产率=实际生成产物的物质的量÷理论上可得到产物的物质的量×100%.


 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:
【题目】
(1)如图所示的装置在实验室中用途比较广泛: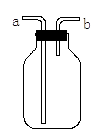
①排空气法收集气体,若收集CO2气体,进气口为 (填“a”或“b”)。
②若瓶中装满水,可用于收集下列气体中的(选填编号)。
A、NO B、NO2 C、NH3 D、HCl
此时进气口为(填“a”或“b”)。
③如果广口瓶中盛放浓硫酸,可用作气体干燥装置,则该装置不可以干燥的气体有(选填编号)。
A、HCl B、NH3 C、H2 D、CO
④此装置还可用于除去气体中的杂质气体。若要用此装置除去CO2中混有的少量SO2气体,则装置中应盛放的液体可能是(选填编号)。
A、NaOH溶液 B、饱和Na2CO3溶液 C、饱和NaHCO3溶液 D、浓H2SO4
(2)下面是中学化学实验中常见的几种仪器:
A.量筒 B.容量瓶 C.试管 D.圆底烧瓶 E.托盘天平
①其中仪器上要标出使用温度的是(填选项)
②可用作反应容器并能进行加热的是(填选项)
③下列操作,使得实验结果偏小的是(填选项)
A.称取5.2 gNaCl固体时,将砝码放在左盘,NaCl固体放在右盘
B.配制一定物质的量浓度的NaCl溶液,转移NaCl溶液前,容量瓶中已有少许蒸馏水
C. 配制一定物质的量浓度的NaCl溶液,定容时俯视读数。
D.用量筒量取一定体积的浓硫酸,浓硫酸倒入烧杯后,用蒸馏水继续冲洗量筒内壁并将洗涤液倒入烧杯。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积为2L密闭容器中加入反应物A、B,发生如下反应:A+2B=3C.经2min后,A的浓度从开始时的1.0molL﹣1 降到0.8molL﹣1 . 已知反应开始时B的浓度是1.2molL﹣1 . 则:2min末B的浓度mol/L , C的物质的量mol . 2min内,用A物质的浓度变化来表示该反应的反应速率,即V(A)=mol/(L.min) .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.据此下列说法正确的是( ) 
A.该试剂的物质的量浓度为9.2molL﹣1
B.该硫酸50mL与足量的铜反应可得到标准状况下SO2 10.3L
C.配制50mL 4.6molL﹣1的稀硫酸需取该硫酸12.5mL
D.该硫酸与等体积的水混合所得溶液的质量分数小于49%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,向a L密闭容器中加入1mol X气体和2mol Y气体,发生如下反应:X(g)+2Y(g)2Z(g),此反应达到平衡的标志是( )
A.容器内气体密度不随时间变化
B.v(X):v(Y)=1:2
C.容器内X、Y、Z的浓度不随时间变化
D.单位时间消耗0.1molX同时生成0.2molZ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在1.0L密闭容器中放入0.10 mol X,在一定温度下发生反应:X(g)Y(g)+Z(g)△H<0容器内气体总压强p随反应时间t的变化关系如图所示.以下分析正确的是( ) 
A.从反应开始到t1时的平均反应速率v(X)= ![]() mol/(Lmin)
mol/(Lmin)
B.该温度下此反应的平衡常数K=0.32
C.欲提高平衡体系中Y的含量,可升高体系温度或减少Z的量
D.其他条件不变,再充入0.1 mol 气体X,平衡正向移动,X的转化率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤化工中常需研究不同温度下平衡常数、投料比及热值等问题.已知:CO(g)+H2O(g)H2(g)+CO2(g)平衡常数随温度的变化如下表:
温度/℃ | 400 | 500 | 800 |
平衡常数K | 9.94 | 9 | 1 |
试回答下列问题
(1)上述正向反应是反应 (填“放热”或“吸热”)
(2)要使上述反应的逆反应速率增大且平衡正反应方向移动,下列措施不可行的有( )
A.加入催化剂
B.增大CO的物质的量以提高体系的压强
C.降低温度
D.减小H2的浓度
(3)向某密闭容器中充入2molCO和4molH2O(g),发生反应:CO(g)+H2O(g)H2(g)+CO2(g),当反应达平衡时,CO的体积分数为X,若维持容器的体积和温度不变,起始物质按下列四种配比充入该容器中,达到平衡时CO的体积分数不等于X的有( )
A.1molCO(g)+4molH2O+2molCO2(g)+2molH2(g)
B.2molCO(g)+2molH2O+2molCO2(g)+2molH2(g)
C.1molCO(g)+3molH2O+0.8molCO2(g)+0.8molH2(g)
D.1molCO(g)+3molH2O+1molCO2(g)+1molH2(g)
(4)若反应在800℃时进行,设起始CO和H2O(g)共为5mol,水蒸气的体积分数为X;平衡时CO的转化率为y,则y随x变化的函数关系式为y=
(5)在VL密闭容器中通入10mol CO和10mol水蒸气,在T℃达到平衡,然后急速通过碱石灰,将所得混合气体燃烧,测得放出的热量为2845KJ(已知CO燃烧热为283KJ/mol,H2燃烧热为286KJ/mol),则T℃平衡常数K= , T= K (0℃时T=273K)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com