
| A. | 全部可以 | B. | 仅①不可以 | C. | 仅②可以 | D. | 仅③可以 |
分析 ①铜与氯化铁溶液发生化学反应;
②甲、乙两短周期元素原子的电子层数相同,二者同周期,随原子序数增大金属性减弱;
③金属性强弱与失去电子难易程度有关,与失去电子数目多少无关.
解答 解:①铜与氯化铁溶液发生化学反应,但铁比铜活泼,故①错误;
②甲、乙两短周期元素原子的电子层数相同,二者同周期,随原子序数增大金属性减弱,甲的原子序数小于乙的原子序数,则金属性甲比乙的强,故②正确;
③金属性强弱与失去电子难易程度有关,与失去电子数目多少无关,如Mg失去2个电子、Na失去1个电子,但金属性Na>Mg,故③错误,
故选:C.
点评 本题考查元素周期律应用,掌握金属性、非金属性强弱比较实验事实,注意利用反例法进行解答,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 10 | B. | 9 | C. | 8 | D. | 11 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 玻璃容器可长期盛放各种酸 | B. | 浓氨水可检验氯气管道泄漏 | ||
| C. | 浓硫酸可刻蚀石英制艺术品 | D. | 84消毒液的有效成分是NaClO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 第3列元素种类最多,第14列元素形成的化合物种类最多 | |
| B. | 每一列都有非金属元素 | |
| C. | 从上到下第1列元素的单质熔点逐渐升高,而第17列元素的单质熔点逐渐降低 | |
| D. | 只有第2列元素的原子最外层有2个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4+、Cl-、K+、NO3- | B. | CO32-、Na+、Cl-、K+ | ||
| C. | Fe3+、Mg2+、NO3-、Cl- | D. | Na+、Ag+、NO3-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

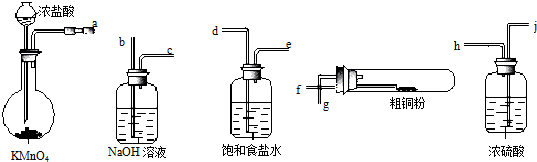
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
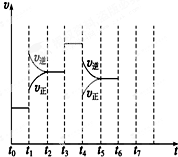 在一密闭容器中发生反应N2+3H22NH3,△H<0达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示:回答下列问题:
在一密闭容器中发生反应N2+3H22NH3,△H<0达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示:回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
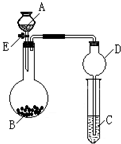 某同学设计了如图所示装置(夹持仪器省略)进行系列实验,实验时将药品A逐滴加入到固体B中,请根据下列实验回答问题:
某同学设计了如图所示装置(夹持仪器省略)进行系列实验,实验时将药品A逐滴加入到固体B中,请根据下列实验回答问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com