
| A. |  设计铜锌原电池 | B. |  制备氢氧化亚铁并观察其颜色 | ||
| C. | 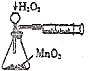 定量测定H2O2的分解速率 | D. | 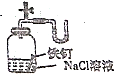 证明铁生锈与空气有关 |
分析 A.离子不能向两极定向移动;
B.氢氧化亚铁易被氧化;
C.生成气体从长颈漏斗逸出;
D.铁钉在氯化钠溶液中发生吸氧腐蚀.
解答 解:A.没有形成闭合回路,离子不能向两极定向移动,不能形成原电池,应用盐桥代替铜丝,故A错误;
B.胶头滴管滴入液体时易携带氧气,氢氧化亚铁易被氧化,故B错误;
C.生成气体从长颈漏斗逸出,不能测定单位内收集的气体的体积,故C错误;
D.铁钉在氯化钠溶液中发生吸氧腐蚀,广口瓶内压强减小,则U形管压面发生变化,可证明氧气参加反应,故D正确.
故选D.
点评 本题综合考查化学基本操作,涉及原电池、反应速率的测定以及制备等操作,为高考常见题型,侧重于学生化学设计和评价的能力的考查,难度不大.


科目:高中化学 来源: 题型:选择题
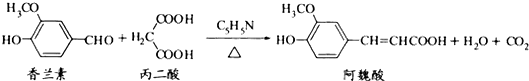
| A. | 与香兰素互为同分异构体,分子中有5种不同化学环境的氢,且能发生银镜反应的酚类化合物有2种 | |
| B. | 香兰素、阿魏酸均可与NaHCO3、NaOH溶液反应 | |
| C. | 通常条件下,香兰素、阿魏酸都能发生取代、加成、消去反应 | |
| D. | 香兰素、阿魏酸均可与溴水反应,且反应类型完全相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 周期/族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ○ |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ⑪ | ⑫ |
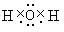 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molNa与O2完全反应生成Na2O2和Na2O的混合物,转移电子的总数为NA | |
| B. | 室温下,31.0g白磷中含有的共价键数目为1.5NA | |
| C. | 常温常压下,17g甲基(-14CH3)含有的电子数为9NA | |
| D. | 常温下,1.0L pH=13的NaOH溶液中,由水电离的OH-离子数目为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 用如图所示的装置进行实验,反应一段时间后断开K,向右侧烧杯中加入0.1molCuO后CuSO4溶液恰好恢复到反应前的浓度和pH.下列说法中不正确的是( )
用如图所示的装置进行实验,反应一段时间后断开K,向右侧烧杯中加入0.1molCuO后CuSO4溶液恰好恢复到反应前的浓度和pH.下列说法中不正确的是( )| A. | 铜棒为正极,其电极反应式为2H++2e-═H2↑ | |
| B. | 烧杯右侧碳棒为阴极,其电极表面有红色物质析出 | |
| C. | 反应中消耗锌的质量为13g | |
| D. | 导线中通过的电子的物质的量为0.2mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | △H3+2△H1+2△H2 | B. | △H3+2△H1+△H2 | C. | △H3+2△H1-△H2 | D. | △H3+2△H1-2△H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3molH2+2molN2 | B. | 2molNH3+1molN2 | ||
| C. | 3molN2+1molH2 | D. | 0.1molNH3+0.95molN2+2.85molH2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 纯铁的抗腐蚀能力比生铁强 | |
| B. | 可用酒精洗涤附着在试管内壁上的固态硫 | |
| C. | 用惰性电极电解熔融NaCl可获得金属钠 | |
| D. | 二氧化硅能与NaOH溶液反应,所以盛放碱液的试剂瓶不能用磨口玻璃塞 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com