
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A. 0.1 mol丙烯酸中含有的双键数目为0.1NA
B. 常温常压下,4.6 g NO2和N2O4的混合气体中分子总数为0.3NA
C. 标准状况下,2.24 L Cl2溶于足量的水中充分反应后,溶液中Cl-数为0.2NA
D. 7.8 g Na2O2和Na2S的固体混合物中含有的离子总数为0.3NA
【答案】D
【解析】
A. 1mol丙烯酸中含2mol双键;
B.二氧化氮、四氧化二氮摩尔质量不同;
C.氯气与水反应生成HCl和HClO,且为可逆反应;
D.过氧化钠阳离子为钠离子,阴离子为过氧根离子。
A.丙烯酸中含碳碳双键和碳氧双键,故1mol丙烯酸中含2mol双键,即0.1mol丙烯酸中含有双键的数目为0.2NA,故A错误;
B.二氧化氮、四氧化二氮摩尔质量不同,只知道混合物总质量无法计算混合气体物质的量,无法计算分子个数,故B错误;
C.标准状况下,2.24LCl2物质的量为![]() =0.1mol,与足量水反应,溶液中Cl-数小于0.2NA,故C错误;
=0.1mol,与足量水反应,溶液中Cl-数小于0.2NA,故C错误;
D、Na2S和Na2O2摩尔质量相同,过氧化钠是由钠离子和过氧根离子构成,7.8g Na2S和Na2O2的混合物物质的量为0.1mol,含有的离子总数为0.3NA,所以D选项是正确的。
故答案选D。


 华东师大版一课一练系列答案
华东师大版一课一练系列答案科目:高中化学 来源: 题型:
【题目】300 ℃时,将2 mol A和2 mol B两种气体混合于2 L密闭容器中,发生如下反应:3A(g)+B(g)![]() 2C(g)+2D(g) ΔH=Q,2 min末达到平衡,生成0.8 mol D。
2C(g)+2D(g) ΔH=Q,2 min末达到平衡,生成0.8 mol D。
(1)300 ℃时,该反应的平衡常数表达式为:K=___________________。已知K300 ℃<K350 ℃,则ΔH______0(填“>”或“<”)。
(2)在2 min末时,B的平衡浓度为________,D的平均反应速率为________。
(3)若温度不变,缩小容器容积,则A的转化率______(填“增大”“减小”或“不变”),原因是_____________________________________________________________。
(4)如果在相同的条件下,上述反应从逆反应方向进行,开始时加入C、D各4/3mol。若使平衡时各物质的物质的量浓度与原平衡相同,则还应该加入B______mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由下列实验操作及现象能得出相应结论的是
操作 | 现象 | 结论 | |
A. | 将蘸有浓氨水的玻璃棒靠近某溶液 | 有白烟产生 | 该溶液一定为浓盐酸 |
B. | 向 CH3COONa 溶液中滴入酚酞试液,加热 | 加热后红色加深 | CH3COONa 水解是吸热反应 |
C. | 向某溶液中加入盐酸,将产生 的气体通入澄清石灰水 | 澄清石灰水变浑浊 | 该溶液中一定有 CO32— |
D. | 向 NaCl 溶液中滴加过量 AgNO3 溶液,再滴加 KI 溶液 | 先出现白色沉淀, 后出现黄色沉淀 | Ksp(AgI) < Ksp(AgCl) |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮及其化合物如NH3及铵盐、N2H4、N2O4等在中学化学、化工工业、国防等领域占有重要地位。
(1)已知反应NO2(g)+CO(g) = NO(g) +CO2(g)的能量变化如上图所示,下列说法正确的是________。
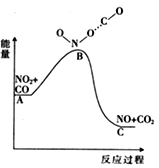
A.图中A→B的过程为放热过程
B.1molNO2和1molCO的键能总和大于1molNO和1molCO2的键能总和
C.该反应为氧化还原反应
D.1molNO2(g)和1molCO(g)的总能量低于1molNO(g)和1molCO2(g)的总能量
(2)N2O4与NO2之间存在反应N2O4(g)![]() 2NO2(g)。将一定量的N2O4放入恒容密闭容器中,测得其平衡转化率[α(N2O4)]随温度的变化如图所示。
2NO2(g)。将一定量的N2O4放入恒容密闭容器中,测得其平衡转化率[α(N2O4)]随温度的变化如图所示。
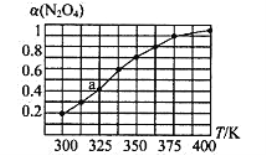
①由图推测该反应的△H___0(填“>”或“<”),理由为________________。
②图中a点对应温度下,已知N2O4的起始压强为108 kPa,则该温度下反应的平衡常数Kp=_________kPa(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
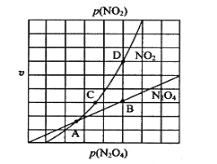
③在一定条件下,该反应N2O4、NO2的消耗速率与自身压强间存在关系υ( N2O4)=k1p(N2O4),υ(NO2)=k2p2(NO2),其中k1、k2是与反应温度有关的常数。相应的速率压强关系如图所示,一定温度下,k1、k2与平衡常数Kp的关系是k1=___________,在下图上标出的点中,能表示反应达到平衡状态的点为__________(填字母代号)。
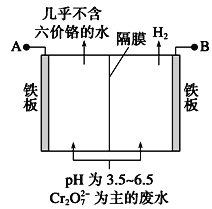
(3)采用电解法处理含铬废水原理如下图所示。阳极的电极反应式为___________,阳极区溶液中发生反应: ________________________,阴极产生的气体为_______(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生利用下面实验装置探究盐桥式原电池的工作原理(Cu:相对原子质量为64)。

按照实验步骤依次回答下列问题:
(1)导线中电流方向为__________________(用a、b表示)。
(2)原电池的正极为___________
(3)写出装置中铜电极上的电极反应式:____________________________________;
(4)若装置中铜电极的质量增加32 g,则导线中转移的电子数目为________;
(5)装置的盐桥中除添加琼脂外,还要添加KCl的饱和溶液,电池工作时,盐桥中的K+向______(填“左侧”或“右侧”)烧杯移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是
A. 硅酸钠溶液与盐酸的反应:Na2SiO3+2H+===H2SiO3↓+2Na+
B. 用KIO3氧化酸性溶液中的KI:5I-+IO3-+3H2O===3I2+6OH-
C. 饱和Na2CO3溶液与CaSO4固体反应:CO32+CaSO4![]() CaCO3+SO42
CaCO3+SO42
D. 向NaHCO3溶液中滴加少量Ba(OH)2溶液:Ba2++OH-+HCO3—===BaCO3↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求表达下列变化过程中的化学用语,写化学方程式,其中(4)(5)写出反应的离子方程式。
⑴金属镁在CO2中燃烧_______________________
⑵加热碳酸氢钠固体___________________
⑶过氧化钠与水的反应________________
⑷KCl溶液与AgNO3溶液反应____________
⑸钠与硫酸铜溶液反应__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知2H2(g)+O2(g)=2H2O(l) ΔH=-569.6kJ/mol,2H2O(g)=2H2(g)+O2(g) ΔH=+482.1 kJ/mol。现有1g液态H2O,蒸发时吸收的热量是 ( )
A. 2.43 kJ B. 4.86 kJ C. 43.8 kJ D. 87.5 kJ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com