
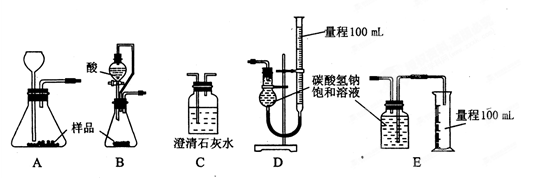
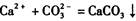 的反应设计了如下方案:称取样品→配成溶液→加入足量浓CaCl2溶液→充分反应后过滤→洗涤→干燥→称量→计算纯度。
的反应设计了如下方案:称取样品→配成溶液→加入足量浓CaCl2溶液→充分反应后过滤→洗涤→干燥→称量→计算纯度。


科目:高中化学 来源:不详 题型:实验题
| 装置 | 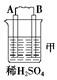 | 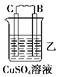 | 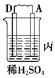 |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
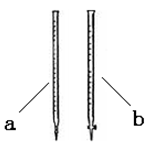
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 NaCl杂质,为测
NaCl杂质,为测 定样品中纯碱的质量分数,甲同学用下图装置及试剂进行实验(夹持仪器略)。填写下列空白处。
定样品中纯碱的质量分数,甲同学用下图装置及试剂进行实验(夹持仪器略)。填写下列空白处。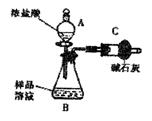
 可重复使用,夹持仪器略)
可重复使用,夹持仪器略)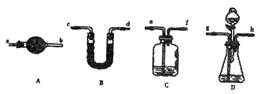
选用的 仪器 仪器 | | | | | |
| 添加的药品及必要的操作 | | | | | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 滴定次数 | 盐酸体积(mL) | NaOH溶液体积读数(mL) | |
| 滴定前 | 滴定后 | ||
| 1 | 20.00 | 0.00 | 18.10 |
| 2 | 20.00 | 0.00 | 16.30 |
| 3 | 20.00 | 0.00 | 16.22 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.配制NaOH标准液时,所用的NaOH固体中含有少量的KOH杂质 |
| B.滴定前对碱式滴定管仰视读数,滴定后又俯视 |
| C.滴定前,碱式滴定管尖嘴部分有气泡,滴定后气泡消失 |
| D.碱式滴定管用蒸馏水洗净后,直接装入标准NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| | 操作 | 现象 | 结论 |
| A | 用CH3COOH溶液浸泡水垢 | 水垢溶解,有无色气泡 | 酸性:CH3COOH>H2CO3 |
| B | 测定等浓度的Na2CO3和Na2SO3溶液的pH | 前者pH比后者的大 | 非金属性:S>C |
| C | 向FeBr2溶液中通入过量Cl2 | 溶液由浅绿色变成黄色 | 氧化性:Br2>Fe3+ |
| D | 用石墨电极电解滴有酚酞的饱和NaCl溶液 | 在阴极附近溶液呈现红色 | 离子移动方向:OH-移向阴极 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 滴定 次数 | 待测溶液的体积/mL | 标准溶液的体积 | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 0.20 | 20.20 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 烯中碳、氢两种元素的质量比。
烯中碳、氢两种元素的质量比。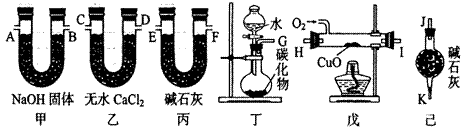
 方程式: 。
方程式: 。 。
。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com