
【题目】下列关于化学元素的叙述,错误的是( )
A. 在你的身体中,含量最高的化学元素是O
B. 沙漠中仙人掌,含量最多的化合物和含量最多的有机物共有的元素是H和O
C. 组成蛋白质的元素都是大量元素
D. 活细胞中的主要元素是C、H、O、N、P、S
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z是原子序数依次增大的短周期元素.W的最外层电子数是电子层数的2倍.Y是金属,可以和X形成1:1和2:1两种化合物.Z的最高正价与最低负价的代数和为4.
(1)写出WX2的电子式 .
(2)用元素符号表示X、Y、Z原子半径由大到小的顺序 > > .
(3)含1molZ的最高价氧化物对应水化物的稀溶液与足量Y的最高价氧化物对应水化物的稀溶液反应放出热量114.6kJ,写出此反应的热化学方程式: .
(4)在一定量Y的最高价氧化物对应水化物的稀溶液中通入过量WX2,用离子浓度表示该溶液中的电荷守恒 .
(5)Y2ZX4与WX、H2在高温和铁做催化剂条件下反应,0.1molY2ZX4参加反应转移0.8mol电子,消耗标况下H2的体积为4.48L,该反应的化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于氨基酸和蛋白质的叙述,错误的是( )
A. 甲硫氨酸的R基是-CH2-CH2-S-CH3,则它的分子式是C5H11O2NS
B. 分子式为C63H105O45N17S2的多肽化合物中,最多含有肽键17个
C. 两个氨基酸脱水缩合过程中失去的H2O中的氢来源于氨基和羧基中的氢
D. 如果有足量的三种氨基酸甲、乙、丙,则他们能形成三肽种类最多有6种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述不相符的是( )

A.图1表示KNO3的溶解度曲线,图中a点所示的溶液是80℃时KNO3的不饱和溶液
B.图2表示某放热反应分别在有、无催化剂的情况下反应过程中的能量变化
C.图3表示0.1000molL﹣1NaOH溶液滴定20.00mL0.1000molL﹣1醋酸溶液得到滴定曲线
D.图4 表示向NH4Al(SO4)2溶液中逐滴滴入Ba(OH)2溶液,随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下,ag气体A与bg气体B的分子数相同,下列说法中不正确的是( )
A.同温同压下A、B两气体的密度之比为a:b
B.同质量气体A与B的分子数之比为b:a
C.两种气体A与B的相对分子质量之比为b:a
D.相同状况下同体积A、B质量之比为a:b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为有效控制雾霾,各地积极采取措施改善大气质量,研究并有效控制空气中的氮氧化物、碳氧化物和硫氧化物含量显得尤为重要。
I.汽车内燃机工作时会引起N2和O2的反应:N2+O2![]() 2NO,是导致汽车尾气中含有NO的原因之一。
2NO,是导致汽车尾气中含有NO的原因之一。
(1)在T1、T2温度下,一定量的NO发生分解反应时N2 的体积分数随时间变化如右图所示,根据图像判断反应N2(g)+O2(g)![]() 2NO(g)的△H__________0(填“>"或“ <”)。
2NO(g)的△H__________0(填“>"或“ <”)。

(2)在T3温度下,向2L密闭容器中充入10molN2与5molO2,50秒后达到平衡,测得NO的物质的量为2mol,则该反应的速率v(N2)_________。该温度下,若增大压强此反应的平衡常数将____________(填“增大”、“减小”、“不变”或“无法确记”);若开始时向上述容器中充入N2与O2均为1 mol,则达到平衡后O2的转化率为__________。
II.甲烷和甲醇可以做燃料电池,具有广阔的开发和应用前景,回答下列问题
(3)甲醇燃料电池(简称DMFC )由于结构简单、能量转化率高、对环境无污染,可作为常规能源的替代品而越来越受到关注。DMFC工作原理如右图所示:
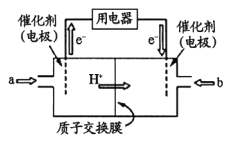
通入a气体的电极是原电池的____________极(填“正”或“负”),其电极反应式为_______________。
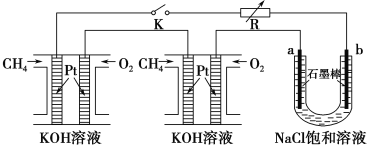
(4)某研究小组将两个甲烷燃料电池串联后作为电源,进行饱和氯化钠溶液电解实验,如图所示U形管中氯化钠溶液的体积为800ml。闭合K后,若每个电池甲烷用量为0.224L (标况),且反应完全,则理论上通过电解池的电量为 __________(法拉第常数F=9.65×104C/mol),若产生的气体全部逸出,电解后溶液混合均匀,电解后U形管中溶液的pH为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(化学---选修:5:有机化学基础)H是一种新型香料的主要成分之一,其结构中含有三个六元环。H的合成路线如下(部分产物和部分反应条件略去):

①![]()
②B中核磁共振氢谱图显示分子中有6种不同环境的氢原子。
③D和G是同系物
请回答下列问题:
(1)用系统命名法命名(CH3)2C=CH2:___________________。
(2)A→B反应过程中涉及的反应类型有____________________。
(3)写出D分子中含有的官能团名称:
(4)写出生成F与足量氢氧化钠溶液在加热条件下反应的化学方程式____________。
(5)写出E在铜催化下与O2反应的化学方程式:_____________________。
(6)同时满足下列条件:①与FeCl3溶液发生显色反应;②能发生水解反应;③苯环上有两个取代基的G的同分异构体有 种(不包括立体异构),其中核磁共振氢谱为5组峰的为 (写结构简式)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用50mL 0.50 mol/L盐酸与50 mL 0.55 mol/L NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:

(1)观察实验装置,图中尚缺少的一种玻璃用品是__________。
(2)烧杯间填满碎纸条的作用是_________________________。
(3)大烧杯上如不盖硬纸板,测得的中和热数值 __________(填“偏大、偏小、无影响”)。
(4)实验中改用55mL 0.50 mol/L盐酸与55mL 0.55 mol/L NaOH溶液进行反应,与上述实验相比,所放出的热量__________ (填“相等、不相等”),所求中和热__________ (填“相等、不相等”)。
(5)在中和热测定实验中,若用相同浓度和体积的氨水代替NaOH溶液进行实验,测得的中和热的数值会________ (填“偏大”、“偏小”“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 用于纺织的棉花和蚕丝的主要成分是纤维素
B. 美国化学家科里提出了同位素示踪法,对反应历程的研究贡献突出
C. 糖类,油脂,蛋白质都是高分子化合物
D. 李比希创立了有机物的定量分析方法
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com